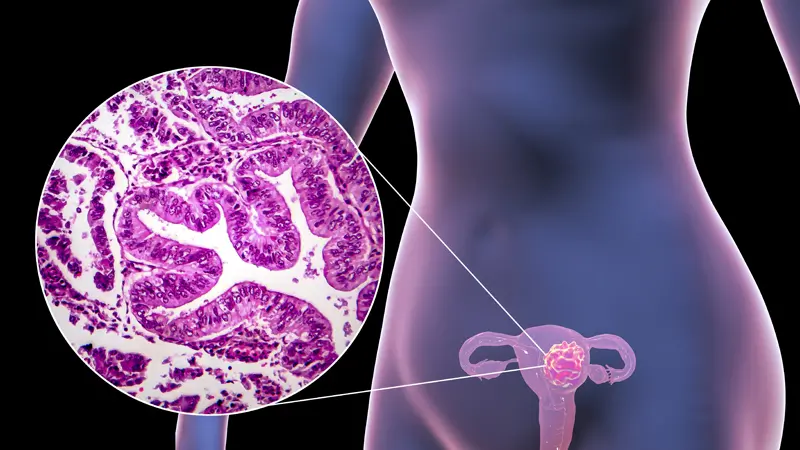
摘要 美国食品药品监督管理局(FDA)授予前沿药CTX-009与紫杉醇联合,用于先前接受过治疗的转移性或局部晚期胆道癌患者的快速通道认定。 注:快速通道认定(FTD)是美国食品药品监督管理局(FDA)提供的一种制度,旨在促进新药的开发和审批,尤其是针对治疗严重或威胁生命的药物。该认定旨在加速这些药物的研发、审批和上市,以更迅速地满足患者的医疗需求。 来源:摄图网 关键信息如下: 1.CTX-009是由美国生物制药公司Compass Therapeutics研发的一款双特异性抗体药物,靶向DLL4和VEGF-A,在先前的研究中证实,在多种实体瘤中具有抗肿瘤活性。 2.围绕CTX-009与紫杉醇联合用于晚期胆道癌患者的2期试验中,已经观察到了令人鼓舞的初步疗效,24名患者中,有9名患者肿瘤大幅缩… Read More... "美国前沿药CTX-009与紫杉醇联合获快速通道认定,用于晚期胆道癌患者"
摘要 近日,美国MD安德森癌症中心早期药物开发和1期临床试验主任、妇科肿瘤学和生殖医学系教授威斯汀,在接受采访时介绍了一款前沿WEE1抑制剂在妇科恶性肿瘤患者中的众多研究信息。 来源:摄图网 关键信息如下: 1.美国前沿WEE1抑制剂Azenosertib,在妇科恶性肿瘤的单药临床研究中表现良好,尤其是治疗高级别浆液性卵巢癌患者,对所有人都有效,部分患者肿瘤大幅缩小。 2.Azenosertib采用的是非常前沿的“合成致死”机制,对于TP53基因突变的肿瘤可能存在良好治疗效果。而TP53突变又是癌症当中极为常见的靶点,未来可能有大量患者凭借该药受益。 研究详情 (专业人士阅读) 近日,美国MD安德森癌症中心早期药物开发和1期临床试验主任、妇科肿瘤学和生殖医学系教授威斯汀,在接受采访时介绍了一… Read More... "美国前沿WEE1抑制剂,剑指TP53突变型卵巢癌,疗效喜人!"
摘要 近日,美国食品药品监督管理局(FDA)已完全批准Tivdak(Tisotumab vedotin-tftv)用于治疗化疗期间或化疗后疾病进展的复发性或转移性宫颈癌患者。 来源:摄图网 关键信息如下: 1.美国前沿药Tisotumab vedotin获得了美国食品药品监督管理局(FDA)的完全批准,用于治疗化疗进展的复发性或转移性宫颈癌患者。 2.该药在临床试验中,无论是疾病控制还是肿瘤缓解,各方面治疗数据都比化疗更好,给原本非常缺少有效治疗方案的宫颈癌患者带来了新的良好治疗选择。 研究详情 (专业人士阅读) 近日,美国食品药品监督管理局(FDA)已完全批准Tivdak(Tisotumab vedotin-tftv)用于治疗化疗期间或化疗后疾病进展的复发性或转移性宫颈癌患者。 这项批准决… Read More... "美国前沿药Tivdak,获批治疗复发性或转移性宫颈癌患者"
摘要 美国ImmunityBio公司宣布:根据一项2b期研究的数据结果,前沿药Anktiva联合免疫检查点抑制剂,将晚期非小细胞肺癌(NSCLC)患者的平均总生存期,几乎翻了一倍! 来源:参考资料[1] 关键信息如下: 1.该联合疗法具体针对接受免疫检查点抑制剂和化疗后疾病进展的非小细胞肺癌(NSCLC)患者。 2.无论患者的PD-L1状态如何,该联合疗法均展现出了积极疗效。 3.Anktiva刚刚获得美国食品药品监督管理局(FDA)的批准,与卡介苗联合用于非肌层浸润性膀胱癌(NMIBC)患者,该药还有很大潜力,有望对多种实体瘤产生良好疗效,为更多晚期癌症患者带来新希望。 研究详情 (专业人士阅读) 美国ImmunityBio公司宣布:根据2b期QUILT-3.055研究(NCT032286… Read More... "美国前沿药Anktiva联合免疫检查点抑制剂,显著改善晚期非小细胞肺癌患者总生存期"
摘要 美国食品药品监督管理局(FDA)加速批准Ojemda,用于6个月及以上的复发或难治性儿童低级别胶质瘤患者,患者携带BRAF融合或重排,或者BRAF V600突变。 Ojemda是由美国生物制药公司Day One研发的一款口服II型RAF抑制剂。 来源:摄图网 关键信息如下: 1.Ojemda共取得了51%的客观缓解率,即有51%的患者肿瘤大幅缩小或消失。 2.在2023年6月5日的数据截止日期,平均缓解持续时间(DOR)为13.8个月。 3.对于携带BRAF融合或重排的患者,Ojemda共取得了52%的客观缓解率,即有52%的患者肿瘤大幅缩小或消失。 4.对于携带BRAF V600突变的患者,Ojemda共取得了50%的客观缓解率,即有50%的患者肿瘤大幅缩小或消失。 研究详情… Read More... "51%的患者肿瘤大幅缩小或消失,儿童胶质瘤新疗法Ojemda在美国获批"
摘要 美国食品药品监督管理局(FDA)已批准美国ImmunityBio公司的前沿药Anktiva与卡介苗联合,用于对卡介苗治疗无效且伴有原位癌的非肌层浸润性膀胱癌(NMIBC)患者。 来源:摄图网 关键信息如下: 1.该疗法取得了62%的完全缓解率(CR),即有62%的患者肿瘤完全消失。 2.在获得完全缓解(CR)的患者中,有58%的患者治疗后至少一年疾病没有出现复发或进展,有40%的患者治疗后至少两年疾病没有出现复发或进展。 3.该疗法的安全性良好。 研究详情 (专业人士阅读) 美国食品药品监督管理局(FDA)已批准ogapendekin alfa inbakicept-pml(商品名Anktiva)与卡介苗(BCG)联合,用于对卡介苗治疗无效且伴有原位癌(CIS)的非肌层浸润性膀胱癌… Read More... "62%的患者肿瘤完全消失,膀胱癌新疗法在美国正式获批上市"
摘要 根据2024年美国癌症研究协会(AACR)年会上发布的研究表明,美国前沿“冷冻溶瘤疗法”SYNC-T,对于转移性去势抵抗性前列腺癌患者显示出良好的抗肿瘤活性,84.6%的患者肿瘤大幅缓解(缩小或消失),38.5%的患者肿瘤全消失。 来源:摄图网 关键信息如下: 1.转移性去势抵抗性前列腺癌患者极度缺少有效治疗方案,因此SYNC-T疗法的出现,对这部分患者来说毫无疑问是雪中送炭。 2.研究显示,使用美国SYNC-T疗法的患者无人病情进展,其中有84.6%的患者肿瘤大幅缩小或消失,其中大幅缩小的人占比46.1%,剩下38.5%的人肿瘤全消失, 研究详情 (专业人士阅读) 根据2024年美国癌症研究协会(AACR)年会上发布的研究表明,美国前沿溶瘤+免疫新型组合疗法SYNC-T,对于转移性去… Read More... "美国“冷冻溶瘤疗法”,让38.5%的转移性前列腺癌患者肿瘤全消失!"
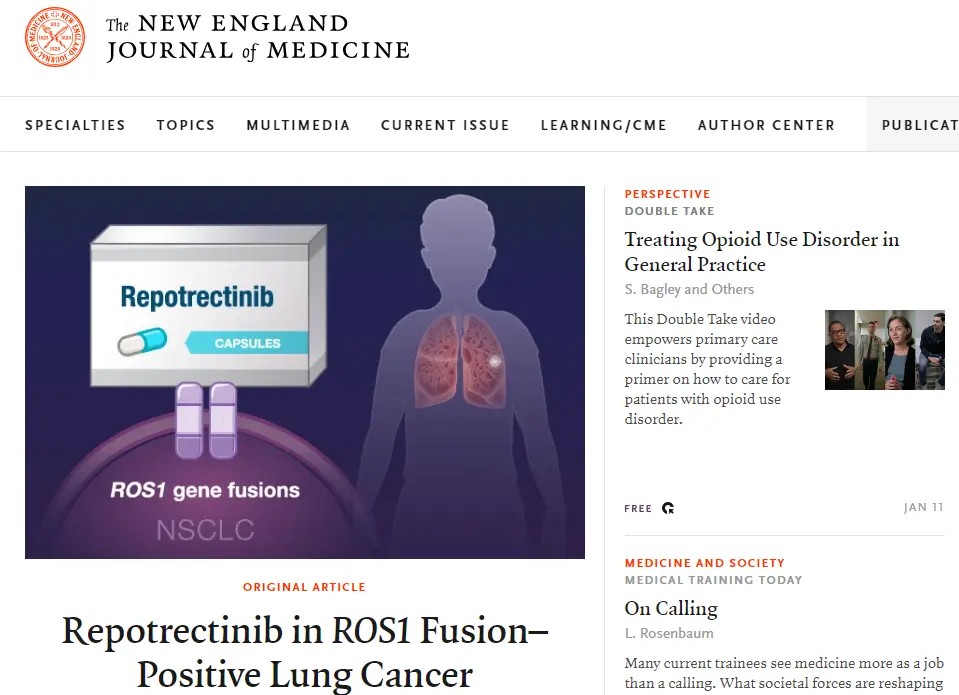
摘要 近日,全球知名医学期刊《新英格兰医学杂志》(NEJM)重磅发布了全球制药公司百时美施贵宝的肺癌前沿靶向药Repotrectinib的1/2期临床试验新进展,详细阐述了该药在ROS1融合阳性非小细胞肺癌患者中的应用情况。 来源:《新英格兰医学杂志》(NEJM)官网截图 关键信息如下: 1.Repotrectinib在ROS1融合阳性非小细胞肺癌患者中效果显著,无论患者先前是否接受过ROS1 TKI(酪氨酸激酶抑制剂)治疗。 2.在先前未曾接受过ROS1 TKI(酪氨酸激酶抑制剂)治疗的ROS1融合阳性非小细胞肺癌患者中,有79%的患者接受Repotrectinib治疗后肿瘤大幅缩小或消失。 3.该药的安全性也很良好,患者出现的大多是比较轻微的副作用,适合长期使用。 研究详情 (专业人士阅… Read More... "近八成患者肿瘤大幅缩小或消失,美国肺癌前沿药Repotrectinib公布临床试验新进展"
摘要 美国食品药品监督管理局(FDA)授予美国生物技术公司CG Oncology的溶瘤病毒疗法Cretostimogene Grenadenorepvec用于膀胱癌患者的的快速通道和突破性疗法双重认定。该疗法疗效惊艳,在一项3期试验中,使得高达75.7%的患者肿瘤完全消失。 来源:摄图网 关键信息如下: 1.在一项3期试验中,66名接受Cretostimogene Grenadenorepvec治疗的膀胱癌患者中,有75.7%的患者肿瘤完全消失。 2.在另一项2期试验中,34名接受Cretostimogene Grenadenorepvec联合PD-1抑制剂Pembrolizumab治疗的膀胱癌患者中,有85%的患者肿瘤完全消失。 3.该疗法的安全性也良好可控,患者接受治疗后仅出现了… Read More... "美国溶瘤病毒疗法:膀胱癌患者肿瘤完全消失率达75.7%"
摘要 加拿大生物技术公司BriaCell的新型细胞免疫疗法Bria-IMT™在晚期脑转移乳腺癌患者中引发了令人振奋的疗效,使得71%的患者肿瘤大幅缩小或消失。 来源:BriaCell公司官网截图 关键信息如下: 1.7名乳腺癌脑转移患者中,5名患者颅内肿瘤显著缩小。 2.在先前经过多种治疗失败的转移性乳腺癌患者中,Bria-IMT™也带来了显著的临床益处。 3.在所有乳腺癌亚型患者中,接受Bria-IMT™治疗均观察到了肿瘤消退,凸显了Bria-IMT™在脑转移患者中的治疗潜力。 研究详情 (专业人士阅读) 近日,加拿大生物技术公司BriaCell的新型细胞免疫疗法Bria-IMT™在晚期脑转移乳腺癌患者中引发了令人振奋的疗效:在脑转移患者,具体为中枢神经系统(CNS)转移患者中,Bria-… Read More... "71%的患者肿瘤大幅缩小或消失,新型细胞免疫疗法治疗乳腺癌脑转移疗效振奋!"
摘要 美国食品药品监督管理局(FDA)授予美国生物技术公司Diakonos研发的癌症疫苗DOC1021用于恶性胶质瘤的孤儿药认定,包括新诊断和难治性胶质母细胞瘤,给脑癌患者带来了新的曙光。 孤儿药认定(ODD):孤儿药一般指用于治疗罕见病的药物,一旦获得孤儿药认定,将获得一系列激励措施,以加速该药物的临床试验和获批上市。 来源:摄图网 关键信息如下: 1.胶质母细胞瘤是一种恶性程度极高、致命性极强的脑癌,患者的平均生存期仅15-21个月,急需有效的新疗法。 2.在1期临床试验中,16名接受DOC1021疫苗治疗的患者,治疗两年多后,13名至今仍存活,并且大多数患者疾病没有进展。 3.患者接受DOC1021疫苗治疗的安全性也普遍良好,试验中未观察到严重不良事件。 研究详情 (专业人… Read More... "美国前沿癌症疫苗DOC1021,向攻克脑癌迈出关键一步!"
摘要 近日,美国纪念斯隆凯特琳癌症中心一项1期研究数据显示,美国SELLAS公司研发的癌症疫苗Galinpepimut-S联合纳武利尤单抗,将恶性胸膜间皮瘤患者生存期延长了3倍。 来源:摄图网 关键信息如下: 1.接受Galinpepimut-S疫苗治疗的患者平均总生存期为17.6个月,而接受标准治疗的患者生存期只有7个月左右。 2.Galinpepimut-S疫苗治疗有效的患者中,平均总生存期更是高达27.8个月,相比标准治疗,生存期延长了3倍! 3.该疫苗安全性良好,联合纳武利尤单抗,几乎无新增副作用。 研究详情 (专业人士阅读) GPS是一种靶向WT1蛋白的疫苗,由纪念斯隆凯特琳癌症中心开发出来。WT1蛋白存在于多种肿瘤类型中,包括恶性胸膜间皮瘤。 该试验纳入了10名可评估疗效的患者,… Read More... "美国新研究:癌症疫苗联合疗法将恶性间皮瘤患者生存期延长3倍!"
摘要 3b期临床研究数据显示,晚期小细胞肺癌(ES-SCLC)患者使用新型的免疫联合化疗方案,可明显提升肿瘤大幅缩小的概率,延长患者生存期。 来源:摄图网 关键信息如下: 1.研究显示,晚期小细胞肺癌患者使用新型免疫联合EP化疗方案的安全性和有效性数据良好。 2.研究人员发现,患者接受EP化疗的周期越多,疗效越显著,肿瘤大幅缩小的概率和总生存期提升更明显。 研究详情 (专业人士阅读) 3b期LUMINANCE研究(NCT04774380)的数据显示,对晚期小细胞肺癌(ES-SCLC)患者使用5个或更多个周期的顺铂/依托泊苷(EP方案)治疗,同时加入PD-L1免疫检查点抑制剂德瓦鲁单抗(Imfinzi),对患者的安全性和有效性数据良好,与之前的3期CASPIAN研究所报道的数据结果基本一致。 … Read More... "超给力!晚期小细胞肺癌前沿疗法,显著提升患者生存期!"
摘要 美国食品药品监督管理局(FDA)授予美国强生制药公司的新型靶向药物输送系统TAR-200突破性疗法认定,用于膀胱癌患者。该疗法在临床试验中展现强劲疗效,使得约80%的患者肿瘤完全消失! 来源:摄图网 突破性疗法认定(BTD):指美国食品药品监督管理局(FDA)对新药或新疗法的一种特殊授予,获得BTD的药物通常用于治疗严重或危及生命的疾病,并在早期临床试验中显示出相对于现有疗法更加显著的疗效。该认定旨在加速药物的研发和审批过程,以便更快地使患者受益。 关键信息如下: 1.TAR-200是一种新型靶向药物输送系统,可以将化疗药吉西他滨持续、可控地释放到膀胱中,并且可以在长达数周的时间内保持药物在膀胱内的浓度,持续产生疗效。 2.试验中,TAR-200单一疗法达到了非常惊艳的疗效,使得约80… Read More... "美国新疗法TAR-200获突破性疗法认定,膀胱癌患者肿瘤完全消失率达80%"
摘要 近日,一项新研究发现,一种新药成功地通过阻止胰腺癌细胞获取能量降低了临床前实验中小鼠体内胰腺癌的生长,而且很安全。 来源:摄图网 关键信息如下: 1.新型药物DRP-104在临床前研究中,对小鼠的胰腺癌细胞起到了抑制能量获取的作用,有望“饿死”癌细胞,阻止癌症进展。 2.该研究是一种治疗癌症的全新策略,有望对耐药性肿瘤细胞起到治疗效果。 3.研究团队发现,将新药和现有的靶向药曲美替尼联用时,可进一步提高对胰腺癌的疗效。 研究详情 (专业人士阅读) 近日,一项新研究发现,一种新药成功阻止了胰腺癌细胞获取能量,并压制了临床前实验中小鼠体内胰腺癌的生长,而且安全性良好。 这项研究建立在纽约大学朗格尼医学中心之前的研究成果基础之上,由纽约大学格罗斯曼医学院放射肿瘤学系以及佩尔穆特癌症中心的研究… Read More... "新型药物DRP-104有望阻断胰腺癌能量获取途径,“饿死”癌细胞!"
摘要 近日,新的临床研究显示,使用英国新型PD-1免疫药物Dostarlimab的新组合疗法,可显著改善晚期、复发性子宫内膜癌患者的疗效,大幅延长肿瘤控制时长。 来源:摄图网 关键信息如下: 1.新的研究显示,前沿免疫药物Dostarlimab的新组合疗法对于子宫内膜癌患者疗效显著,可大幅延长患者的肿瘤控制时长。 2.尤其是经检测,对免疫治疗较为敏感的患者,使用该药后疗效更佳,还有可能实现无瘤状态! 研究详情 (专业人士阅读) 近日,对3期RUBY/ENGOT-EN6/GOG3031/NSGO 试验的第2部分进行的分析显示,使用英国新型PD-1免疫检查点抑制剂Dostarlimab-gxly(Jemperli)联合标准化疗治疗后,再以Dostarlimab联合PARP抑制剂尼拉帕尼作为维持治… Read More... "Dostarlimab多斯塔利单抗联合疗法显著延长晚期子宫内膜癌患者无进展生存期"
摘要 近日,来自荷兰的研究人员成功地让一种毫米机器人在狭窄的血管内实现导航行进。未来,这类机器人将有望用于清除人体血栓以及携带药物实现目标区域精准治疗。 来源:特温特大学 关键信息如下: 1.宛如“毛毛虫”一样的前沿毫米级机器人,目前已能够在无线操作下进入人体狭窄的血管中自由行进。该技术有望帮助清除人体血栓,推动血管疾病的治疗。 2.毫米级机器人还有望用于携带药物前往某些需要高剂量治疗的区域,降低患者全身用药剂量,实现局部精准给药,降低治疗毒副作用。 研究详情 (专业人士阅读) 近日,来自荷兰特温特大学和拉德堡德大学医学中心的研究人员,成功地让无线毫米机器人在狭窄的血管内实现导航行进,包括顺向和逆向动脉血流两个方向。研究人员将一种类似“毛毛虫”的螺旋形状机器人置于一个带有肾脏的离体主动脉中,… Read More... "荷兰研究人员开发出“毛毛虫”毫米级机器人,用于血栓治疗!"
摘要 美国食品药品监督管理局(FDA)已批准美国生物技术公司Vittoria Biotherapeutics的CAR-T新疗法VIPER-101治疗T细胞淋巴瘤的新药临床试验申请,该疗法的头个人体临床试验计划于2024年上半年启动。 注:新药临床试验申请(IND)是美国食品药品监督管理局(FDA)用于监管新药开发的一种许可和监管制度。具体而言,IND是一种申请,由制药公司或研究机构向FDA提交,以获得许可开始在人类中进行新药临床试验。 来源:摄图网 关键信息如下: 1.VIPER-101是一种结合基因编辑技术的CAR-T疗法,抗肿瘤疗效更强。 2.传统的CAR-T疗法可能会导致CAR-T细胞在攻击肿瘤细胞时与患者体内的T细胞“自相残杀”,VIPER-101能很好地规避这一问题。 3.CA… Read More... "美国CAR-T新疗法VIPER-101获批开展临床试验,治疗T细胞淋巴瘤"
摘要 近日,美国西北大学医院发表在知名科学杂志——《自然医学》上的一项研究显示,一款新型人工智能(AI)工具可能帮助医生更精确地预测乳腺癌患者预后,从而避免患者进行本无必要的治疗。 来源:摄图网 关键信息如下: 1.病理学家用肉眼对癌细胞形态进行评估,之后对乳腺癌分级、指导治疗方案的旧模式,有望被美国一款新型AI工具颠覆。 2.美国科研人员开发的新型AI模型,可以对癌细胞和非癌细胞进行更好地评估,为病理学家提供更详实、精准的肿瘤信息,这有助于帮助患者避免某些本无必要的治疗,以及更好地为患者快速调整方案。 研究详情 (专业人士阅读) 近日,美国西北大学医院发表在知名科学杂志——《自然医学》上的一项研究显示,一款新型人工智能(AI)工具可能帮助医生更精确地预测乳腺癌患者预后,从而避免一部分患者进… Read More... "美国乳腺癌新型AI工具:超越肉眼极限,有望颠覆传统病理评估!"
摘要 美国食品药品监督管理局(FDA)授予美国生命科学公司Solid Biosciences的基因疗法SGT-003快速通道认定,用于治疗杜氏肌营养不良症(DMD)。 快速通道认定(FTD):快速通道认定是美国食品药品监督管理局(FDA)提供的一种制度,旨在促进新药的开发和审批,尤其是针对治疗严重或威胁生命的药物。该认定旨在加速这些药物的研发、审批和上市,以更迅速地满足患者的医疗需求。 来源:摄图网 关键信息如下: 1.杜氏肌营养不良症是一种会导致患儿肌肉萎缩的遗传性疾病,不可逆转并且会危及患儿的生命,急需有效的治疗方法。 2.SGT-003是一种基因疗法,采用了特殊的设计,临床前研究数据表明,该疗法能够改善小鼠的肌肉功能,并且具有持久的治疗效果。 3.SGT-003即将开展的1… Read More... "杜氏肌营养不良症患者新希望!美国新疗法SGT-003值得期待"