本文深度解析2025年ESMO会议上晚期非小细胞肺癌少见靶点突变(如EGFR Ex20ins、ALK、HER2、BRAF V600E)的最新靶向治疗进展。齐帕勒替尼、伏美替尼、阿来替尼等新药在临床研究中展现显著疗效,包括颅内转移患者的获益及中位OS、PFS数据的提升。这些突破为患者带来新的生存希望,MedFind持续关注前沿资讯,助您寻找最佳治疗方案。 Read More... "2025 ESMO肺癌靶向治疗最新进展:EGFR/ALK/HER2/BRAF少见突变药物深度解析"
肺腺癌患者在酪氨酸激酶抑制剂(TKI)治疗后面临耐药挑战,其中腺-鳞转化是重要原因。最新研究揭示,KMT2D基因缺失驱动了这一转化过程并导致TKI耐药。研究发现AURKA可作为针对KMT2D缺陷肿瘤的特异性靶点,为克服非小细胞肺癌TKI耐药提供了新的精准治疗策略和希望,提升患者治疗成功率。 Read More... "非小细胞肺癌TKI耐药难题破解:KMT2D缺失引发腺-鳞转化,AURKA抑制或成新希望"
复旦大学团队在三阴性乳腺癌免疫耐药研究取得重大进展,首次揭示感觉神经元是免疫治疗耐药“元凶”,并发现治疗偏头痛的药物利美吉泮有望逆转耐药,为三阴性乳腺癌患者带来新的治疗希望。MedFind为您解析这一“中国方案”的突破性意义。 Read More... "三阴性乳腺癌免疫耐药终结者?中国方案揭示偏头痛药新潜力"
最新研究揭示,SLC6A6将牛磺酸转运至线粒体,这一过程对肿瘤生长至关重要。深入了解这一机制,为癌症治疗提供了全新的靶点思路,有望带来突破性进展。 Read More... "癌症治疗新突破?SLC6A6与牛磺酸如何影响肿瘤生长及潜在靶点解析"
《柳叶刀》子刊最新研究揭示,遵循“低超加工食品、高植物性饮食、高食物多样性”的3V饮食原则,可将肠癌风险直降近30%。本文深度解读3V饮食原理与实践方法,帮助您轻松掌握日常饮食防癌秘诀,为肠道健康筑牢防线。 Read More... "“柳叶刀”重磅:遵循“3V饮食”,肠癌风险直降近30%!您的防癌秘籍"
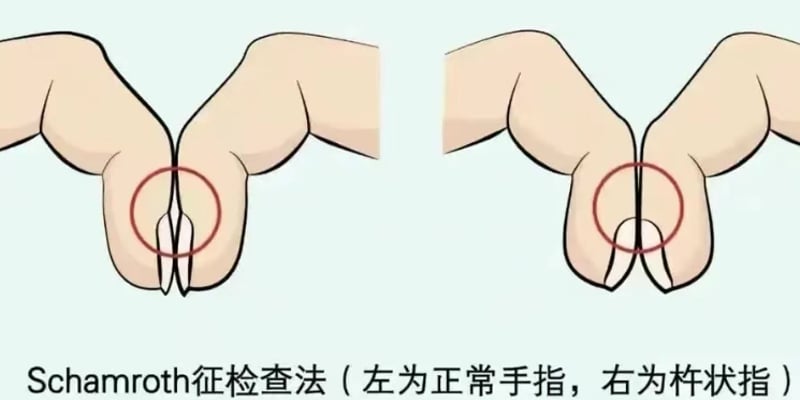
肺癌早期信号常被忽视,但您的指甲可能藏着救命线索。本文深度解析“手指杵状膨大”这一关键预警症状,教您30秒在家自测方法,并详细解读其与肺癌的关系,帮助您及时发现异常,守护肺部健康。 Read More... "肺癌早期预警:指甲异常或是救命信号?专家详解手指杵状膨大与自测方法"
《Cell》杂志最新研究揭示癌症恶病质患者体重暴瘦的深层原因:肝脏并非旁观者,而是病程的“放大器”。文章详细解读肝脏在恶病质中的独特作用机制,特别是REV-ERBα蛋白的关键调控,为未来逆转患者消耗性症状、改善预后提供了全新治疗思路。了解这一突破性发现,为抗癌之路增添新希望。 Read More... "癌症患者暴瘦元凶新发现:肝脏竟是恶病质“放大器”?《Cell》重磅研究揭示深层机制与治疗前景"
最新研究显示,尽管多数癌症死亡率下降,但年轻人结直肠癌死亡率却逆势上升,已成该群体癌症死因首位。本文深入解读美国癌症协会研究,探讨早发性结直肠癌高发原因、风险因素,并提供关键筛查与预防建议,帮助患者与家属了解如何积极应对,提升生存希望。 Read More... "年轻人结直肠癌死亡率为何逆势增长?权威解读与自救指南"
免疫治疗为肿瘤患者带来治愈希望,但免疫相关不良反应(irAEs)不容忽视。本文深度解析irAEs的识别、分级、激素用药、心肌炎等凶险irAEs的早期预警与预测指标,帮助患者和家属了解免疫治疗的风险管理,在获得疗效的同时确保安全。了解更多抗癌知识与药物信息,请访问MedFind。 Read More... "免疫治疗不良反应(irAEs)如何安全应对?深度解析用药管理与预警"
肺腺癌患者检出EGFR p.S645C罕见突变?本文深入解读这种“万里挑一”的基因变异,分析阿法替尼在罕见突变中的治疗潜力,并结合真实案例,为您提供精准的靶向治疗策略、副作用管理及海外购药渠道,点燃生命新希望。 Read More... "肺腺癌EGFR p.S645C罕见突变:阿法替尼治疗案例揭秘与海外购药指南"
最新研究发现,对于急性淋巴细胞白血病(ALL)患者,采用骨髓清除性预处理的异基因造血干细胞移植可显著延长长期生存期。本文深入解读研究数据,分析影响生存的关键因素,为患者及家属提供全面、专业的治疗策略解读与指导。 Read More... "急性淋巴细胞白血病(ALL)患者福音:异基因移植显著改善长期生存期,最新研究揭示关键因素"
针对晚期黑色素瘤,Lifileucel(AmTagvi)肿瘤浸润淋巴细胞(TIL)疗法带来生存希望。本文深度解读其疗效数据、治疗流程中的挑战及克服之道,并为您揭示如何通过MedFind获取这一前沿抗癌药物。 Read More... "晚期黑色素瘤新希望:Lifileucel(AmTagvi)TIL疗法深度解析,疗效、挑战与全球获取策略"
软组织肉瘤治疗迎来革新。基因检测,特别是融合基因检测,正成为晚期肉瘤精准治疗的关键。本文深入探讨基因检测如何助力识别驱动基因,指导靶向药物选择,为软组织肉瘤患者带来新的治疗突破与希望,包括对抗传统疗法无效的困境。 Read More... "软组织肉瘤治疗新纪元:基因检测如何精准捕捉融合基因,开启靶向治疗新希望?"
在2026年移植与细胞治疗大会上,一项最新分析显示,新型细胞疗法Orca-T在骨髓增生异常综合征(MDS)等血液肿瘤的造血干细胞移植中,展现出远超传统标准治疗的生存率优势。这项创新技术有望显著改善患者预后,为急需有效治疗的MDS、AML、ALL患者带来新的希望和更优的选择。 Read More... "Orca-T细胞疗法:骨髓增生异常综合征(MDS)造血干细胞移植新希望,生存率大幅提升!"
胰腺癌患者常受腹腔神经丛相关剧痛折磨,传统止痛方式效果不佳。最新研究揭示,创新性高剂量单次放射治疗腹腔神经丛,能显著缓解癌痛,降低阿片类药物依赖,为晚期患者带来生活质量的重大改善,是未来癌痛管理的重要方向。 Read More... "胰腺癌痛难忍?“腹腔神经丛放疗”新突破,精准缓解剧痛,提升生命质量!"
西湖大学蔡尚团队在Cell发表重磅研究,首次揭示肿瘤内细菌在胞内与胞外状态下,如何截然相反地调控肿瘤免疫微环境。该发现深入解读乳腺癌“冷热”肿瘤形成机制,为克服免疫治疗耐药、预防癌症转移复发提供了全新策略与潜在靶点,有望改变未来癌症诊疗方向。 Read More... "西湖大学Cell重磅:肿瘤内细菌如何决定癌症“冷热”?揭示乳腺癌免疫逃逸新机制"
最新研究揭示超加工食品与癌症患者死亡风险可能升高,但研究设计引争议。本文深入解读研究结果,剖析超加工食品的潜在危害,并提供权威健康饮食建议,助您科学管理饮食,提升生存质量。 Read More... "警惕!超加工食品或影响癌症患者生存期?专家解读与饮食指南"
一项发表于《自然-癌症》的重磅研究揭示,免疫系统并非多发性骨髓瘤治疗的旁观者,而是疾病发生、发展及治疗效果的核心驱动力。深入理解骨髓微环境的紊乱,将为患者带来更精准的个性化免疫治疗新希望。MedFind为您解读这项前沿研究,并提供最新的抗癌资讯与支持。 Read More... "多发性骨髓瘤新突破:骨髓微环境与免疫系统如何决定治疗成败?"
一项最新II期临床试验发现,在接受造血干细胞移植的患者中,乌司奴单抗联合标准预防方案可显著降低清髓性预处理(MAC)患者的急性移植物抗宿主病(GVHD)发生率及非复发死亡率,为这类患者带来了新的治疗希望,且未影响抗肿瘤效果。 Read More... "造血干细胞移植患者福音:乌司奴单抗预防GVHD,清髓预处理效果显著"
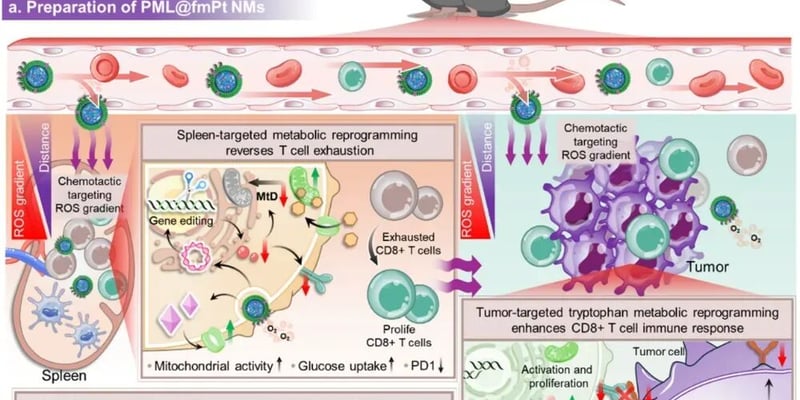
南京大学团队研发的创新纳米马达技术,通过相分离工程实现脾脏与肿瘤双靶向,协同递送二甲双胍与CRISPR/Cas9,旨在逆转CD8+T细胞耗竭,改善肿瘤微环境,为癌症免疫治疗带来新的曙光。这项临床前研究展现了重塑抗癌免疫的巨大潜力。 Read More... "南京大学科研突破:纳米马达靶向脾脏肿瘤,有望逆转T细胞耗竭重塑抗癌免疫力"