儿童肾癌治疗的挑战与新希望
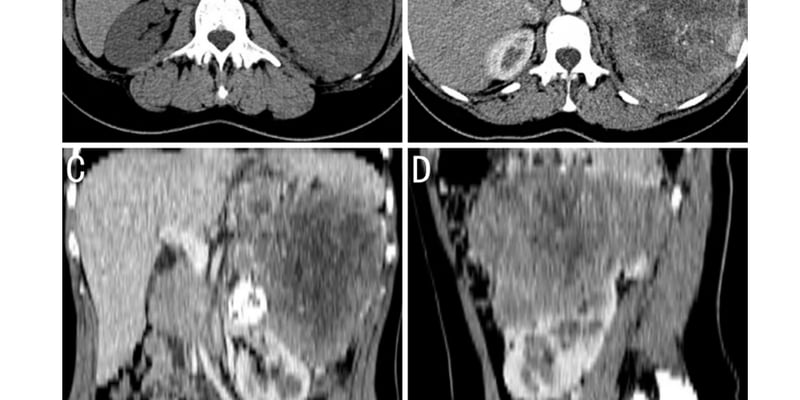
易位性肾细胞癌(tRCC)是一种罕见但极具侵袭性的儿童肾脏肿瘤,约占所有儿童肾癌的30%。其治疗长期以来都是一个棘手的难题。然而,近期发表于国际顶尖期刊《Nature Communications》的一项研究为tRCC患儿带来了新的希望。科学家们不仅揭示了其独特的致癌机制,还开发出一种创新的“分子开关”,能够精准摧毁癌细胞的“作战指挥中心”。
揭秘癌细胞的“液态指挥中心”
tRCC的罪魁祸首是一种名为“TFE3融合蛋白”的异常分子。当细胞内染色体发生错误重组时,TFE3基因会与其他基因意外“联姻”,形成这种驱动癌症的融合蛋白。但它究竟是如何发号施令,驱动肿瘤疯狂生长的呢?
传统观念认为,RNA分子主要负责传递遗传信息。但这项新研究发现,在tRCC细胞中,RNA扮演了截然不同的角色——它被TFE3融合蛋白“策反”,成为了构建肿瘤“指挥中心”的关键材料。研究团队发现,TFE3融合蛋白能够招募大量的RNA分子,在细胞核内形成一个个液滴状的“转录凝聚体”。这些凝聚体如同癌细胞的特种作战指挥部,高效地将RNA聚合酶II、PSPC1等关键蛋白聚集起来,从而大规模启动下游促癌基因的表达,为肿瘤的生长提供源源不断的动力。
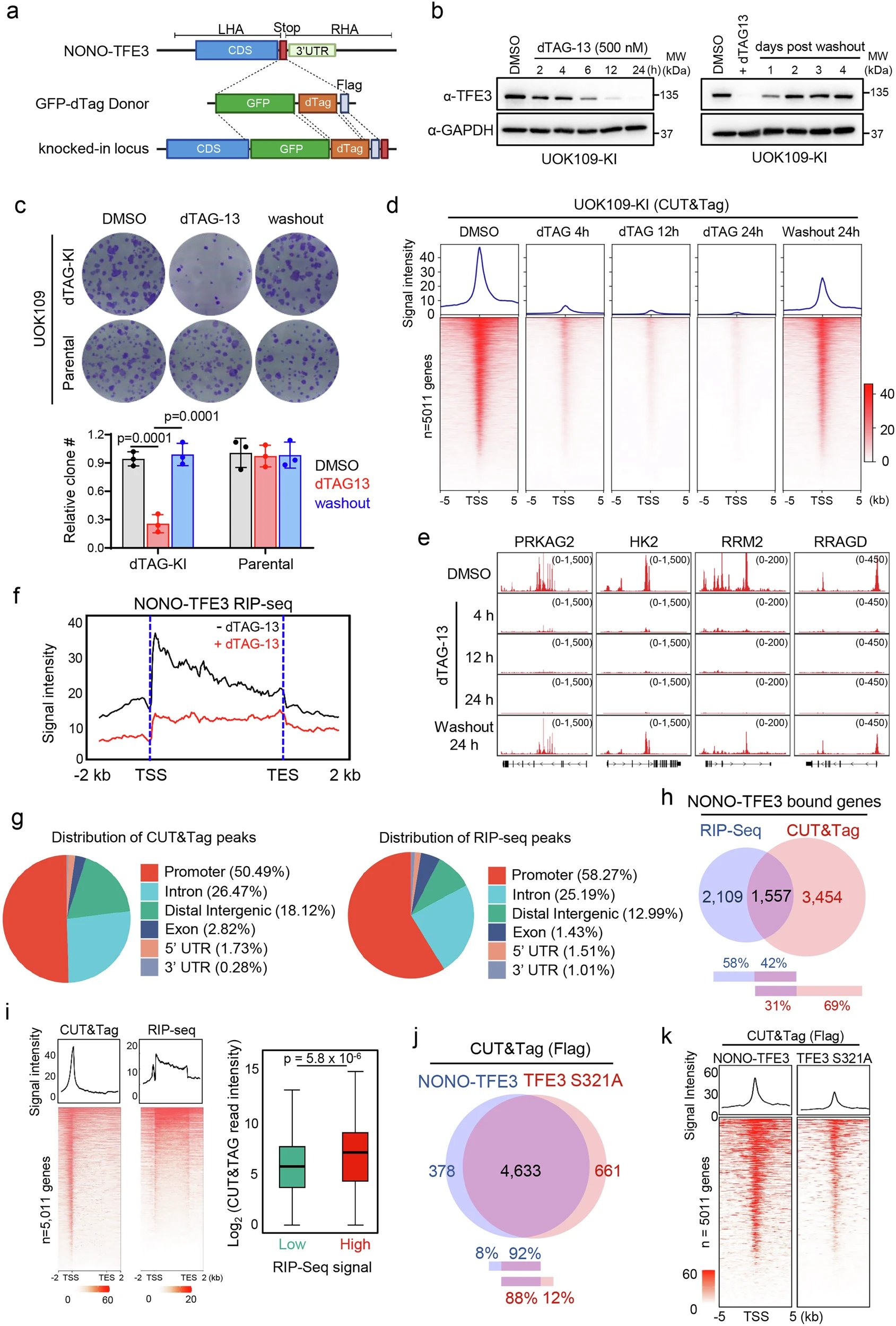
研究人员进一步发现,RNA结合蛋白PSPC1在其中扮演了“加固工程师”的角色,它的参与使得这些“指挥中心”结构更加稳定,成为驱动肿瘤生长的强力引擎。对于这种复杂的罕见癌症,获取专业的第二诊疗意见至关重要。MedFind的AI问诊服务可以帮助您快速了解前沿治疗方案。
“分子拆弹装置”:精准瓦解肿瘤核心
发现机制只是第一步,更关键的是如何摧毁这些“指挥中心”。为此,研究团队设计了一种基于纳米抗体的化学遗传学工具,可以将其比作一个可远程遥控的“分子拆弹装置”。
它的工作原理十分精妙:首先,微小的纳米抗体能够精准识别并锁定癌细胞内的TFE3融合蛋白;然后,当研究人员加入特定的化学诱导剂时,与纳米抗体相连的分解蛋白就会被激活,迅速“融化”整个液滴结构,使“指挥中心”瞬间土崩瓦解。
实验结果令人鼓舞。无论是在体外培养的癌细胞中,还是在tRCC小鼠模型体内,这种策略都成功地瓦解了转录凝聚体,并有效抑制了肿瘤的生长。
靶向相分离:抗癌治疗的新范式
这项研究的重大意义在于,它不仅解释了易位性肾细胞癌为何如此凶险,更重要的是找到了其“阿喀琉斯之踵”。通过瓦解癌细胞的“液态指挥中心”,就如同切断了整个肿瘤工厂的电源,从根本上遏制了其生长。
这种“靶向相分离”的抗癌新范式,为未来药物研发开辟了新道路。由于许多儿童癌症都是由类似的融合蛋白驱动的,该策略有望成为一种普适性的抗癌新途径。与传统化疗药物相比,这种疗法能更精准地打击癌细胞,有望大幅降低毒副作用。您可以访问MedFind抗癌资讯板块,获取更多前沿疗法信息。对于那些正与罕见儿童癌症抗争的家庭而言,这项突破性的研究无疑点亮了一盏充满希望的明灯。