肝癌转移的“幕后黑手”:肿瘤相关巨噬细胞
肝细胞癌(HCC),即我们常说的肝癌,其高转移率是导致患者预后不佳的主要原因之一。癌细胞为何能如此“狡猾”地扩散和转移?长期以来,科学家们一直在探索其背后的复杂机制。近日,一项发表在国际顶级期刊《Nature Metabolism》上的研究为我们揭示了答案的一角。
这项由中科院上海营养与健康研究所、复旦大学附属华山医院等机构合作完成的研究发现,在肿瘤微环境中,一类被称为肿瘤相关巨噬细胞(TAMs)的免疫细胞,扮演了促进肝癌转移的“帮凶”角色。

癌细胞的“特供燃料”:乙酸
研究团队通过精密的实验发现,这些肿瘤相关巨噬细胞(TAMs)就像一个“乙酸储库”,会持续不断地生产并分泌一种名为乙酸(acetate)的小分子物质。
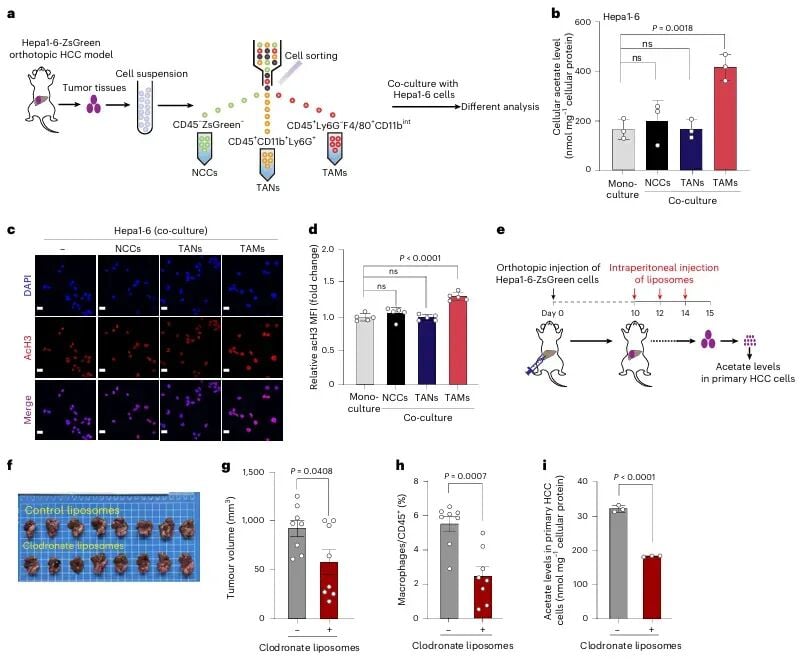
肝癌细胞一旦捕获到这些由TAMs提供的乙酸,就会将其作为“特供燃料”。在ACSS2酶的作用下,乙酸被转化为乙酰辅酶A(acetyl-CoA),这不仅为癌细胞提供了能量,更关键的是,它能通过调控基因表达,启动“上皮-间质转化(EMT)”程序,极大地增强了癌细胞的迁移和侵袭能力,最终导致肝癌的远处转移。
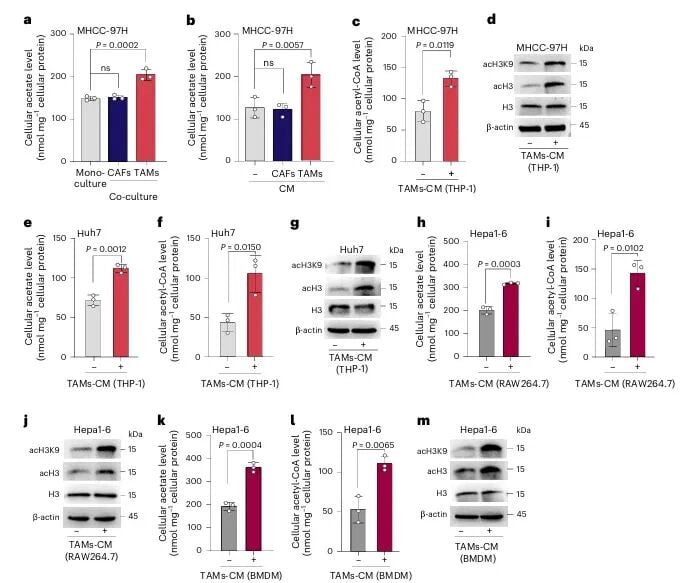
“燃料工厂”的关键开关:ALDH2通路
那么,TAMs是如何生产出这些乙酸的呢?研究进一步揭示,其核心在于一个名为“脂质过氧化-ALDH2”的代谢通路。
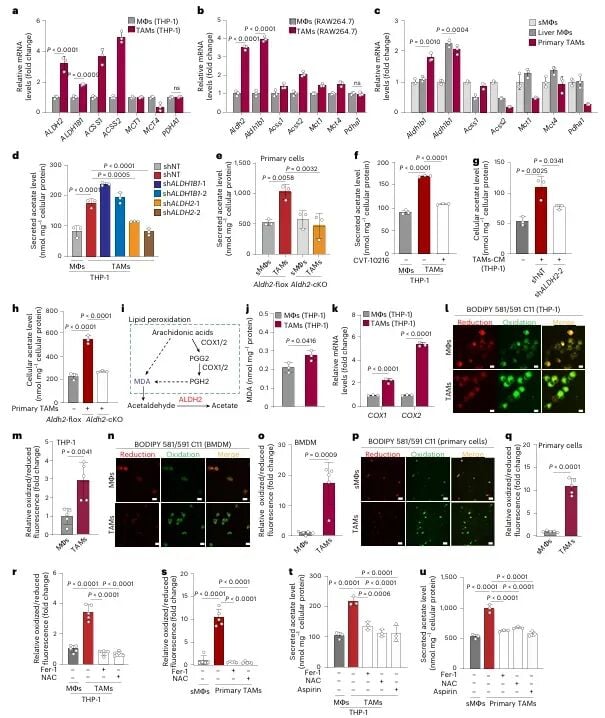
在肿瘤微环境中,TAMs内部的脂质过氧化水平升高,其产物可被ALDH2酶转化为乙酸。当研究人员通过技术手段抑制ALDH2的活性或抑制脂质过氧化过程时,TAMs分泌乙酸的能力显著下降,从而有效阻断了对肝癌细胞迁移的促进作用。这一发现为开发新的肝癌治疗策略提供了重要思路。如果您正在寻求前沿的抗癌资讯或治疗方案,MedFind可以为您提供帮助。
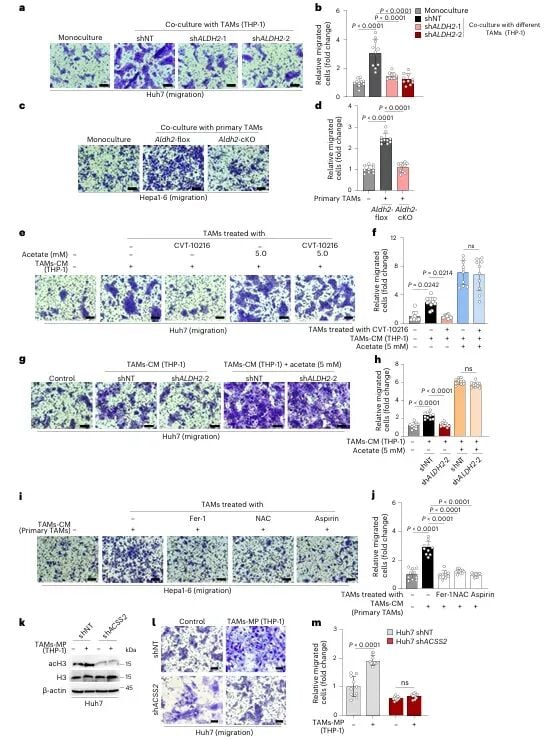
一个危险的“互利”循环
更令人惊讶的是,研究还发现肝癌细胞与TAMs之间存在一种“互利共生”的恶性循环。肝癌细胞自身会分泌大量乳酸,而这些乳酸又能反过来刺激TAMs,激活其“脂质过氧化-ALDH2”通路,使其生产更多的乙酸。
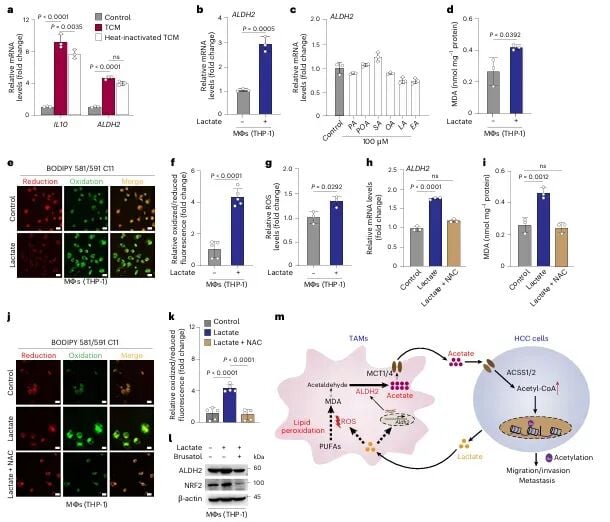
这样一来,肝癌细胞通过“喂养”TAMs,让其为自己提供更多“燃料”,形成了一个自我强化的正向反馈环路,不断推动着肿瘤的恶性进展和转移。理解这种复杂的机制对于制定有效的治疗方案至关重要。如果您对自己的病情和治疗方案有疑问,可以尝试使用MedFind的AI问诊服务,获取专业的第二诊疗意见。
研究意义:为肝癌治疗带来新曙光
总而言之,这项重磅研究系统地揭示了肿瘤微环境中癌细胞与免疫细胞之间全新的代谢交互模式,阐明了TAMs作为乙酸供应者在驱动肝癌转移中的关键作用。
这一发现不仅深化了我们对肝癌转移机制的理解,更重要的是,它为肝癌治疗提供了潜在的新靶点。未来,针对TAMs中的ALDH2等关键分子开发的靶向药物,有望通过切断癌细胞的“燃料供应”,从而有效抑制肝癌转移,为广大患者带来新的希望。虽然针对这一新机制的靶向药物尚在研发中,但目前已有多种获批的肝癌靶向药。患者可以通过MedFind海外靶向药代购平台获取更多药物信息和购买渠道。





