在癌症诊疗的复杂世界中,肺部多发性肿瘤结节(MPTN)的诊断与鉴别一直是临床医生面临的重大挑战。随着低剂量CT筛查的普及和高分辨率影像技术的进步,越来越多的患者被发现肺部存在多个病灶。然而,这些病灶究竟是独立的原发性肺腺癌(SPLCs),还是由单一原发灶扩散而来的肺内转移瘤(IPMs),其区分对于患者的精准分期、治疗方案制定及预后评估至关重要。
国际肺癌研究协会病理委员会(IASLC)发布的《肺腺癌原发灶与肺内转移灶的病理及分子鉴别:IASLC的共识建议》为这一难题提供了权威指导。本文将深入解读这份共识,旨在帮助患者及家属更好地理解多发性肺肿瘤的诊断逻辑,并为寻求海外靶向药代购等服务的用户提供有价值的抗癌资讯。
多发性肺肿瘤结节的挑战与分类
多发性肺肿瘤结节(MPTN)的出现率日益增高,其发病率受多种因素影响。在这些复杂病例中,准确区分独立原发性肺癌(SPLCs)与肺内转移瘤(IPMs)是制定有效治疗策略的关键。此外,MPTN还需与肺外转移病灶及良性病变进行鉴别。
IASLC的共识建议将MPTN细分为四类,以更精准地反映其预后特征:
- 独立原发性肺癌(SPLCs): 包括异时性(间隔≥2年)和同时性(间隔≤2年)病灶,彼此独立发生。若组织学亚型不同(如腺癌与鳞癌),诊断相对明确;若相同,则需全面病理评估。同时性SPLCs的预后通常取决于分期最高的肿瘤。
- 肺内转移瘤(IPMs): 影像学常表现为实性结节。根据病灶位置,可分期为T3(同侧肺叶内)、T4(同侧不同肺叶)或M1a(双侧肺叶)。IPMs的鉴别高度依赖组织学与分子检测。
- 多灶性磨玻璃腺癌: 属于SPLCs的亚型,CT显示至少两个纯磨玻璃或部分实性结节。常见于女性非吸烟者,预后相对较好,淋巴结转移率低。分期依据T分期最高的病灶。
- 肺炎型腺癌(侵袭性黏液腺癌,IMA): 占肺腺癌的3%~10%,CT表现类似肺炎。IMA多提示肺内转移性病变,而非SPLCs,常伴有KRAS突变或NRG1融合,缺乏EGFR突变。预后通常较差,易广泛播散。
精准的分类和分期对于后续的治疗方案选择具有决定性意义。例如,IPMs可能导致更晚期的分期(T3、T4或M1a),需要差异化的治疗策略。
影像学与病理学:传统诊断基石
在多发性肺肿瘤结节的诊断中,影像学和病理学是不可或缺的初步评估工具。
影像学诊断
影像学特征能提供初步线索。例如,在存在单一较大原发性肺癌的情况下,若外周肺野及下叶出现多发小圆形实性结节,高度提示为IPMs。然而,多发性双侧同时性肺腺癌并不少见,特别是当影像表现为多发性双侧磨玻璃结节或大小相近的亚实性结节时,可能提示独立原发灶。值得注意的是,即使是体积小、生长缓慢的磨玻璃结节,也可能预示肺腺癌,需长期随访。
病理学诊断
共识建议强调,在手术切除的肺腺癌中,组织病理学特征是区分SPLCs与IPMs最常用的标准。通过全面组织学评估,结合肿瘤亚型和细胞学特征,可初步判断病灶的性质。例如,影像学表现为多发磨玻璃样结节且组织学对应非黏液性原位腺癌、微浸润性腺癌或贴壁为主型肺腺癌,通常被视为独立原发灶。
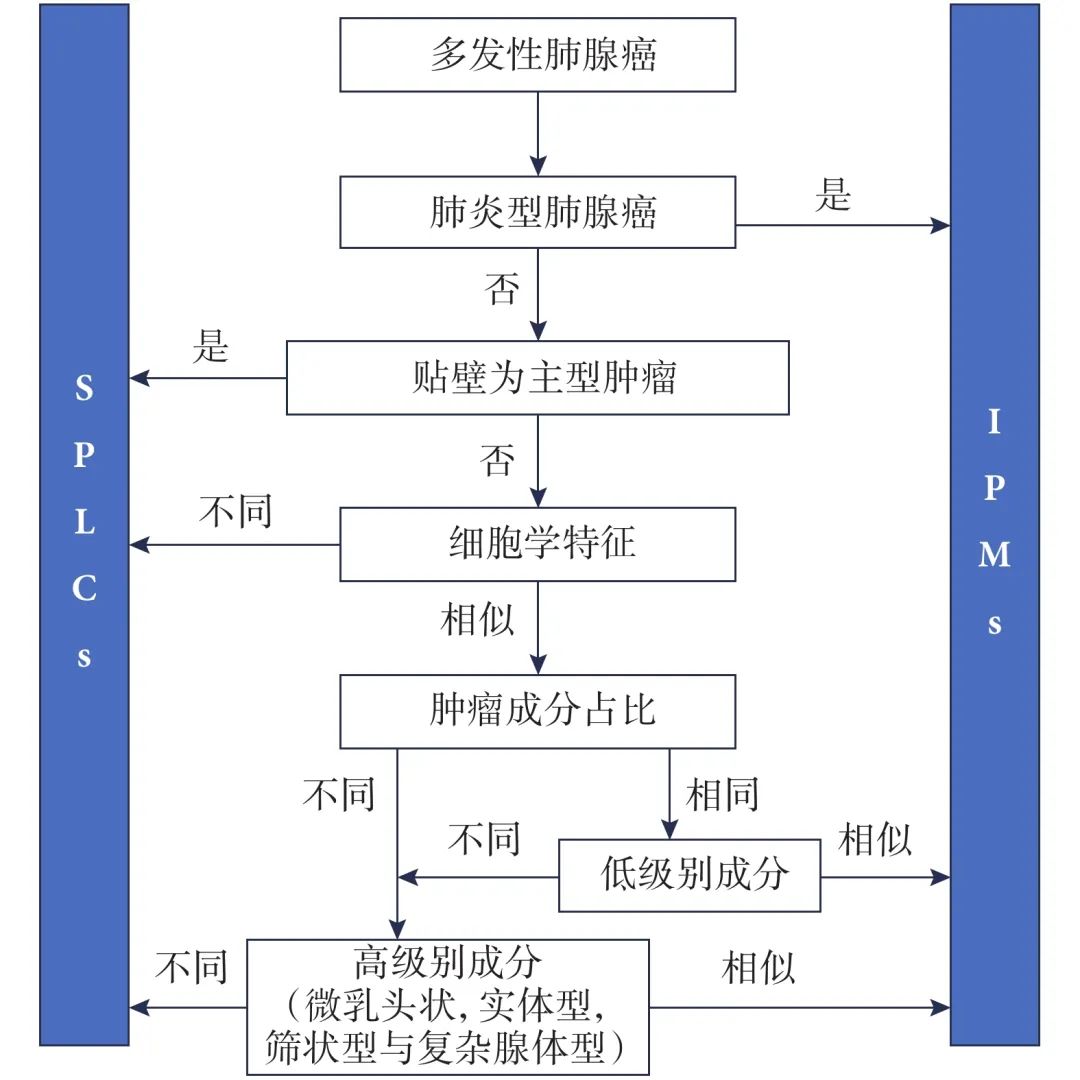
图1 用于确定MPTN病灶间克隆性关系的组织学评估方法
然而,组织学评估存在局限性,如肿瘤内异质性、去分化及治疗引起的形态改变,可能导致诊断不一致。因此,分子分析,特别是高通量测序技术(NGS),被认为是鉴别SPLCs与IPMs的更可靠标准。
分子诊断:NGS技术革新鉴别方法
在传统病理学诊断面临挑战时,分子学诊断技术为肺腺癌的精准鉴别提供了强大支持。从早期的DNA微卫星分析到如今的二代测序(NGS),分子技术在揭示肿瘤克隆性关系方面发挥着越来越重要的作用。
基因突变分析
共识建议指出,当多处肺肿瘤中仅单肿瘤出现基因突变或存在不同突变时,明确支持SPLCs的诊断。反之,若多处肺肿瘤存在相同的基因突变,则高度提示IPMs。例如,EGFR、KRAS、BRAF、CDKN2A及TP53等驱动基因突变在原发灶与转移灶间常表现出高度一致性。然而,需结合突变在人群中的流行率进行综合考量,以避免“区域癌化效应”带来的混淆。
靶向NGS技术能够扩大基因组合分析范围,显著提升克隆关系判定的准确性,从而为临床决策提供更坚实的依据。如果您对基因检测结果有疑问,或需要进一步了解药物信息,MedFind提供专业的AI问诊服务,助您解答疑惑。
四步分类评估法:整合诊断新标准
为了克服单一诊断方法的局限性,IASLC共识建议提出了一种结合组织学与分子学特征的“四步分类评估诊断方法”,旨在实现对SPLCs与IPMs的精准鉴别:
- 第一步:特定组织学类型评估。 对于原位腺癌、微浸润腺癌、贴壁型为主的腺癌或黏液腺癌等特定组织学类型,单纯组织学评估即可初步明确诊断。但对于多发性肺黏液腺癌,若病灶间存在显著异质性,仍需分子检测辅助。
- 第二步:同行评议的组织学评估。 若初步组织学分类无法明确诊断,建议通过多位病理学家进行同行评议,以达成更全面的组织学共识。
- 第三步:驱动基因突变检测。 若同行评议仍无法达成一致,则需开展KRAS、EGFR、ALK等驱动基因突变检测。若检测到不同驱动基因突变,可诊断为SPLCs。
- 第四步:高通量分子检测。 对于简单分子分析显示相同驱动基因突变或未检出突变的病例,需采用大规模NGS测序组合、全外显子组测序或全基因组测序等高通量分子检测技术进行深入分析。若肿瘤存在一个或多个除驱动基因突变以外的共有体细胞突变,则诊断为IPMs。但若TP53突变状态不同,则更倾向于诊断为SPLCs。
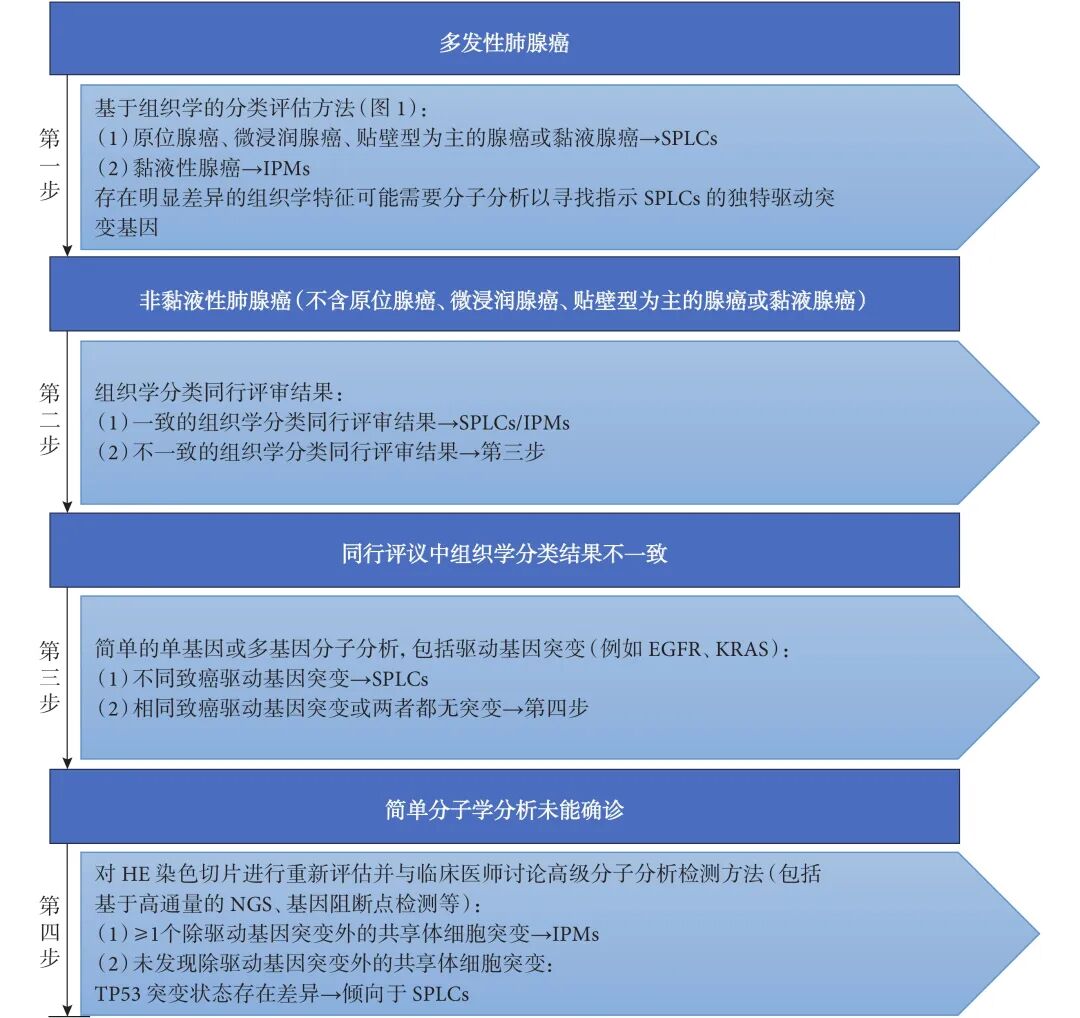
图2 结合组织学和分子学特征的四步分类评估诊断方法
这一整合性诊断策略,尽管对医疗资源配置要求较高,但被视为区分SPLCs与IPMs的“标准诊疗流程”,为患者的后续治疗提供了坚实基础。
多发性肺癌的治疗策略与药物选择
在精准鉴别多发性肺腺癌的性质后,制定个体化的治疗方案至关重要。NCCN指南指出,手术是同时性或异时性SPLCs的标准治疗方式。对于无法手术的早期病灶,立体定向体部放疗可作为替代方案。
对于局部晚期患者,辅助治疗的选择日益丰富:
- 辅助化疗: 适用于Ⅱ~ⅢA期患者。
- 靶向治疗: 对于携带EGFR突变的ⅠB~ⅢA期患者,可考虑使用奥希替尼等靶向药物。
- 免疫治疗: Ⅱ~ⅢA期且PD-L1肿瘤比例评分≥1%的患者,辅助化疗后可联合阿替利珠单抗等免疫治疗。晚期患者中,铂类化疗联合帕博利珠单抗等免疫治疗在PD-L1高表达人群中显示出协同效应。
值得注意的是,同一患者不同肿瘤对特定治疗的生物学反应可能存在异质性,因此辅助治疗需个体化评估。对于复发的寡转移病灶,射频消融术联合褪黑素可改善局部控制。全身治疗(化疗、免疫治疗、靶向治疗)在SPLCs患者的治疗中占据重要地位,特别是对于携带EGFR或ALK等驱动基因突变的患者,靶向治疗可显著延长生存期。
MedFind致力于为癌症患者提供全球优质靶向药代购服务,包括多种海外靶向药。我们深知患者对高效、安全购药的需求,并提供全面的药物信息和诊疗指南,助您做出明智的治疗选择。
总结与展望
IASLC的共识建议为多发性肺腺癌的鉴别诊断提供了系统性框架,强调了组织学评估与高通量NGS分子分析相结合的整合性诊断策略。这种“四步分类评估诊断方法”有望成为未来的标准诊疗流程,尽管其对医疗资源配置提出了更高要求。
随着数字病理学与机器学习技术的不断发展,未来有望出现更高效、更精准的诊断工具,为SPLCs与IPMs的鉴别提供新途径,最终惠及广大肺癌患者。MedFind将持续关注前沿抗癌资讯,为患者提供最新的药物信息和诊疗进展。