时光荏苒,科学探索的脚步从未停歇。在刚刚过去的8月,国际顶级科学期刊《Nature》再次发布了一系列重磅研究成果,为人类对抗重大疾病带来了新的曙光。这些突破性发现不仅深入揭示了疾病的复杂机制,更指明了未来治疗策略的潜在方向。对于正在寻求创新疗法的癌症患者及其他疾病群体而言,这些前沿进展无疑是令人振奋的希望。
阿尔兹海默病:锂缺乏与疾病发生的新关联
阿尔兹海默病(AD)作为全球最常见的神经退行性疾病之一,其日益增长的发病率对全球健康构成严峻挑战。尽管科学家们投入了大量精力,但有效的治疗方法依然匮乏。近期,《Nature》杂志刊登的一项研究揭示了锂在大脑中的生理作用,并阐释了锂缺乏与阿尔兹海默病发病机制之间的潜在联系。
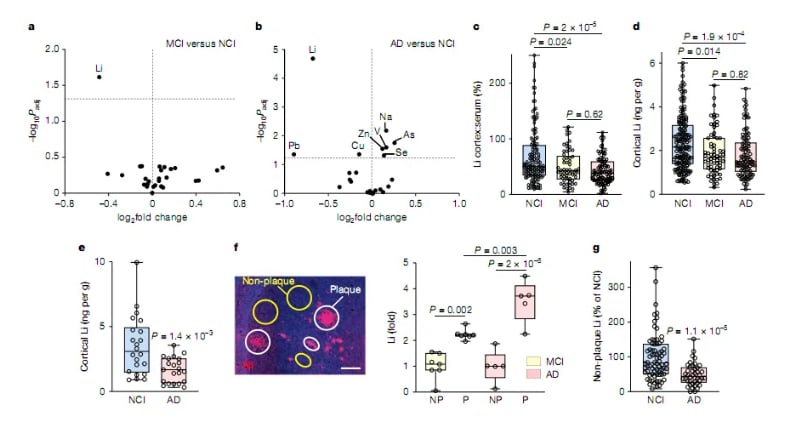
研究人员通过分析健康老年人及轻度认知障碍(MCI)和阿尔兹海默病患者的脑组织样本,发现MCI和AD患者前额叶皮层中的锂水平显著降低。这种锂缺乏与淀粉样斑块(Aβ)沉积和tau蛋白过度磷酸化密切相关,并会激活在Aβ和tau病理中发挥关键作用的GSK3β激酶。这一发现为阿尔兹海默病的早期诊断和干预提供了新的思路。
自身免疫性疾病:RNA修饰与免疫系统异常激活
自身免疫性疾病和慢性炎症性疾病正成为影响人类健康的重大挑战,例如系统性红斑狼疮(SLE)。这些疾病的发病机制往往与免疫系统对自身核酸的异常识别密切相关。一项发表在《Nature》上的研究深入探讨了RNA糖基化这一新兴修饰方式,如何通过调节免疫系统来影响细胞凋亡后的清除过程及自身免疫性疾病的发病机制。
研究揭示,RNA糖基化在免疫逃逸和细胞凋亡后清除过程中扮演着重要角色。去糖基化的小RNA能强烈激活巨噬细胞并诱导I型干扰素产生,而这种免疫激活作用依赖于Toll样受体3(TLR3)和Toll样受体7(TLR7)。此外,细胞表面的糖基化RNA在细胞凋亡后被巨噬细胞吞噬时,能阻止内质网RNA传感器的激活,从而促进非炎症性清除,这对于维持组织稳态至关重要。理解这些机制,有助于开发针对自身免疫性疾病的创新疗法。
癌症疗法新突破:NSD2抑制剂有望治疗肺癌和胰腺癌
肺癌和胰腺癌以其高发病率和高死亡率,对人类健康构成严重威胁。寻找新型有效的治疗策略迫在眉睫。近期,《Nature》杂志刊登的一项研究报告,揭示了一种针对NSD2的抑制剂,有望为肺癌和胰腺癌的治疗带来新的希望。
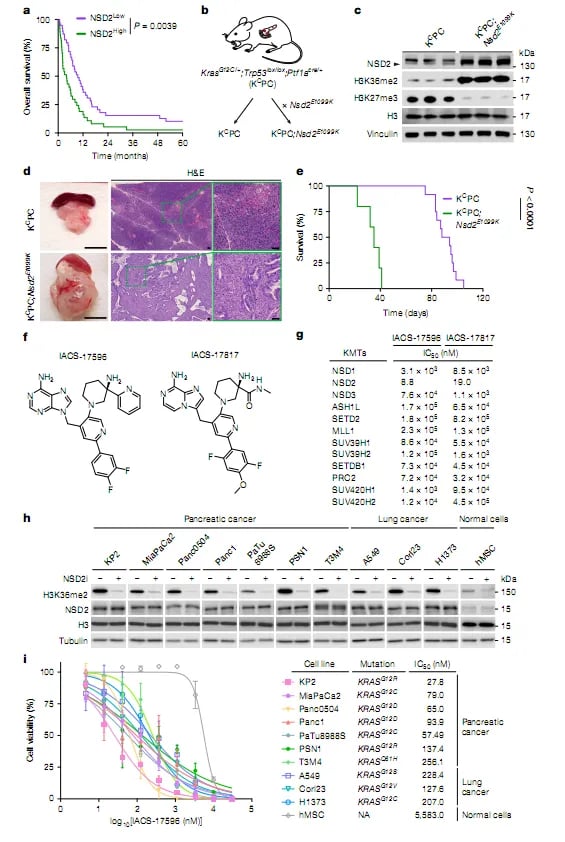
NSD2是一种关键的表观遗传修饰酶,其异常激活与多种癌症的发生发展密切相关。研究人员成功开发了一系列高选择性、高活性的NSD2抑制剂(NSD2i),并系统评估了其在KRAS驱动的肺癌和胰腺癌模型中的治疗效果。这一突破性进展为开发针对这些难治性癌症的靶向疗法开辟了新途径。对于正在寻找前沿靶向药的患者,了解这类研究进展至关重要。您可以通过MedFind的药品代购服务,探索全球最新的抗癌药物选择。
人类基因数据库上线:解读近50万英国人的“生命源代码”
基因、环境与运气,究竟谁在疾病发生中占据主导?一项发表在《Nature》上的重磅研究,通过对490,640名英国人的全基因组测序,构建了人类最大的基因数据库,为我们解读“生命源代码”提供了前所未有的视角。
这项研究挖出了15亿个变异,比传统技术暴涨数十倍,首次将90%的非编码“暗物质”拉到聚光灯下。研究发现,这些隐形段落中藏着甲状腺功能减退、白内障等常见病的开关。更重要的是,研究揭示了同样的突变在不同祖先背景下可能产生天差地别的结局,强调了基因组学研究中考虑人群多样性的重要性。这些海量数据将极大地推动疾病机制研究和个性化医疗的发展。如果您想了解更多前沿抗癌资讯,MedFind的资讯平台将为您提供最新、最全面的信息。
遗传性脑病:脑部细胞移植带来生命之门
泰-萨克斯病和桑霍夫病等遗传性脑病是一类罕见但极其严重的神经退行性疾病,通常在患者生命早期导致死亡。目前尚无有效治疗方法。近期,《Nature》杂志刊登的一项研究报告,为治疗这些罕见疾病带来了新的希望。
斯坦福大学的科学家们开发了一种新方法,能在不进行全身性毒性预处理的情况下,将超过一半的受损小胶质细胞替换为非基因匹配的前体细胞。这项研究的核心是开发一种脑部限制性的高效率小胶质细胞替代方法,发现Sca1定向前体细胞在脑内注射后能够高效地替代小胶质细胞,避免了移植物抗宿主病等并发症。这一突破性进展为遗传性脑病患者打开了生命之门。
免疫学新发现:B-1a细胞如何控制炎症?
B-1a细胞是一类先天免疫样B细胞,在快速产生天然抗体和分泌抗炎因子方面发挥着重要作用,有助于防止过度炎症反应和自身免疫性疾病。然而,这类细胞在人体中是否存在、如何维持、功能如何调控,一直是免疫学领域的争议焦点。一项发表在《Nature》上的研究不仅确认了人类B-1a细胞的存在,还揭示了两个关键转录因子TCF1和LEF1如何调控这群细胞的生存与功能。
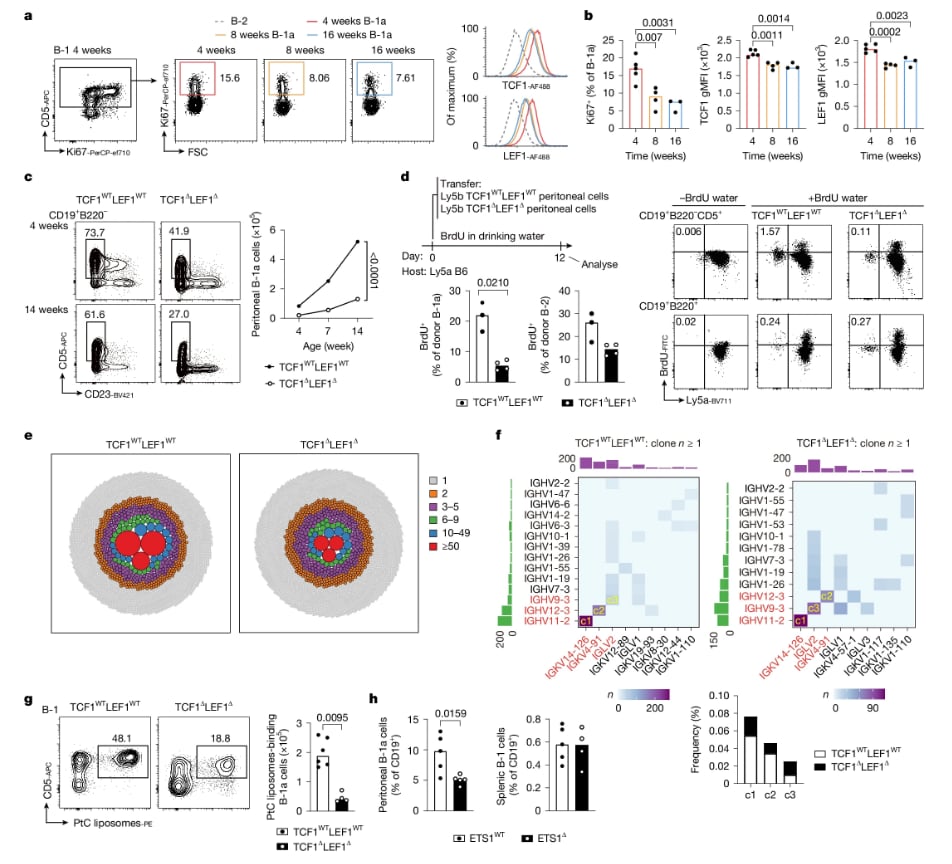
这项研究解开了免疫学中的一个谜团,为未来治疗自身免疫疾病、慢性感染甚至癌症提供了新思路。深入理解免疫系统的复杂性,对于开发更精准的治疗方案至关重要。如果您对复杂的医学研究有疑问,可以尝试MedFind的AI问诊服务,获取专业的解读和建议。
慢性疼痛难题有望破解:SLC45A4基因带来新希望
慢性疼痛困扰着全球五分之一的成年人,是全球致残的首要原因,但现有治疗手段往往疗效有限。近期,《Nature》杂志刊登的一项研究报告,发现了一种名为SLC45A4的基因,其能编码一种神经元多胺转运蛋白且与慢性疼痛密切相关。
研究人员通过全基因组关联研究(GWAS)分析发现,SLC45A4基因中的某些单核苷酸变异与疼痛强度显著相关,并在多个大型人群队列中得到验证。这一发现不仅为理解疼痛的分子机制提供了新的视角,还可能为开发新型镇痛药物开辟道路,为慢性疼痛患者带来新的治疗希望。
癌症治疗瓶颈突破:新型细胞周期抑制剂的发现之旅
癌症的复杂性和多样性使得治疗面临重重挑战,而细胞周期的异常调控是癌症发生发展的重要因素之一。开发针对细胞周期调控的新型药物成为了癌症治疗领域的前沿热点。近期,《Nature》杂志刊登的一项研究报告,开发了一种治疗小细胞肺癌的新型策略。
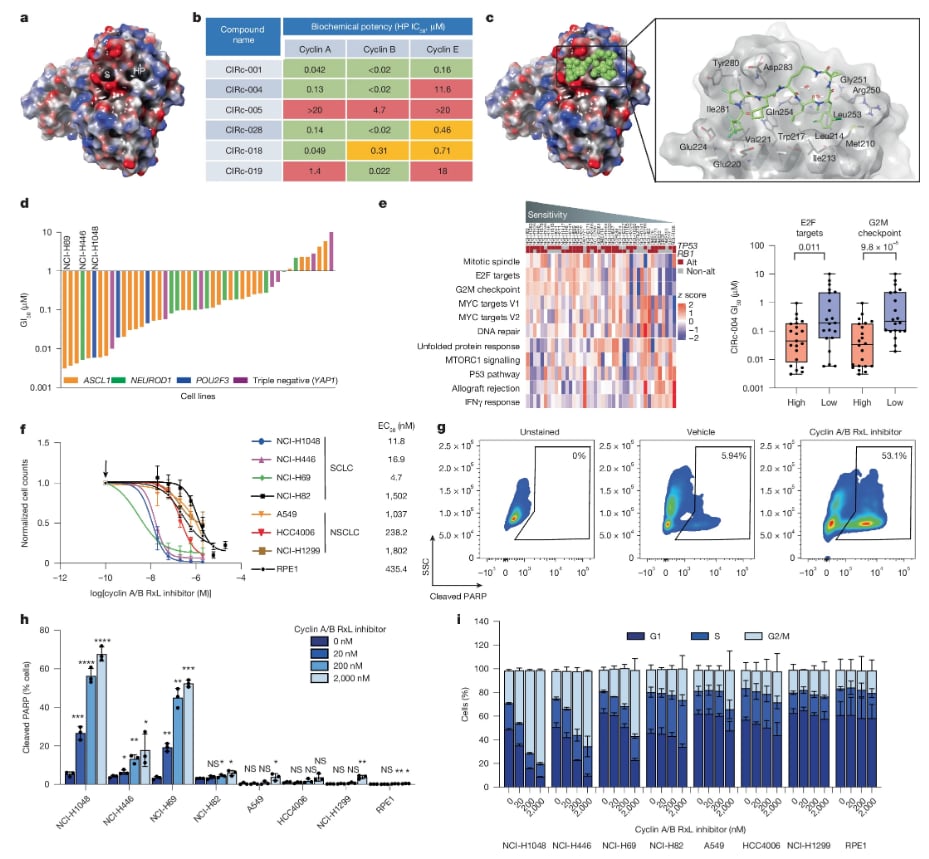
研究者开发了一种新型的细胞周期抑制剂,尤其是针对细胞周期蛋白A和B的RxL基序抑制剂。在小细胞肺癌(SCLC)等某些癌症类型中,细胞周期蛋白A和B的活性异常升高会导致细胞过度增殖和肿瘤形成。因此,抑制其活性有望成为有效的癌症治疗策略,有望进一步推动临床试验的开展。
癌症“绑架”神经系统:PD-1抑制剂耐药机制揭示
癌症不仅侵蚀器官,还能狡黠地“操控”神经系统,进而使免疫治疗这一抗癌利器失去效力。近期,《Nature》杂志发表的一项重磅研究,揭示了全新的抗癌耐药机制——癌细胞能够主动损害机体周围神经,引发慢性炎症,进而诱导免疫系统“叛变”,最终致使免疫治疗宣告失败。
研究人员聚焦于“神经周围侵犯”(PNI)现象,发现接受PD-1抑制剂治疗无响应的皮肤癌患者中,PNI现象的比例显著更高。进一步探究发现,受侵犯的神经会呈现“受伤状态”,大量高表达损伤标志物,表明神经损伤与机体对抗PD-1抑制剂疗法的耐受性之间存在直接且紧密的关联。这项研究精准阐释了部分患者对PD-1抑制剂治疗无反应的深层原因,并为逆转耐药提供了一系列创新策略,为黑色素瘤、皮肤鳞癌、胃癌等多种癌症的治疗带来新思路。
胶质母细胞瘤:阻断大脑损伤或能减缓肿瘤生长
胶质母细胞瘤(GBM)因其高度侵袭性和治疗抵抗性,是神经科学领域中最棘手的难题之一。尽管医学技术不断进步,但患者生存期仍不理想。近期,《Nature》杂志刊登的一项研究发现,轴突损伤可能是胶质母细胞瘤进展的关键驱动因素,而抑制这一过程或许能成为治疗胶质母细胞瘤的新策略。
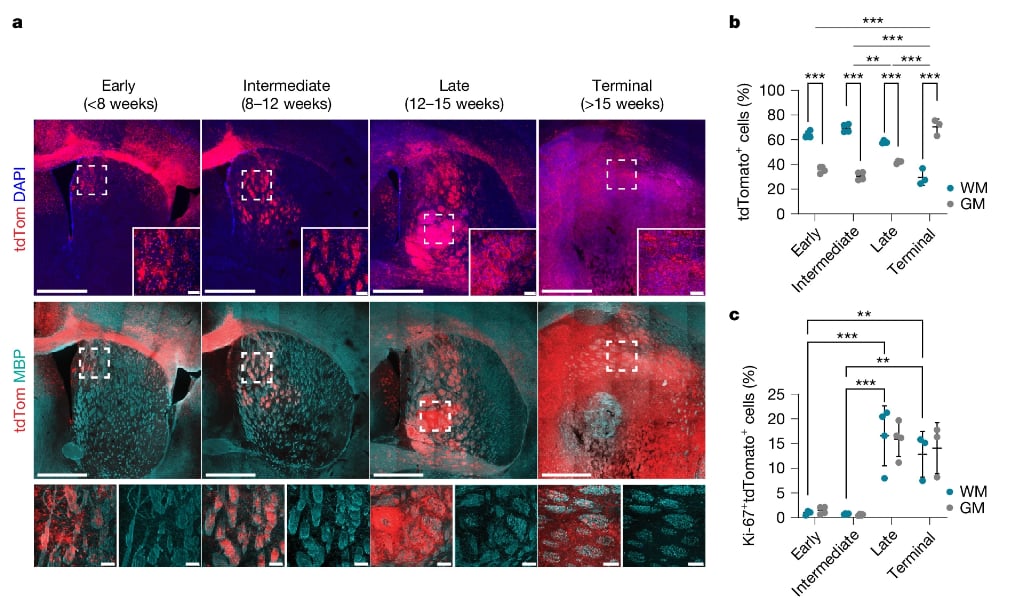
研究人员旨在探索轴突损伤在胶质母细胞瘤早期发展中的作用,并验证抑制轴突损伤是否能减缓肿瘤进展。通过小鼠模型和患者来源的异种移植(PDX)模型等多种实验,研究发现肿瘤的发展会优先出现在大脑白质中,且轴突损伤与肿瘤进展密切相关。这一发现不仅有助于我们更好地理解胶质母细胞瘤的发病机制,还可能为开发新的治疗方法提供理论基础。





