癌症,作为全球性的健康难题,其复杂多变性使得治疗之路充满挑战。然而,随着医学科研的不断深入,科学家们正逐步揭示癌症发生的深层机制,为攻克这一顽疾带来新的曙光。其中,细胞周期的异常调控被认为是癌症发生发展的关键因素之一。细胞周期是细胞生长、复制和分裂的生命律动,而其精确性依赖于一系列蛋白质的协同作用,特别是细胞周期蛋白(Cyclin)和细胞周期蛋白依赖性激酶(CDK)。当这些关键调控因子失控,细胞便可能无限制增殖,最终形成肿瘤。因此,开发针对细胞周期关键环节的创新药物,已成为癌症治疗领域的前沿焦点。
近日,国际权威期刊Nature发表了一项突破性研究,题为“Targeting G1–S-checkpoint-compromised cancers with cyclin A/B RxL inhibitors”。该研究由哈佛医学院等机构的科学家团队主导,成功开发出一种治疗小细胞肺癌(SCLC)的全新策略,有望为未来的临床试验奠定基础。这项研究的核心在于发现了一种新型的细胞周期抑制剂,特别是针对细胞周期蛋白A和细胞周期蛋白B的RxL基序抑制剂。
靶向细胞周期蛋白A/B:小细胞肺癌治疗的新希望
细胞周期蛋白A和细胞周期蛋白B在细胞周期的精确调控中扮演着至关重要的角色,它们通过与特定底物蛋白的相互作用,精细控制着细胞的增殖与分裂进程。在多种癌症类型中,尤其是像小细胞肺癌这类恶性程度较高的肿瘤中,细胞周期蛋白A和细胞周期蛋白B的活性异常升高,是导致细胞过度增殖和肿瘤形成的关键驱动力。因此,精准抑制这两种细胞周期蛋白的活性,被视为一种极具潜力的癌症治疗策略。
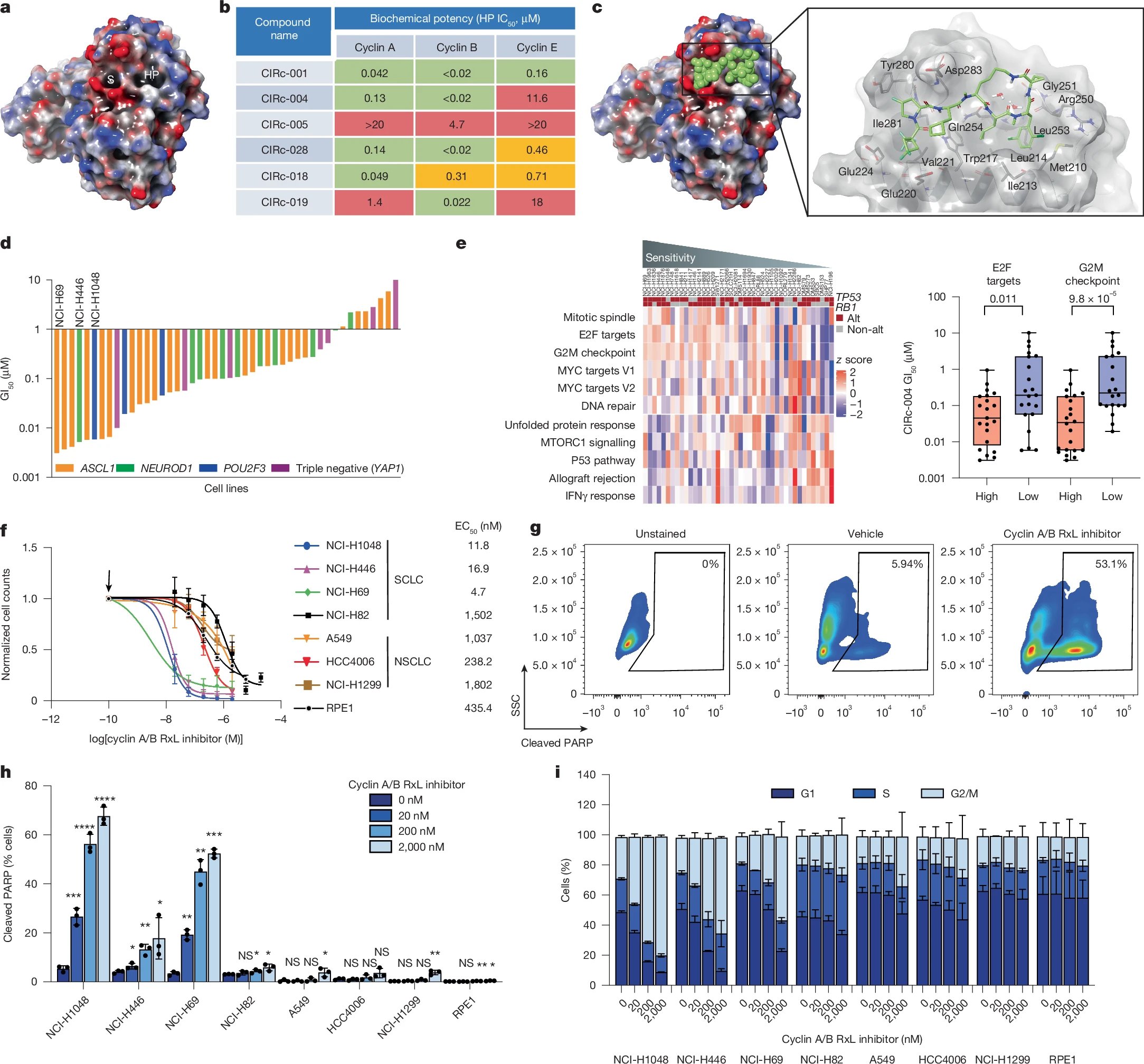
研究团队精心设计并合成了一系列具有良好细胞渗透性和口服生物利用度的巨环肽抑制剂。这些抑制剂能够特异性地结合到细胞周期蛋白A和细胞周期蛋白B的RxL基序上,从而有效阻断它们与底物蛋白的相互作用。在实验阶段,研究人员采用了多种小细胞肺癌细胞系(如NCI-H69、NCI-H1048等)以及正常细胞系(如WI-38成纤维细胞)进行对比研究。通过细胞增殖实验、流式细胞术分析、免疫印迹实验、基因编辑筛选以及动物模型实验等一系列严谨的科学流程,全面评估了新型抑制剂的抗肿瘤活性、细胞毒性及其作用机制。
CIRc-004:双重打击肿瘤细胞的创新机制
实验结果令人鼓舞:新型细胞周期蛋白A/B RxL抑制剂,例如代号为CIRc-004的化合物,在多种小细胞肺癌细胞系中展现出显著的抗增殖活性,而对正常细胞的影响微乎其微,这充分证明了其高度的选择性和较低的毒性。深入的机制研究揭示,CIRc-004通过阻断细胞周期蛋白A与E2F1的相互作用,导致E2F1活性过度升高,进而诱导细胞周期阻滞和细胞凋亡。更值得关注的是,CIRc-004还能通过阻断细胞周期蛋白B与MYT1的相互作用,激活纺锤体组装检查点(SAC),最终导致有丝分裂细胞死亡,实现了对肿瘤细胞的“双重打击”。
在动物模型实验中,口服给药的CIRc-014(原文提及,可能为CIRc-004的口服优化版本或相关化合物)在化疗耐药的小细胞肺癌患者来源异种移植(PDX)模型中,展现出强大的抗肿瘤活性,并且未观察到明显的毒性反应。这一发现无疑为小细胞肺癌等难治性癌症的治疗带来了新的希望和潜在的治疗策略。
这项研究的重大意义在于,它不仅开发出一种具有良好细胞渗透性和口服生物利用度的新型细胞周期蛋白A/B RxL抑制剂,更重要的是,该抑制剂在体外和体内模型中均表现出卓越的抗肿瘤效果。通过同时靶向细胞周期蛋白A和细胞周期蛋白B,这种抑制剂为肿瘤细胞提供了双重打击,为未来小细胞肺癌及其他相关癌症的治疗开辟了全新的路径。
了解更多前沿抗癌资讯,可访问 MedFind抗癌资讯平台。对于需要海外靶向药的患者,MedFind海外靶向药代购服务提供便捷可靠的购药途径。若您对治疗方案有疑问,MedFind的AI问诊服务也能提供初步参考。
参考文献:
Singh, S., Gleason, C.E., Fang, M. et al. Targeting G1–S-checkpoint-compromised cancers with cyclin A/B RxL inhibitors. Nature (2025). doi:10.1038/s41586-025-09433-w





