阿美替尼(Almonertinib)作为一种先进的第三代EGFR靶向药,对携带EGFR敏感突变及T790M耐药突变的非小细胞肺癌(NSCLC)显示出显著疗效。然而,正如其他靶向治疗一样,阿美替尼的耐药性问题仍然是临床上面临的一大挑战。已有的研究提示,其耐药机制可能涉及继发性EGFR突变或旁路信号通路的激活。本文将分享一个特殊的临床案例:一名患有罕见EGFR L861Q突变的肺腺鳞癌(ASC)患者,在使用阿美替尼治疗后,肿瘤组织学类型转变为大细胞神经内分泌癌(LCNEC)。
该患者在接受阿美替尼治疗约8个月后,影像学检查显示疾病进展。值得注意的是,血液基因检测不仅再次检测到EGFR L861Q突变,还发现了EGFR L858R以及RB1和TP53等关键基因的突变。为了明确耐药机制,患者接受了再次活检,病理结果令人意外地证实肿瘤已转化为大细胞神经内分泌癌。基于这一发现,调整治疗策略为以顺铂联合依托泊苷为基础的化疗方案,并观察到了积极的治疗效果。这个病例提示,组织学转化为神经内分泌癌是肺腺鳞癌对阿美替尼产生耐药的一种可能机制,并且即使发生了转化,原有的EGFR突变仍可能存在。因此,对于接受阿美替尼或其他EGFR-TKI治疗的非小细胞肺癌患者,在出现耐药迹象时,及时进行病理组织活检具有极其重要的临床指导意义。对于需要了解阿美替尼价格或寻求可靠阿美替尼代购渠道的患者,获取全面的药物信息至关重要。
病例背景介绍
肺腺鳞癌(ASC)是非小细胞肺癌(NSCLC)中一种较为少见的混合型亚型,约占所有肺癌的2%–3%。流行病学数据显示,ASC在男性和有吸烟史的人群中更为常见。分子层面研究发现,ASC可能涉及多种基因突变,包括EGFR、ERBB2、KRAS、BRAF、PIK3CA、RET、ALK等。本案例聚焦于一位携带罕见EGFR L861Q突变的ASC患者,在接受阿美替尼这一靶向药治疗后出现病情进展,通过重复活检明确了其耐药机制为向大细胞神经内分泌癌(LCNEC)的转化,并最终通过针对性的化疗方案有效控制了病情。
详细诊疗经过
患者为一名43岁男性,无吸烟史。其诊疗时间线如图1所示。2021年11月,因咳嗽、咯血、胸闷就诊,CT发现右肺上叶占位伴多处转移。12月,经肺组织和胸膜活检,病理诊断为肺腺鳞癌。免疫组化结果支持该诊断(图2A),临床分期为IVa期。基因检测揭示存在EGFR L861Q(丰度70.50%)和PTEN突变。患者开始接受每日110mg阿美替尼口服治疗,初期病情稳定(SD)。
然而,2022年8月复查CT显示胸膜转移灶增大并出现心包积液,评估为疾病进展(PD)。由于患者当时拒绝再次组织活检,进行了血液基因检测,结果显示EGFR L861Q(丰度11.00%)、EGFR L858M(丰度11.94%),同时检出RB1(9.20%)、TP53(12.97%)、PTEN(12.51%)和SMARCA4(0.96%)等突变。随后患者尝试了“培美曲塞+顺铂+贝伐珠单抗+信迪利单抗”的联合方案治疗3周期,但效果不佳,病情持续恶化,出现脑、肝、骨转移,胸闷气促症状加剧。
考虑到神经元特异性烯醇化酶(NSE)指标显著升高,提示神经内分泌肿瘤的可能性,于2023年2月再次进行了肺组织活检。这次的病理结果确诊为大细胞神经内分泌癌(LCNEC)。免疫组化特征也发生了显著变化(图2B-E),Ki-67指数高达95%+,证实了从ASC向LCNEC的病理转化是导致阿美替尼耐药的原因。面对如此复杂的病情演变,患者和家属可能会感到困惑,此时,利用如MedFind AI问诊这样的工具进行初步咨询,或许能帮助梳理治疗思路。
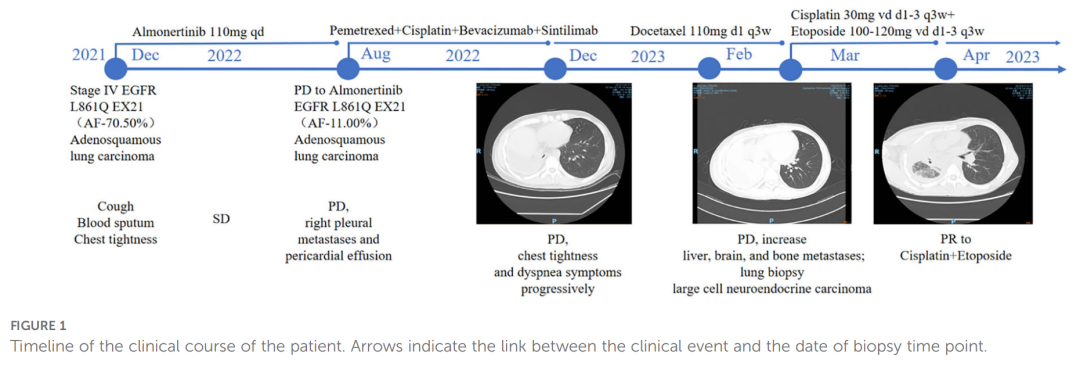
▲图1 患者临床病程的时间线
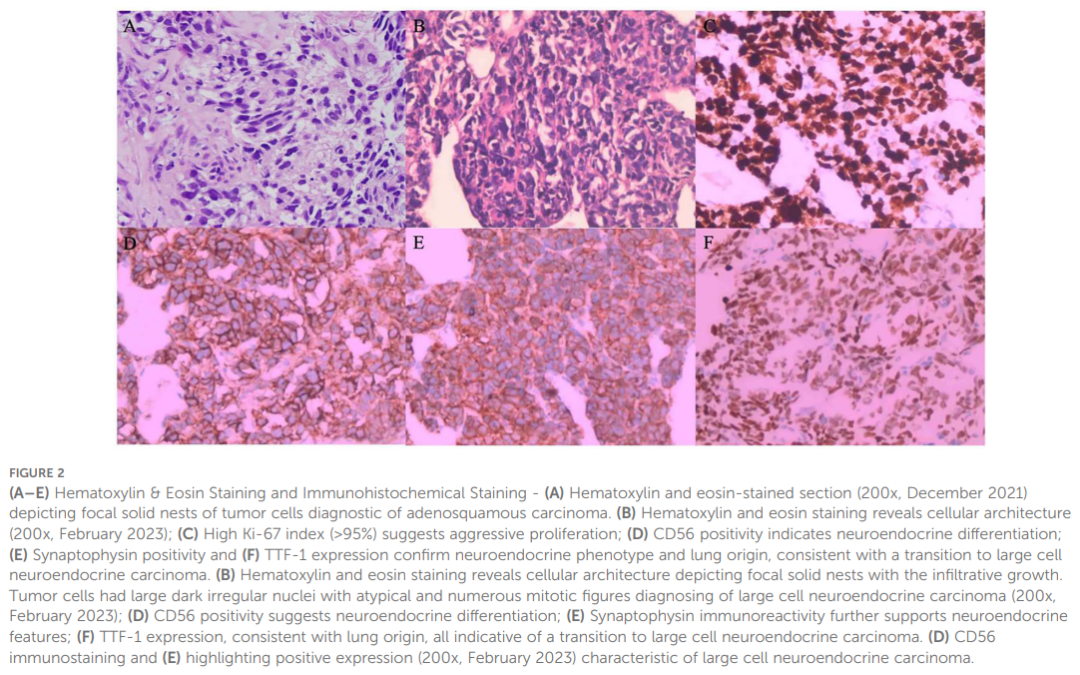
▲图2 HE染色和免疫组化结果
讨论与启示
据我们所知,这是首次报道使用阿美替尼治疗后,肺腺鳞癌(ASC)转化为大细胞神经内分泌癌(LCNEC)的案例。ASC本身是一种侵袭性较强的NSCLC亚型,预后相对较差。携带EGFR突变的ASC患者通常对EGFR-TKI治疗反应良好,这与肺腺癌相似。
阿美替尼作为中国自主研发的第三代EGFR-TKI,不仅对常见EGFR突变有效,对T790M耐药突变也具有强大的抑制活性。临床研究(如AIM研究和AENEAS研究)已证实,阿美替尼在EGFR突变(包括G719X、L861Q、S768I等罕见突变)NSCLC患者的一线和二线治疗中均表现出优越的疗效和良好的安全性。寻找可靠的阿美替尼购买渠道,了解其在全球不同市场的价格差异,是许多患者关心的问题,MedFind等海外药房代购平台可提供相关信息。
本案例中,患者在阿美替尼治疗8个月后出现进展,血液基因检测发现了EGFR L861Q、L858M以及RB1、TP53等共突变。结合最终的病理活检结果(LCNEC),明确了其耐药机制是组织学转化,而非典型的继发EGFR突变(如C797S)或旁路激活(如MET扩增)。
大细胞神经内分泌癌(LCNEC)和小细胞肺癌(SCLC)同属于高级别神经内分泌肿瘤,两者在临床和基因层面有诸多相似之处。腺癌向SCLC转化的机制研究相对较多,通常认为与TP53和RB1基因的失活密切相关。这两个基因的缺失是SCLC的标志性特征。此外,MYC扩增、PTEN通路改变、NOTCH信号通路失活等也可能参与其中。虽然关于LCNEC转化的具体机制研究尚少,但推测可能与SCLC的转化通路有共通之处。本案例中ASC向LCNEC的转化机制,尤其是在阿美替尼治疗背景下,值得进一步深入研究。
现有研究提示,同时携带EGFR/RB1/TP53三重突变的NSCLC患者,发生向SCLC转化的风险更高。本案例患者二次基因检测恰好符合这一特征。遗憾的是,患者在首次确认耐药后未能立即进行活检,尝试的化疗联合免疫治疗方案效果不佳。直到6个月后再次活检才最终确诊LCNEC。LCNEC目前的标准治疗仍以化疗为主,常参考SCLC的方案。基于此,医生为该患者选用了EP方案(顺铂+依托泊苷),治疗两个周期后评估为部分缓解(PR),患者症状明显改善,证明了该方案的有效性。
总结来说,本案例强调了以下几点:
- 组织学转化为神经内分泌癌(如LCNEC)是阿美替尼等EGFR-TKI获得性耐药的机制之一。
- 即使发生转化,原有的EGFR突变可能仍然存在。
- 对于EGFR-TKI治疗后耐药的患者,尤其是检测到EGFR/RB1/TP53共突变的患者,强烈建议及时进行重复组织活检,以明确耐药机制,指导后续治疗。
- 对于转化为LCNEC的患者,以铂类为基础的化疗(如EP方案)是有效的治疗选择。
获取准确的诊断和基因信息对于制定最佳治疗策略至关重要。未来,更先进的分子检测技术有望帮助我们更早地识别这种转化的风险。更多关于靶向药、仿制药的最新资讯和治疗进展,可以在MedFind抗癌资讯版块查阅。
参考文献:
Cheng K, Zhu Y, Sang R, Kuang Z, Cao Y. Case report: A patient with EGFR L861Q positive adenosquamous lung carcinoma transforming into large cell neuroendocrine cancer after treatment with Almonertinib. Front Oncol. 2025 Feb 18;15:1453066. doi: 10.3389/fonc.2025.1453066. PMID: 40040728; PMCID: PMC11876032. (原始文献信息,仅供参考)






