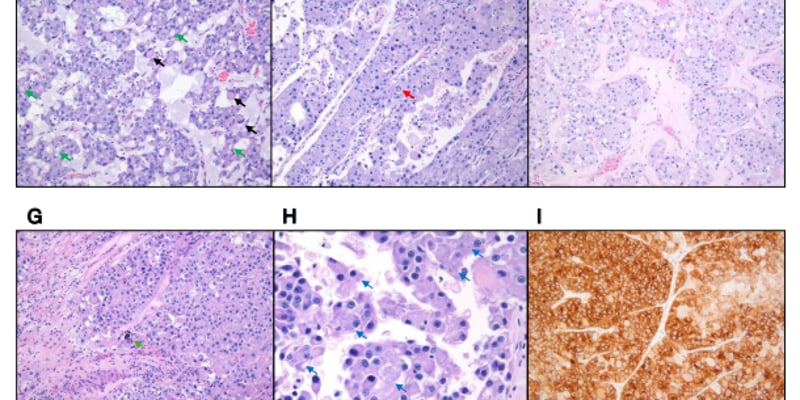
对于晚期高级别非黏液性上皮性卵巢癌患者而言,同源重组缺陷(HRD)状态的检测已成为指导后续维持治疗,特别是聚腺苷二磷酸核糖聚合酶抑制剂(PARPi)用药决策的核心依据。国际指南明确推荐所有晚期高级别上皮性卵巢癌患者都应接受HRD肿瘤基因组检测。然而,在临床实践中,部分患者可能因为病情进展快或未接受初始肿瘤细胞减灭术等原因,缺乏足够的手术组织样本进行检测,这给临床诊断带来了挑战。本篇深度解析基于一项真实世界研究,旨在评估在缺乏标准手术组织的情况下,如何通过替代样本(如腹水、胸腔积液或粗针穿刺活检)高效、准确地完成HRD检测,从而确保患者能够及时启动如奥拉帕利(Olaparib)或尼拉帕利(Niraparib)等PARP抑制剂的维持治疗,最大化生存获益。
HRD检测:PARP抑制剂维持治疗的基石
卵巢癌是全球女性常见的恶性肿瘤之一,由于缺乏有效的早期筛查手段,多数患者确诊时已处于晚期。尽管初始治疗(手术联合化疗)效果显著,但高达80%的患者最终会面临疾病复发。近年来,靶向治疗的突破,特别是PARP抑制剂的应用,极大地改善了晚期卵巢癌患者的预后。
同源重组缺陷(HRD)与PARPi的合成致死效应
约50%的高级别非黏液性上皮性卵巢癌具有HRD特征。同源重组(HR)是DNA双链断裂修复通路中一种高保真度的修复机制。当HR通路发生缺陷(即HRD)时,细胞转而依赖其他低保真度的修复机制,如PARP介导的单链断裂修复。
PARP抑制剂正是利用了这种“合成致死”的原理:
- 在HRD肿瘤细胞中,PARP抑制剂通过阻断PARP功能,导致DNA损伤无法被有效修复。
- 由于HR通路本身也存在缺陷,细胞无法启动备用修复机制。
- 最终,DNA损伤累积,导致肿瘤细胞凋亡。
HRD状态通常由BRCA1/2基因突变(胚系或体细胞)或基因组不稳定性(如杂合性缺失LOH、端粒等位基因失衡TAI、大规模基因组状态转换LST)共同决定。
PARPi在卵巢癌维持治疗中的地位
多项关键临床试验确立了PARPi在卵巢癌一线维持治疗中的核心地位:
- SOLO-1试验:证实对于新确诊携带BRCA1/2突变的晚期卵巢癌患者,使用口服PARPi奥拉帕利进行一线维持治疗,可显著延长患者的无进展生存期(PFS)。
- PRIMA试验:显示PARPi尼拉帕利相较于安慰剂,能显著延长HRD阳性肿瘤患者的PFS,无论其BRCA突变状态如何。
- PAOLA-1试验:证实对于HRD阳性且BRCA野生型(BRCAwt)的晚期卵巢癌患者,奥拉帕利联合贝伐珠单抗进行一线维持治疗,同样能带来显著的PFS获益。
基于这些证据,国际和国家指南均推荐对所有晚期高级别上皮性卵巢癌患者进行BRCA及HRD肿瘤基因组检测,以指导PARPi的精准用药。患者如果希望了解这些药物的海外用药选择和获取渠道,可以进一步咨询专业平台。
真实世界研究:HRD检测样本获取的成功率分析
本研究回顾性分析了西澳大利亚州立妇科癌症中心(WAGCS)开展HRD检测首年的真实世界数据,重点关注影响HRD确诊检测结果的因素,特别是对于那些没有标准手术组织的患者。
研究方法与检测平台
该中心是西澳大利亚州唯一的公立妇科癌症诊疗机构。研究期间,HRD检测采用了两种不同的二代测序(NGS)平台:
- 早期:采用赛菲亚基因(SOPHiA Genetics)的SOPHiA DDM HRD检测试剂盒,通过基因组不稳定性指数(GII)评估HRD状态。
- 后期:改用因美纳(Illumina)TruSight Oncology 500(TSO 500)靶向杂交捕获NGS试剂盒,通过基因组不稳定性评分(GIS)评估HRD状态。GIS由LOH、TAI及LST三项指标计算得出,评分≥42判定为HRD阳性。
无论采用哪种方法,样本肿瘤细胞占比均需≥30%方可纳入检测。样本来源包括手术组织、影像引导下粗针穿刺活检组织,以及经过离心富集处理的腹水/胸腔积液样本。
核心结果:高完成率与阳性率
研究共纳入84例符合HRD检测指征的患者,其中79例接受了检测。检测完成率非常高,总共79名患者中,仅有3名(3.8%)的检测结果因肿瘤组织量不足(存活肿瘤细胞占比低于30%)而无法确诊(非诊断性/不确定结果)。
在76例获得明确HRD检测结果的患者中:
- HRD阳性率:38.2% (29例)。
- BRCA突变情况:29例HRD阳性患者中,6例(20.7%)检测出体细胞BRCA突变,23例(79.3%)为HRD阳性、BRCA野生型(BRCAwt)。
此外,该中心胚系检测的依从率为85.7%,肿瘤检测的依从率为94%,虽然略低于国际指南推荐的95%标准,但考虑到部分患者因疾病快速进展或拒绝检测,这一依从率仍具有重要的临床参考价值。
关键发现:非手术样本的检测成功率
该研究最关键的结论在于对不同样本采集方式的成功率评估,这为临床医生在没有手术标本时如何获取诊断依据提供了明确指导:
1. 腹水/胸腔积液样本:100%成功率
所有送检的腹水/胸腔积液样本均获得了明确的诊断结果。这一发现与现有文献一致,表明腹水中的游离肿瘤DNA(cftDNA)或富集的肿瘤细胞检测效能与肿瘤组织检测具有可比性。对于晚期卵巢癌患者,腹水或胸腔积液的采集相对微创且容易获取,是缺乏实体瘤组织时的理想替代样本。
2. 粗针穿刺活检样本:16G和18G表现优异
研究中,共有16例患者通过影像引导下粗针穿刺活检获取组织样本。结果显示:
- 16G和18G穿刺针获取的样本:均100%满足检测要求,并获得了明确的HRD诊断结果。
- 20G穿刺针获取的样本:2例采用20G穿刺针取样的患者中,有1例获得了非诊断性HRD结果。
这一数据有力支持了近期国际妇产科超声学会(ISUOG)/欧洲妇科肿瘤学会(ESGO)的共识声明:建议至少采用2枚18G或更粗规格的穿刺针取样,以确保获取足量的肿瘤细胞用于体细胞检测。
3. 化疗后样本的挑战
11例接受新辅助化疗且于间歇性肿瘤细胞减灭术时取样的患者中,10例的肿瘤组织量满足检测要求。然而,研究者强调,化疗暴露后采集的肿瘤样本,其存活肿瘤细胞占比和DNA提取产量通常较低,尤其是在化疗反应评分(CRS)为2~3分的样本中。理想情况下,HRD检测应采用全身治疗前采集的肿瘤组织样本,以避免化疗可能导致的基因启动子去甲基化或继发性回复突变,这些变化可能恢复BRCA功能,使检测结果无法真实反映患者的同源重组状态,进而影响PARPi的疗效判断。

图1

表1、2

图2

表3

表4
HRD检测的临床实践挑战与应对策略
尽管HRD检测在临床应用中取得了显著进展,但在实际操作中仍面临多重挑战,包括检测流程、结果解读和周转时间等。
检测周转时间与临床决策
本研究中,HRD检测从申请到结果报告的中位时长为57天(范围15~122天)。
- 初始手术患者:如果患者接受初始肿瘤细胞减灭术,并在术后开始6个周期(约126天)的化疗,57天的周转时间通常是可接受的,能够为指导PARPi维持治疗预留充足时间。
- 新辅助化疗患者:如果样本是在新辅助化疗后、间歇性肿瘤细胞减灭术时采集,57天的周转时间可能不够理想,可能延误维持治疗的启动。
因此,优化样本采集和检测流程,缩短周转时间,对于需要快速启动维持治疗的患者至关重要。
HRD阴性但伴有BRCA突变的特殊情况
研究中发现,有3例患者的基因组不稳定性评分(GIS)判定为HRD阴性,但进一步检测发现其携带肿瘤BRCA突变。据估计,高达10%的高级别上皮性卵巢癌患者可能存在致病性BRCA1/2肿瘤突变,但其基因组不稳定性评分却不符合HRD阳性特征。
这种现象的生物学机制复杂,可能包括:
- 野生型BRCA等位基因因启动子甲基化而沉默,导致功能缺失表型,但未伴随杂合性缺失(LOH)。
- 肿瘤内出现杂合性体细胞BRCA突变。
- BRCA回复突变,恢复了胚系突变等位基因的功能。
临床上认为,这类HRD阴性但携带BRCA突变的患者对PARPi的应答效果可能较差,需要更密切的监测。这也提示我们,HRD检测结果的解读不能仅仅依赖于GIS/GII评分,必须结合BRCA突变状态进行综合判断。
检测方法学的差异与标准化
HRD检测的临床应用受到检测方法学差异、检测流程要求与物流配送限制、HRD状态定义不统一等因素的显著影响。本研究中采用了两种不同的NGS平台(SOPHiA DDM和TSO 500),虽然都获得了高成功率,但不同平台之间对HRD状态的评估标准(GII vs GIS)存在差异,这可能限制PARPi治疗患者的最优筛选。
随着商业化NGS检测方法日益增多,缺乏标准化的检测流程和数据解读方案,使得HRD检测的准确性与可重复性面临挑战。尽管院内开展HRD检测有助于缩小分子分析与常规诊断之间的差距,但实现检测流程标准化与结果一致性仍是全球肿瘤学界需要解决的难题。
给患者及家属的建议:如何确保HRD检测成功
对于正在寻求晚期卵巢癌治疗方案的患者及家属,确保HRD检测成功是获得PARP抑制剂维持治疗机会的关键一步。以下是基于临床研究结果的实用建议:
1. 优先采集化疗前样本
如果可能,应在开始任何全身治疗(如新辅助化疗)之前采集肿瘤组织样本。化疗可能会改变肿瘤细胞的同源重组状态,导致检测结果失真。
2. 积极利用非手术样本
如果患者不适合进行初始肿瘤细胞减灭术,或者缺乏足够的组织标本,应积极考虑以下替代样本采集方式:
- 腹水或胸腔积液:这是成功率最高的替代样本之一,通过离心富集肿瘤细胞后进行检测,效果可靠。
- 影像引导下粗针穿刺活检:务必与医生沟通,确保采用16G或18G等较粗规格的穿刺针取样,以保证样本量和肿瘤细胞纯度达到检测要求(≥30%)。
3. 肿瘤与胚系基因同步检测
国际指南推荐同步进行肿瘤HRD检测和胚系基因检测。胚系检测通常以外周血为样本,可以明确患者是否遗传了BRCA1/2等基因突变,这不仅影响治疗决策,也对家族遗传风险评估至关重要。
4. 关注药物可及性与价格
一旦确诊为HRD阳性,患者将有资格接受PARP抑制剂(如奥拉帕利或尼拉帕利)的维持治疗。由于这些药物可能涉及长期用药,患者和家属需要提前了解药物的价格、购买渠道和医保覆盖情况。对于国内尚未上市或价格较高的药物,许多患者会选择通过专业平台获取海外直邮的仿制药或原研药,以确保治疗的连续性和经济性。如果您对特定药物的海外用药选择和咨询有疑问,可以寻求专业医疗咨询平台的帮助。
总结
本研究的真实世界数据证实了在晚期高级别非黏液性上皮性卵巢癌患者中,HRD检测具有很高的完成率。对于缺乏手术组织或不适合手术的患者,腹水/胸腔积液样本以及16G/18G粗针穿刺活检样本是获取明确HRD诊断结果的可靠途径。这一发现极大地拓宽了HRD检测的适用范围,有助于更多患者及时获得PARP抑制剂维持治疗的指导,从而改善长期生存预后。临床医生应优先采用化疗前采集的足量样本,并结合BRCA突变状态,对HRD检测结果进行全面评估,确保精准用药。
参考文献:
Planisamy K, Ctori E, Amanuel B, et al. Routine Tumor Testing for Homologous Recombination Deficiency in Patients With High Grade Epithelial Ovarian Cancer at a Statewide Gynecological Cancer Service in Western Australia: An Observational Study. Cancer Rep (Hoboken). 2025;8(9):e70335. doi:10.1002/cnr2.70335