尽管CAR-T细胞疗法在血液系统恶性肿瘤中取得了革命性成功,但其在治疗实体瘤方面的效果仍面临巨大挑战。主要原因在于实体瘤复杂的免疫抑制微环境,以及树突状细胞(DC)活性不足,特别是负责抗原交叉呈递的常规1型树突状细胞(cDC1)的稀缺与功能障碍,严重阻碍了T细胞的扩增和抗肿瘤反应。
CAR-T疗法在实体瘤中的困境与挑战
过继细胞疗法(ACT),以CAR-T为代表,已彻底改变了B细胞恶性肿瘤的治疗格局。然而,面对实体瘤,其疗效受限于多种因素,包括T细胞浸润不良、功能持久性降低、肿瘤抗原异质性以及免疫抑制性肿瘤微环境(TME)。相较之下,T细胞受体(TCR)工程化T细胞(TCR-T)和肿瘤浸润淋巴细胞(TIL)疗法在实体瘤治疗中展现出一定前景,它们依赖于淋巴结或肿瘤微环境中树突状细胞的广泛激活,这凸显了树突状细胞与T细胞相互作用的关键性。
创新策略:工程化T细胞激活抗肿瘤免疫
为了克服这些挑战,中国医学科学院系统医学研究院/苏州系统医学研究所张连军研究员、王宸研究员,中国科学院大学孙海汐研究员及苏州大学附属第二医院张力元教授团队,在国际知名期刊《Cell Reports Medicine》上发表了一项突破性研究。该研究提出了一种增强CAR-T实体瘤疗效的创新策略:通过基因工程改造T细胞,使其过表达Flt3L和XCL1。
研究发现,前体耗竭CD8+ T(Tpex)细胞高表达XCL1,这与患者对免疫检查点阻断的良好预后相关。鉴于XCL1-XCR1信号轴在招募cDC1中发挥关键作用,而Flt3L能促进树突状细胞的发育,研究团队将这两种分子整合到T细胞中,构建了工程化FX-T细胞。
Flt3L与XCL1:重塑肿瘤免疫微环境的关键
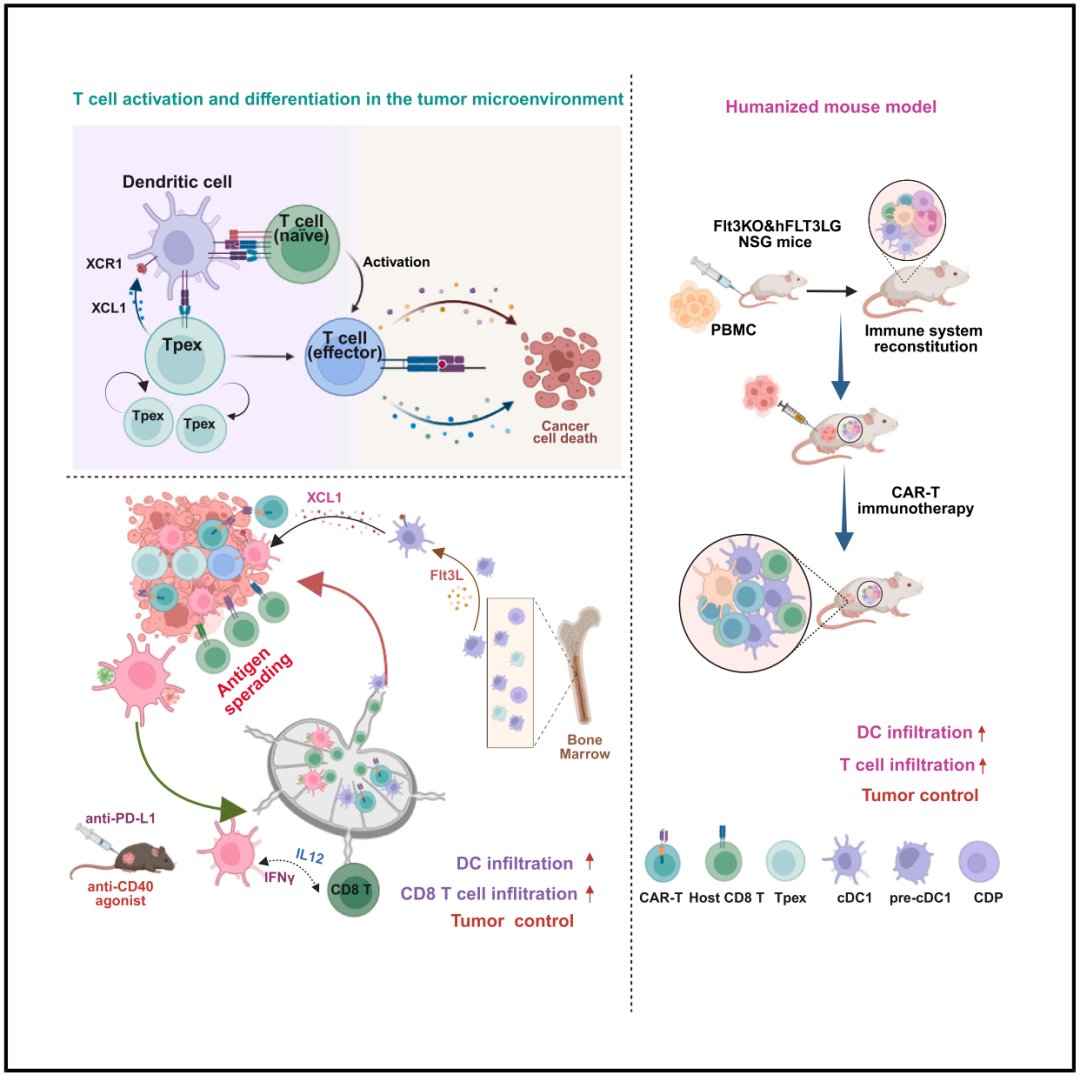
实验证实,这些经基因工程改造可分泌Flt3L和XCL1(FX)的过继转移T细胞,能够显著促进树突状细胞的迁移和成熟,并改善树突状细胞与T细胞的相互作用。更重要的是,FX-T细胞能有效诱导强大的抗原扩散效应和内源性多克隆T细胞反应,从而识别并清除具有异质性抗原的肿瘤,有效防止免疫逃逸。这项研究在临床前模型中,包括Flt3KO&hFLT3LG人源化小鼠模型,验证了携带FX的CAR-T细胞诱导抗原扩散的治疗效果。
核心研究发现总结:
- XCL1表达与CD8+ Tpex特征及患者对免疫检查点阻断的响应呈正相关。
- Flt3L和XCL1(FX)工程化修饰能有效重塑肿瘤微环境的免疫格局。
- 表达FX的T细胞能诱导强大的抗原扩散,并有效控制抗原异质性肿瘤。
- 表达FX的CAR-T细胞在小鼠和人源化小鼠模型中均表现出更优异的抗肿瘤活性。

这些突破性发现为优化CAR-T细胞疗法治疗实体瘤提供了令人信服的证据,为增强树突状细胞与T细胞的相互作用开辟了新途径,预示着未来实体瘤免疫治疗的巨大潜力。对于正在寻求最新癌症治疗方案的患者,了解这些前沿研究至关重要。
MedFind致力于为全球癌症患者提供全面的支持。如果您正在寻找海外靶向药,可以通过我们的药品代购服务获取所需药物。同时,我们的AI问诊服务能为您提供专业的初步咨询,而丰富的抗癌资讯则能帮助您及时了解最新的药物信息和诊疗指南。





