癌痛是许多实体瘤患者面临的严峻问题,但它不仅仅是一种症状。近年来的研究揭示,感觉神经作为肿瘤微环境(TME)的关键组成部分,不仅向大脑传递疼痛信号,还深刻影响着肿瘤的生长、扩散和对治疗的反应。了解感觉神经与癌症的复杂互动,可能为开发新的抗癌策略带来启发。
最近,《Trends in Cancer》杂志发表的一篇综述系统阐述了感觉神经系统在实体肿瘤中的核心作用,特别关注了癌痛的传导通路及其对肿瘤进展的影响,并探讨了干预这些通路的潜在治疗价值。

感觉神经与实体瘤:不仅仅是传递疼痛
传统观点认为神经系统主要通过自主神经(如交感神经)影响癌症,尤其是在压力反应下。然而,癌痛本身也被认为是癌症的一个重要标志。感觉神经末梢广泛分布于体内组织,能够感知并传递疼痛刺激。更重要的是,这些神经元还能释放神经肽等物质到肿瘤微环境中,直接调节肿瘤细胞、免疫细胞的行为,从而影响肿瘤进展。
临床上,治疗前的癌痛(如在口腔癌、皮肤癌、胰腺癌、卵巢癌等实体瘤中)往往预示着更晚期的疾病或神经浸润,提示预后不良。然而,不同癌症类型的疼痛程度差异很大,例如HPV阳性的头颈癌疼痛通常比HPV阴性的轻,而黑色素瘤的疼痛发生率相对较低,这表明肿瘤细胞自身的特性在疼痛产生中扮演重要角色。
癌痛信号的双向传导及其影响
感觉神经元具有独特的结构,可以将信号双向传导:
- 顺向传导(传入信号):将来自肿瘤微环境的疼痛刺激信号传递到中枢神经系统(脊髓、大脑),让我们感知到疼痛。肿瘤细胞及其相关的免疫细胞会分泌多种介质(如细胞外囊泡EVs、神经营养因子NGF、BDNF等),直接激活或“致敏”周围的感觉神经末梢,放大疼痛信号。
- 逆向传导(传出信号):感觉神经元被激活后,不仅向中枢发送信号,也会将信号逆向传回其在外周组织(肿瘤微环境)的末梢,释放神经肽,如降钙素基因相关肽(CGRP)和P物质(SP)。
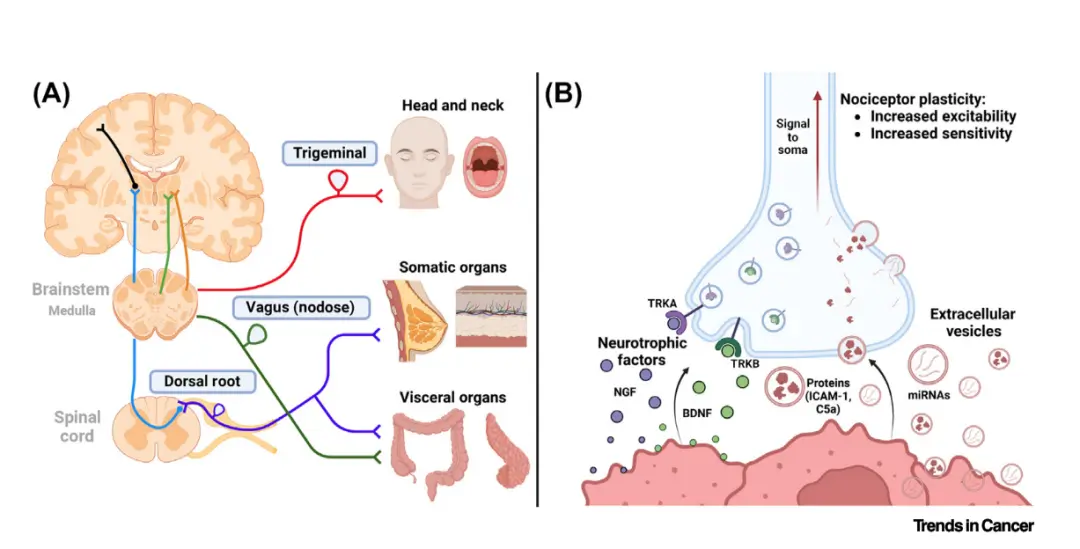
图1. 感觉神经支配和肿瘤微环境(TME)中的癌分泌致痛触发机制示意
神经肽如何影响肿瘤进展与免疫?
研究焦点逐渐集中在表达TRPV1(一种疼痛感受器)的感觉神经元亚群上。这些神经元释放的CGRP和SP对肿瘤进展和免疫反应具有重要影响。
- CGRP:研究表明,肿瘤微环境中的CGRP可以通过多种途径促进肿瘤进展。例如,它可以帮助癌细胞在不利环境下存活(如通过自噬),更重要的是,它可以抑制抗肿瘤免疫反应。在头颈癌和黑色素瘤模型中发现,CGRP会增加免疫细胞(如CD8+ T细胞)上的“耗竭”标记物,降低其杀伤肿瘤的能力。阻断CGRP信号(例如使用CGRP受体拮抗剂,这类药物已用于治疗偏头痛)可以减缓肿瘤生长,增加免疫细胞浸润,并可能增强免疫检查点抑制剂(ICI)的疗效。这提示靶向CGRP通路可能是一种有前景的抗癌新策略。
- SP:P物质(SP)及其受体NK1R也与肿瘤细胞的增殖、迁移有关。一些研究提示,感觉神经元释放的SP可能促进某些癌症(如胰腺癌)的早期病变发展。然而,SP的来源复杂(非神经细胞也能产生),其在肿瘤免疫中的确切作用仍需进一步研究。
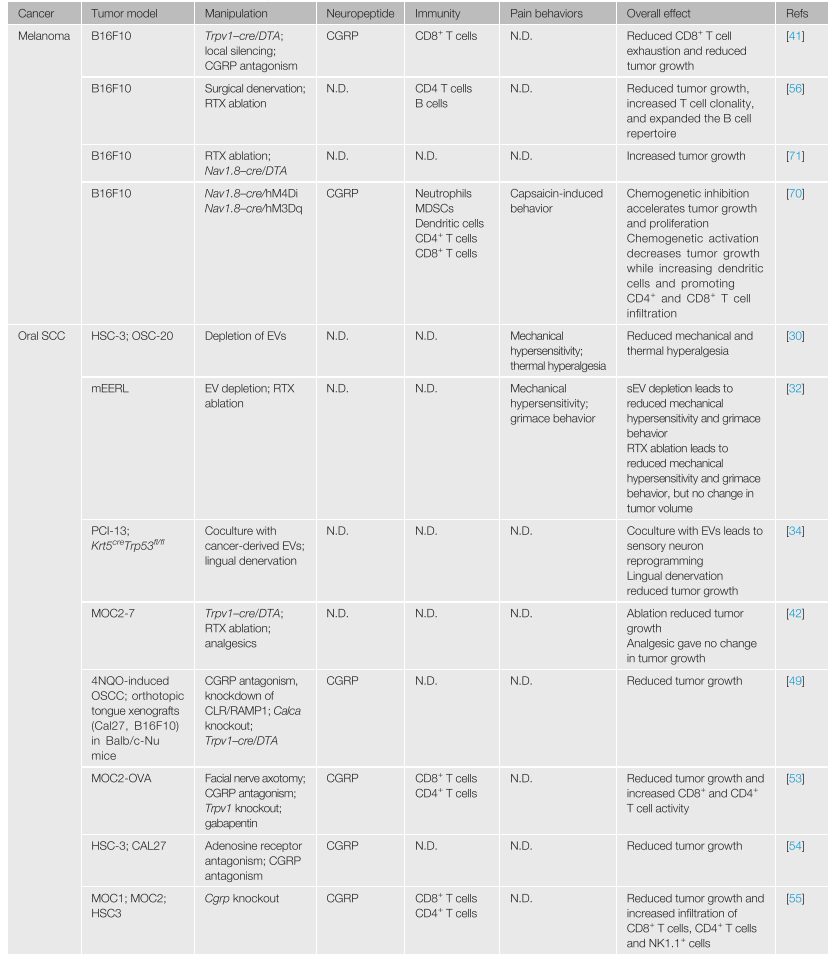
续表
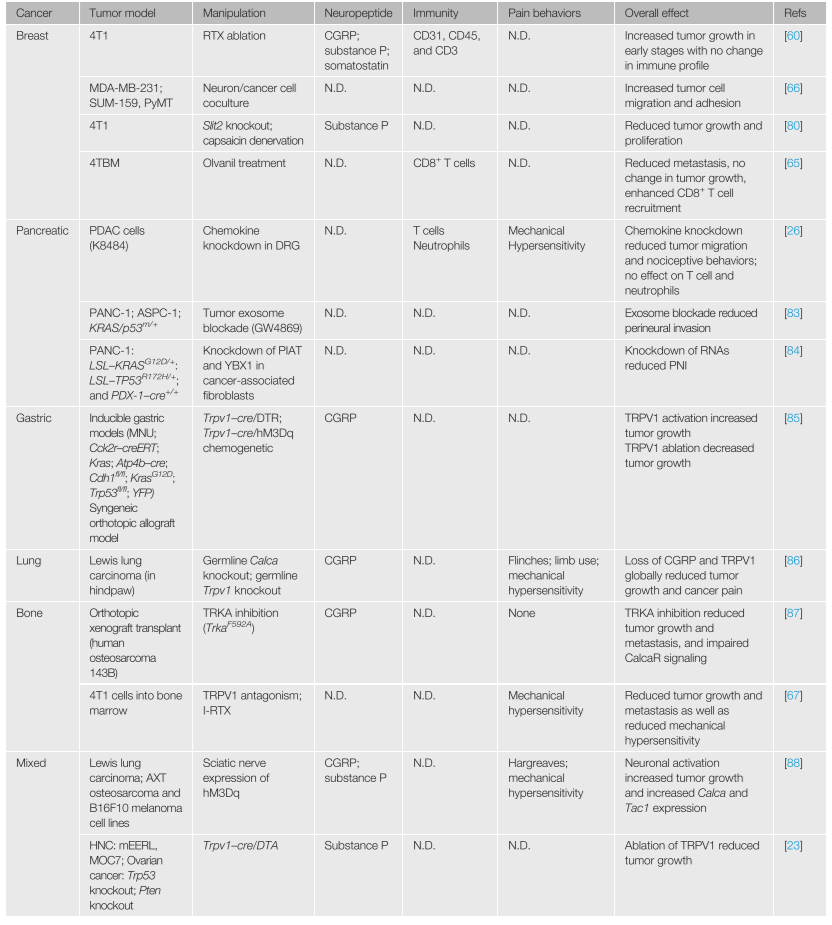
表1. 啮齿类动物模型中感觉神经元对肿瘤生长和相关免疫应答的影响 (2020-2024)
有趣的是,感觉神经信号也可能具有抑制肿瘤的作用。例如,在某些乳腺癌模型中,激活TRPV1神经元反而减少了转移并增强了CD8+ T细胞的募集。这提示感觉神经的作用可能是复杂且依赖于具体癌症类型和环境的。
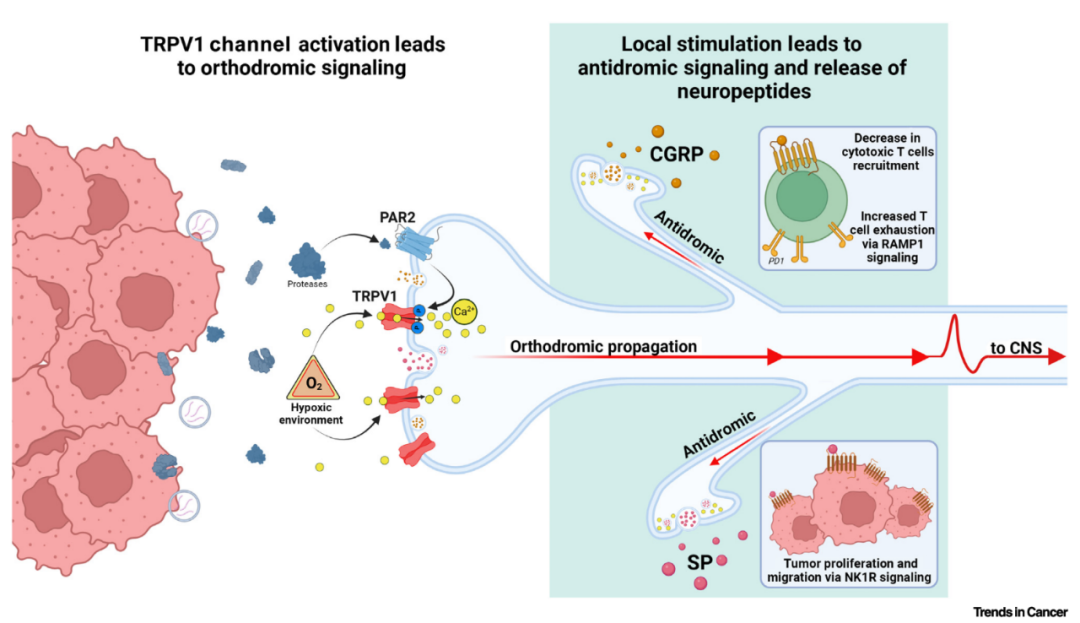
图2. 感觉神经肽释放的两种可能机制示意
癌痛、大脑与肿瘤进展的恶性循环
癌痛信号不仅传递到大脑引起疼痛感,还可能激活大脑中处理情绪、压力和自主神经调控的区域(如杏仁核、下丘脑)。这种激活可能触发全身性的应激反应(如释放去甲肾上腺素),而这些应激反应反过来又可能促进肿瘤生长和疼痛介质的释放,形成一个“疼痛-压力-肿瘤进展”的恶性循环。因此,有效管理癌痛可能不仅仅是缓解症状,也可能对控制肿瘤进展本身具有意义。
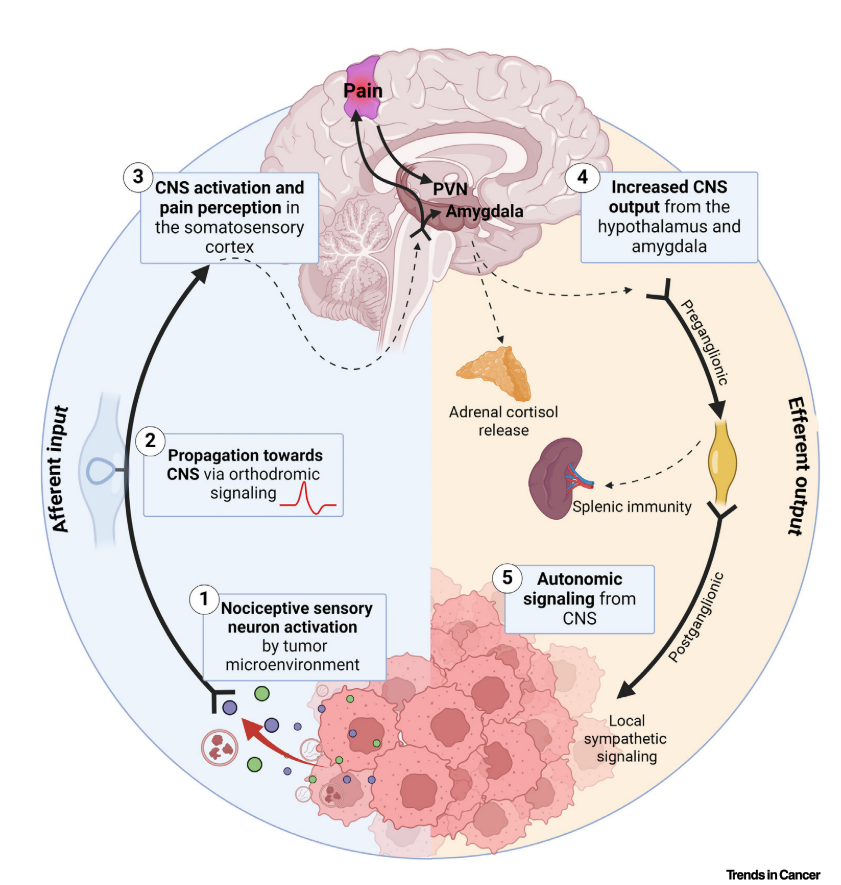
图3. 癌症中伤害性输入(疼痛)和自主神经输出之间的潜在循环
总结与展望
感觉神经在实体瘤的发生发展中扮演着远超疼痛传递本身的关键角色。它们通过释放CGRP等神经肽,深刻影响肿瘤微环境的免疫状态和癌细胞代谢,可能成为免疫逃逸的重要帮凶。靶向这些神经信号通路(如使用CGRP拮抗剂)不仅有望缓解癌痛,还可能成为一种增强抗肿瘤免疫、提高现有疗法(如免疫检查点抑制剂)效果的新型治疗策略。
未来的研究需要更深入地理解不同感觉神经亚型在不同实体瘤中的具体作用,并开发更精准的干预手段。了解这些复杂的生物学机制,有助于患者和医生更好地沟通治疗选择。如果您对最新的抗癌药物信息、靶向治疗方案或需要了解相关药物的海外购药渠道,可以查阅专业的抗癌资讯,或利用AI问诊服务获取初步解答。神经肿瘤学作为一个新兴领域,有望为癌症患者带来更有效的疼痛管理和抗癌治疗新希望。





