ADC药物:癌症治疗的“生物导弹”面临的挑战
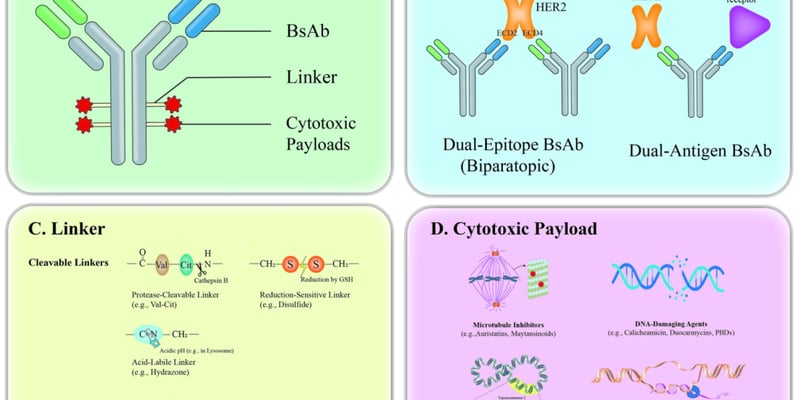
在抗癌药物的研发领域,抗体药物偶联物(ADC)无疑是近年来最耀眼的明星之一。这类药物被誉为“生物导弹”,能够精准地将高效化疗药物递送到癌细胞内部,从而在杀伤肿瘤的同时,最大限度地减少对健康组织的伤害。随着越来越多ADC药物获批上市,整个领域都充满了兴奋与期待。
然而,一个长期困扰着研究人员的难题是:为什么许多在临床前研究(如小鼠模型)中表现出巨大潜力的ADC分子,最终却在人体临床试验中遭遇失败?这不仅造成了巨大的研发资源浪费,也让许多满怀希望的患者失望。在近期举行的第16届世界抗体药物偶联物(ADC)峰会上,来自密歇根大学的化学工程学教授Greg Thurber博士就这一关键问题分享了他的见解。
关键突破:优化临床前给药剂量
Thurber博士指出,解决上述难题的一个关键在于优化临床前模型的给药剂量。他强调,如果在动物模型中使用的药物剂量能够接近于未来在人体临床试验中可耐受的剂量水平,那么这些临床前数据将能更准确地预测药物在患者身上的真实疗效。
“我们的研究传递出的核心信息是,当我们在临床前模型中使用了正确的、接近临床耐受剂量的药物时,其结果与我们在临床上观察到的一致性非常高。” Thurber博士解释道,“这可能成为未来筛选有潜力成功的候选药物的一个重要标志。”
这一发现为新药研发提供了一个更可靠的导航系统,有助于科学家们在早期阶段就筛选出最有可能成功的药物,从而加快新药上市的步伐。如果您想了解更多关于ADC药物或其他前沿抗癌疗法的信息,MedFind的AI问诊服务可以为您提供个性化的解答。
靶向递送:ADC药物疗效的核心驱动力
除了剂量问题,Thurber博士的团队还深入研究了ADC药物的多种作用机制。尽管存在一些非靶向的效应,如免疫效应、巨噬细胞摄取等,但研究最终明确了一点:靶向介导的药物摄取是决定ADC疗效的最主要驱动力。
这意味着,确保ADC药物能够精准识别并进入癌细胞(即“靶向递送”)的努力是完全值得的。这一核心机制的效力远远超过了其他任何次要效应。这一结论再次印证了精准靶向治疗在现代癌症治疗中的核心地位。
ADC领域的进步已经体现在了实际的临床应用中。例如,telisotuzumab vedotin-tllv(Emrelis)就是一款成功的ADC药物,已于2024年5月获得FDA批准,用于治疗携带c-MET蛋白高表达的晚期非小细胞肺癌(NSCLC)患者。寻找最新的抗癌药物可能是一个复杂的过程。MedFind致力于为患者提供全球药品代购渠道,确保您能及时获取所需治疗。
结语
总而言之,通过在临床前研究中模拟真实的临床给药条件,并持续专注于优化药物的靶向递送能力,科学家们可以更有效地将实验室中的 promising 成果转化为能够真正帮助患者的有效疗法。这不仅为ADC药物的未来发展指明了方向,也为广大癌症患者带来了更多治愈的希望。关注MedFind的抗癌资讯,我们将持续为您带来最新的药物研发和临床研究进展。