导言
肺腺癌(LUAD)作为最常见的肺癌类型,其治疗一直是医学界面临的重大挑战。尽管治疗手段不断进步,但肿瘤的进展和转移仍然是影响患者长期生存的主要障碍。因此,寻找能够有效抑制肺腺癌发展的新靶点和新策略,对于改善患者预后至关重要。近期,一项发表于国际顶尖期刊《Molecular Cancer》的研究为我们带来了新的希望。
最新研究揭示肺腺癌进展新机制
该研究系统地探讨了在肺腺癌的发病过程中,一种名为环状RNA(circRNA)的分子如何发挥作用。研究人员发现,在肺腺癌细胞中,一种特定的环状RNA分子——circRAPGEF5的表达水平显著升高。
更重要的是,这个分子的“活跃”与肿瘤的恶性行为密切相关。数据显示,高水平的circRAPGEF5会显著抑制细胞的“自噬”过程,从而促进癌细胞的增殖、迁移和侵袭,最终导致肿瘤的生长和转移。

解密信号通路:circRAPGEF5如何“助纣为虐”?
那么,circRAPGEF5究竟是如何在肺腺癌中发挥作用的呢?研究团队通过深入的分子机制探索,揭示了一条全新的信号传导通路:
- 关键分子互动: 首先,经过一种名为“m6A甲基化”修饰的circRAPGEF5会直接与一种m6A“阅读蛋白”IGF2BP2结合。
- 稳定下游目标: 这种结合会增强IGF2BP2的功能,使其能够稳定另一种名为NUP160的蛋白的信使RNA(mRNA),导致NUP160蛋白的产量增加。
- 抑制细胞自噬: NUP160蛋白的增多,最终会抑制细胞的自噬功能。自噬是细胞一种重要的“自我清理”和“循环利用”机制,能够清除受损的细胞器和蛋白质,维持细胞稳态。当自噬被抑制时,癌细胞内的“垃圾”无法被有效清除,反而为肿瘤的生存和发展创造了有利条件。
简单来说,这条circRAPGEF5/IGF2BP2/NUP160信号轴就像一个多米诺骨牌,最终通过抑制自噬这一关键环节,驱动了肺腺癌的进展和转移。
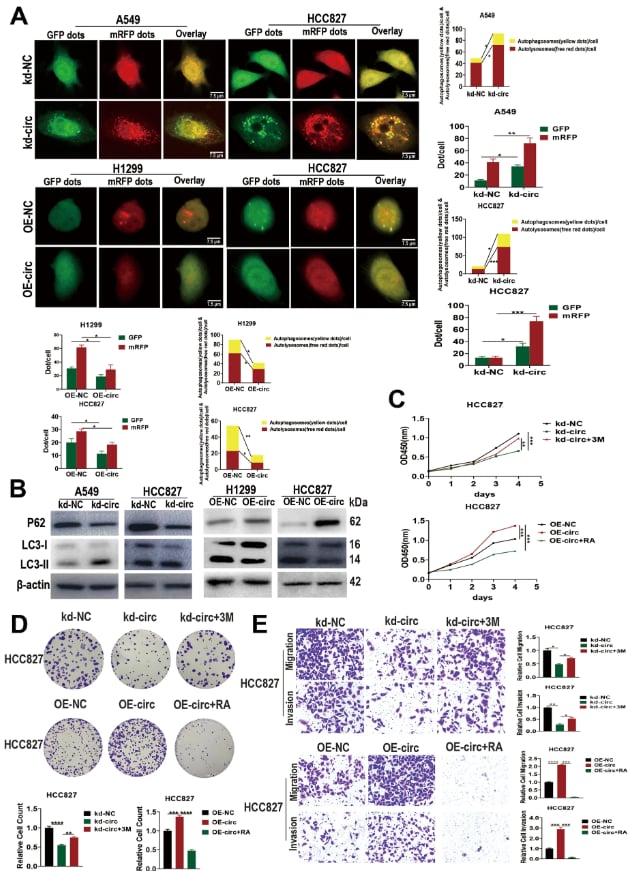
图解:circRAPGEF5/IGF2BP2/NUP160信号轴如何驱动肺腺癌进展
临床启示:肺腺癌治疗的潜在新靶点
这项研究的意义不仅在于揭示了一个新的生物学机制,更重要的是为肺腺癌的治疗提供了极具潜力的新靶点。研究人员在动物模型中也验证了这一发现:抑制circRAPGEF5/IGF2BP2/NUP160信号轴,可以有效地恢复细胞的自噬活性,从而显著减弱肺腺癌细胞的侵袭性,并抑制肿瘤的生长和转移。
这一发现为开发针对肺腺癌的全新治疗药物开辟了道路。未来,如果能设计出靶向这一信号通路中任何一个关键环节(如circRAPGEF5、IGF2BP2或NUP160)的药物,就有可能成为一种全新的、更精准的肺腺癌治疗策略,为那些面临肿瘤进展和转移困境的患者带来新的曙光。