在现代社会的高压环境中,心理压力已成为普遍现象。从日常工作到生活变故,从社交困扰到健康担忧,各种形式的心理压力无时无刻不在影响着我们的身心健康。然而,您是否曾想过,心理压力不仅会影响情绪,还可能在不知不觉中成为癌症发生和发展的“幕后推手”?
心理压力与胰腺癌:不容忽视的关联
近年来,越来越多的科学研究表明,心理压力与多种癌症的进展存在着密切的联系。尤其是在预后极差的胰腺导管腺癌(PDAC)中,心理压力的影响尤为显著。胰腺癌患者往往承受着巨大的生理和心理双重压力,而这些压力不仅会严重降低患者的生活质量,还可能加速疾病的恶化。然而,心理压力究竟是如何在分子层面影响PDAC的进展的呢?这一关键问题长期以来一直是癌症研究领域的焦点和难点。
突破性发现:揭示心理压力促进胰腺癌进展的分子机制
近期,一项发表在国际顶尖期刊《Nature Cell Biology》上的重磅研究,为我们揭示了心理压力与胰腺癌进展之间的分子奥秘。研究团队通过严谨的小鼠模型和细胞实验,首次阐明了心理压力如何通过影响肿瘤细胞中的RNA修饰,从而促进PDAC的进展。这一发现不仅填补了该领域的知识空白,也为开发新的胰腺癌治疗策略提供了重要的理论依据。
研究发现,当机体承受心理压力时,会激活交感神经系统,进而释放大量的去甲肾上腺素。这种神经递质的增加,会导致肿瘤细胞中一种关键的RNA去甲基化酶——ALKBH5的表达显著下降。ALKBH5的减少,使得RNA的N6-甲基腺苷(m6A)修饰异常增加。这些被异常修饰的RNA随后被包装进细胞外囊泡(EVs),并被传递给周围的神经元,从而增强肿瘤的神经支配,最终加速PDAC的恶性进展。

【研究核心发现】
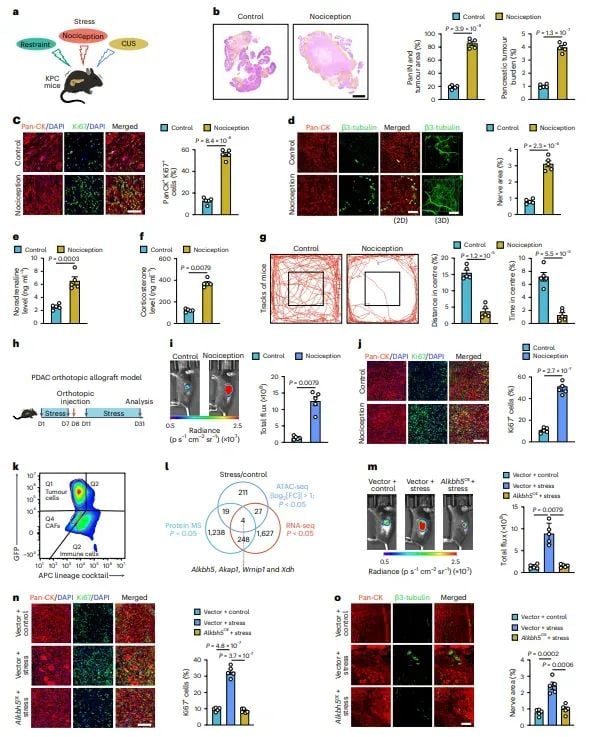
图1 心理压力通过降低Alkbh5表达促进PDAC进展
研究详细展示了心理压力(如束缚应激、慢性不可预测应激和疼痛诱导应激)在小鼠模型中如何显著促进胰腺导管腺癌(PDAC)的进展,具体表现为肿瘤负担增加、癌细胞增殖加快以及肿瘤神经支配的增强。核心机制在于心理压力激活交感神经释放去甲肾上腺素,导致肿瘤细胞中RNA去甲基化酶ALKBH5表达下降,进而影响RNA的m6A修饰,最终促进肿瘤神经支配和PDAC进展。值得注意的是,实验证实过表达ALKBH5能够有效抑制肿瘤生长、细胞增殖和神经支配,并显著延长小鼠的生存时间。
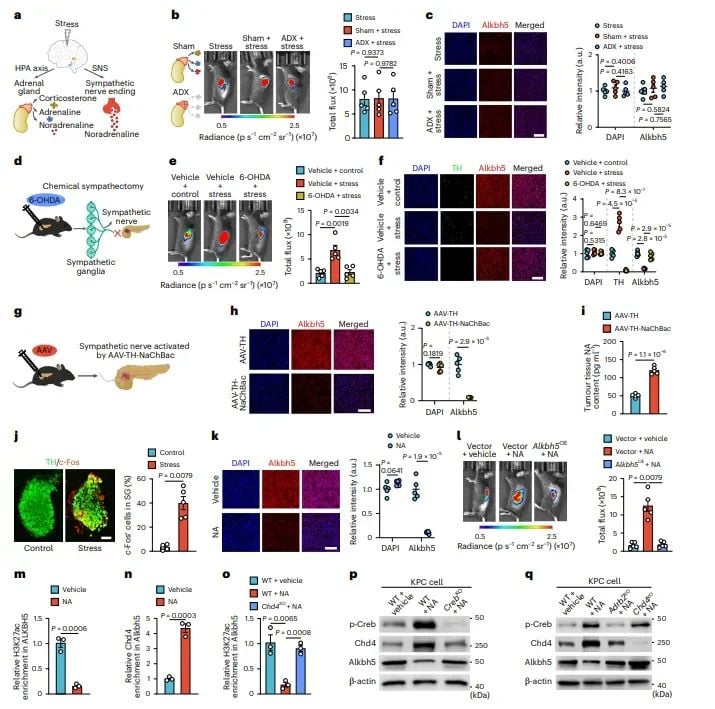
图2 去甲肾上腺素通过ADRB2-p-CREB-CHD4轴降低Alkbh5表达
进一步的机制研究揭示,去甲肾上腺素通过激活β2肾上腺素受体(ADRB2)及其下游的p-CREB-CHD4信号通路,导致ALKBH5表达下降。通过化学交感神经切除或激活交感神经等实验手段,研究人员证实了交感神经在心理压力诱导的ALKBH5表达下降中的关键作用。此外,研究还发现CHD4的结合位点在ALKBH5启动子区域富集,且CHD4的敲除能够恢复ALKBH5的正常表达。
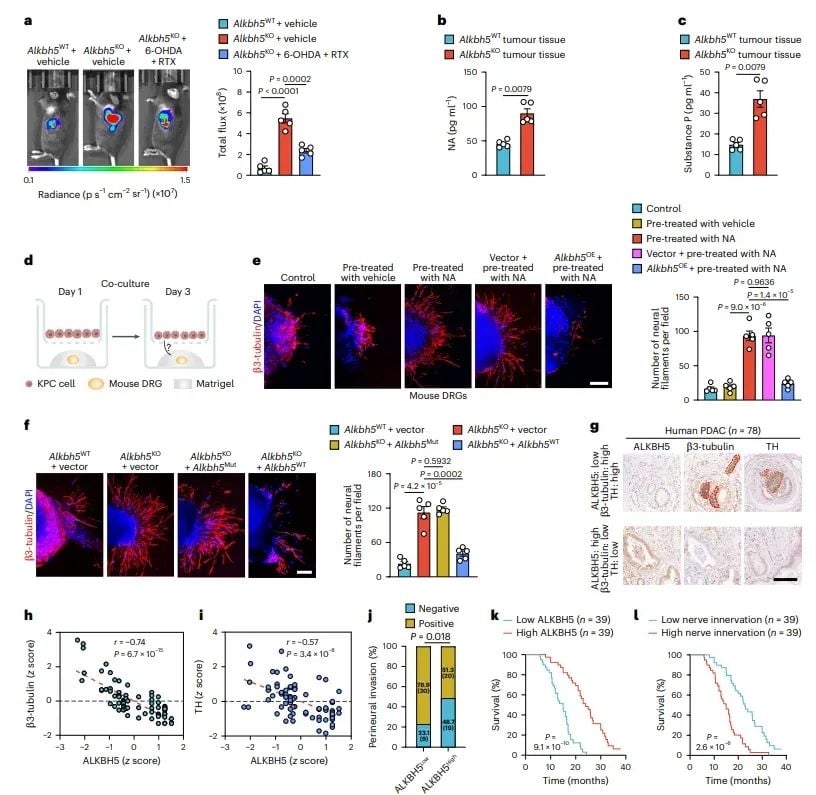
图3 Alkbh5缺陷通过EVs中的m6A修饰RNA增强神经支配
研究深入探讨了ALKBH5缺陷如何通过影响细胞外囊泡(EVs)中的m6A修饰RNA来促进神经支配和PDAC进展。结果显示,ALKBH5缺陷的PDAC细胞产生的EVs含有更多m6A修饰的RNA。当这些EVs被神经元摄取后,显著增强了神经支配。令人振奋的是,通过化学神经切除或使用天然黄酮类化合物fisetin抑制EVs的摄取,可以显著抑制神经支配和肿瘤进展,从而延长小鼠的生存时间。
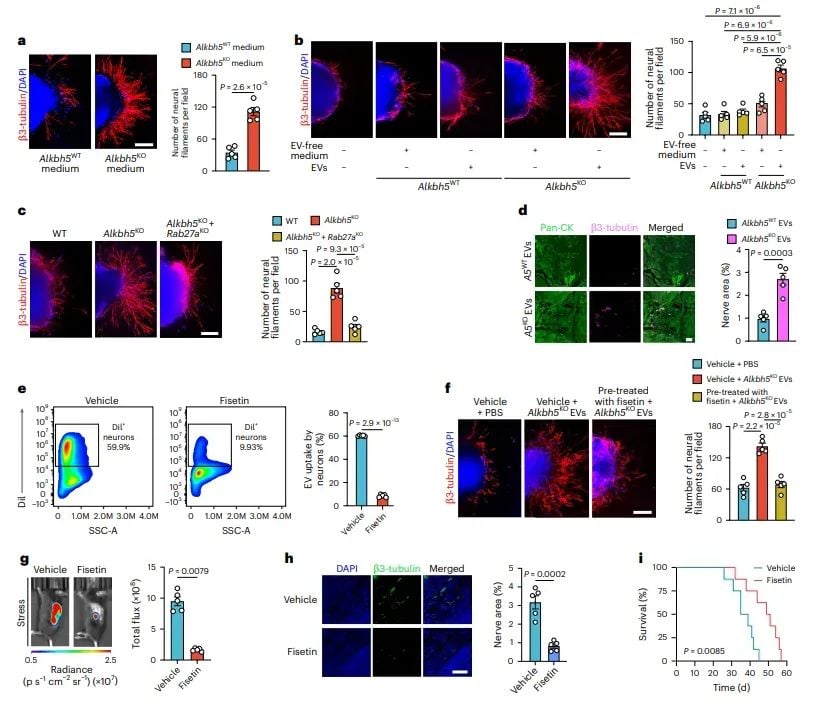
图4 EVs中的m6A修饰RNA通过海绵作用促进神经支配
进一步的机制研究揭示,EVs中的m6A修饰RNA通过“海绵作用”吸附miRNA,从而促进神经支配。研究发现,m6A修饰的EV RNA能够显著促进神经元的轴突生成,而这种作用正是通过miRNA海绵机制实现的。例如,特定的EV RNA转录本3能够吸附miR-155-5p,从而解除其对Bdnf mRNA的抑制,进而促进神经支配。此外,fisetin通过抑制EVs的摄取,显著抑制了这种神经支配的增强作用。
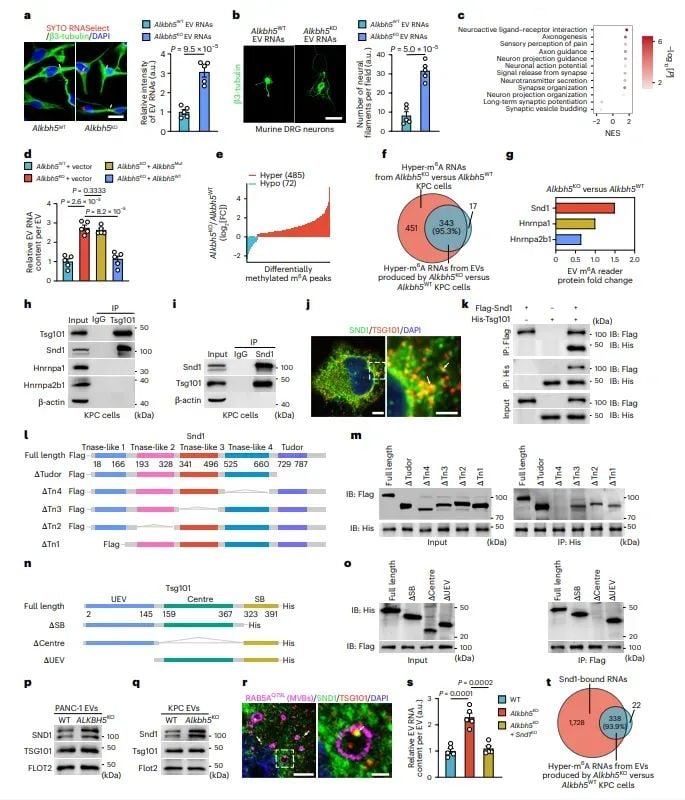
图5 SND1与TSG101相互作用将m6A修饰RNA运输到EVs中
研究还深入揭示了SND1与TSG101之间的相互作用如何将m6A修饰的RNA运输到细胞外囊泡(EVs)中。实验证实,SND1能够与TSG101相互作用,并将其结合的m6A修饰RNA运输到EVs中。通过免疫共沉淀和免疫荧光实验,研究人员证实了SND1与TSG101的相互作用,并且发现SND1的TNase-like 4结构域和TSG101的中心区域是它们相互作用的关键区域。此外,SND1的敲除显著减少了EVs中的RNA含量,抑制了神经支配的增强。
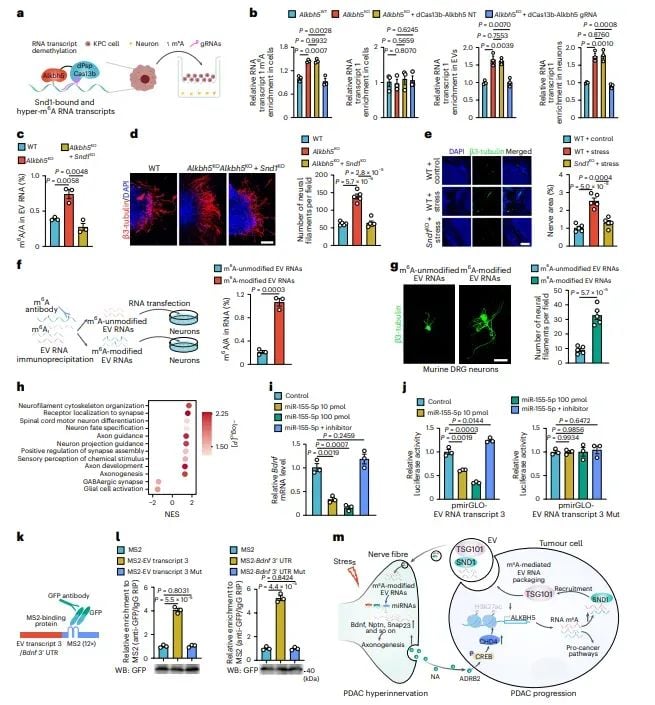
图6 m6A修饰的EV RNA通过海绵作用促进神经支配
最后,研究人员总结了m6A修饰的EV RNA如何通过海绵作用吸附miRNA,从而促进神经支配。研究发现,m6A修饰的EV RNA能够显著促进神经元的轴突生成,而这种作用可以通过miRNA海绵机制实现。例如,EV RNA转录本3能够吸附miR-155-5p,从而解除其对Bdnf mRNA的抑制,进而促进神经支配。此外,通过MS2-RIP实验,证实了miR-155-5p与EV RNA转录本3和Bdnf mRNA 3’UTR的相互作用。
潜在的治疗新策略:天然化合物Fisetin
这项研究的另一个重要发现是,天然黄酮类化合物fisetin(非瑟酮)能够有效阻止神经元摄取这些携带m6A修饰RNA的细胞外囊泡,从而抑制PDAC的神经支配和肿瘤进展。这一发现为胰腺癌的治疗提供了新的潜在策略,预示着未来可能通过干预心理压力诱导的分子通路,或者利用类似fisetin的化合物,来改善胰腺癌患者的预后。
面对癌症,我们能做什么?
这项研究再次强调了身心健康在癌症防治中的重要性。对于胰腺癌患者而言,除了积极配合临床治疗,管理心理压力也应成为治疗方案中不可或缺的一部分。同时,随着癌症研究的不断深入,新的靶向药和抗癌药层出不穷,为患者带来了更多希望。
面对复杂的癌症治疗和不断更新的靶向药信息,患者往往感到迷茫。MedFind致力于为全球癌症患者提供专业的海外靶向药代购服务,确保您能及时获取所需的抗癌药物,包括各类仿制药和创新药。同时,我们还提供AI问诊服务,帮助您更好地理解病情和治疗方案,并提供丰富的药物信息与诊疗指南,助您在抗癌路上少走弯路,获取最前沿的治疗信息和支持。





