近日,日本大鹏药品(Taiho Pharmaceutical)和其子公司Taiho Oncology宣布,FDA已加速批准其产品Lytgobi(Futibatinib)上市,用于治疗携带FGFR2基因融合或其它重排的不可切除、局部晚期或转移性肝内胆管癌经治成人患者。这是自2020年以来,FDA批准的第四款治疗肝内胆管癌的新药,也是针对FGFR2异常的第3款靶向药。
肝内胆管癌(Intrahepatic Cholangiocarcinoma,ICC),是指发源于左右肝管汇合部以上胆管的恶性肿瘤,是原发性肝癌的类型之一,占全部原发性肝癌病例仅为10%~15%。然而,肝内胆管癌的发病率正在不断上升,且致死率高。根据相关数据显示,2018年全球有8.4万~12.6万人新诊断为ICC,我国肝内胆管癌的发病人数约为全球的一半左右。2008-2012年年龄标准化发病率约0.63/10万人,并以每年约11%的速度增长。此外,由于起病隐匿,侵袭性极强,手术切除和化疗是目前主要的治疗手段,但抗癌措施效果比较差,患者平均生存期不超过一年。
FGFR2、IDH1靶向治疗已取得重大突破
根据统计数据显示,肝内胆管癌的常见突变类型包括FGFR,IDH1,IDH2,BRAF等,近年来,FGFR2和IDH1这两种突变亚型的治疗取得了显著的突破,开启了肝内胆管癌靶向药物研发的新赛道。
截至目前,除了刚刚获批的Futibatinib,FDA还批准了2款靶向FGFR2和1款靶向IDH1的新药。据有关数据显示,FGFR2基因融合见于13%~17%肝内胆管癌患者中,IDH1突变发生在约20%的肝内胆管癌中,均是肝内胆管癌非常重要的治疗靶点。
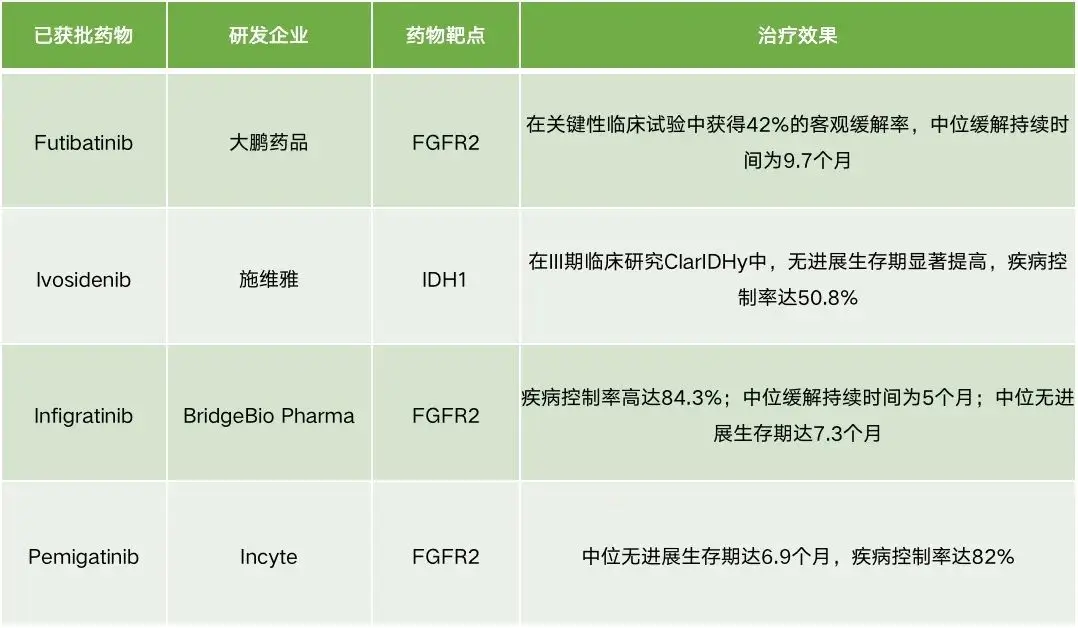
▲表 1 截至目前共获批4款ICC治疗新药 资料来源:作者整理
肝内胆管癌治疗未来可期
除了FGFR2和IDH1两大靶点外,未来还有哪些值得期待的治疗靶点和在研新药?
作者通过Clinical Trial、药物临床试验登记与信息公示平台,对肝内胆管癌在研新药进行梳理,FGFR靶向药仍是药企的研究重点,和记黄埔、北京天诚、Basilea Pharmaceutica等药企均所有布局。
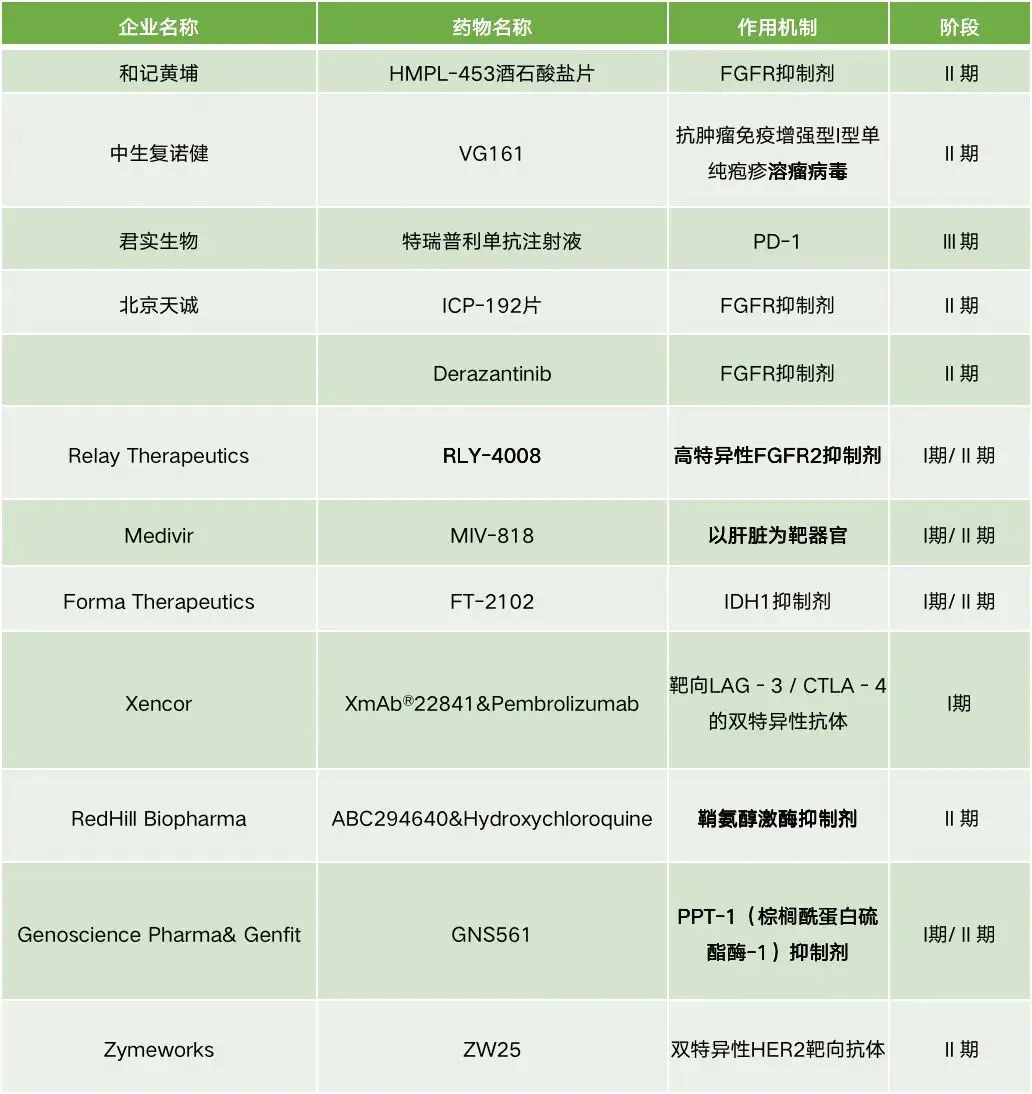
▲表 2 全球肝内胆管癌在研新药情况梳理 资料来源:Clinical Trial,药物临床试验登记与信息公示平台,作者整理
2.1 新型FGFR抑制剂
Relay公司在研新药RLY-4008是一种高特异性FGFR2口服抑制剂。抑制FGFR2活性的小分子通常也会抑制FGFR1和FGFR家族其它成员的活性,这种脱靶效应在临床应用中带来很多毒副作用,Relay公司的专有技术平台通过对蛋白构象的动态平衡进行详细分析,开发出FGFR2特异性抑制剂RLY-4008。相较于其他FGFR抑制剂,RLY-4008在癌细胞系中表现出FGFR2依赖性的抗癌活性,在缩小肿瘤同时,对其他靶标(包括FGFR家族的其他蛋白)影响极小,具有良好的抗脱靶特性。
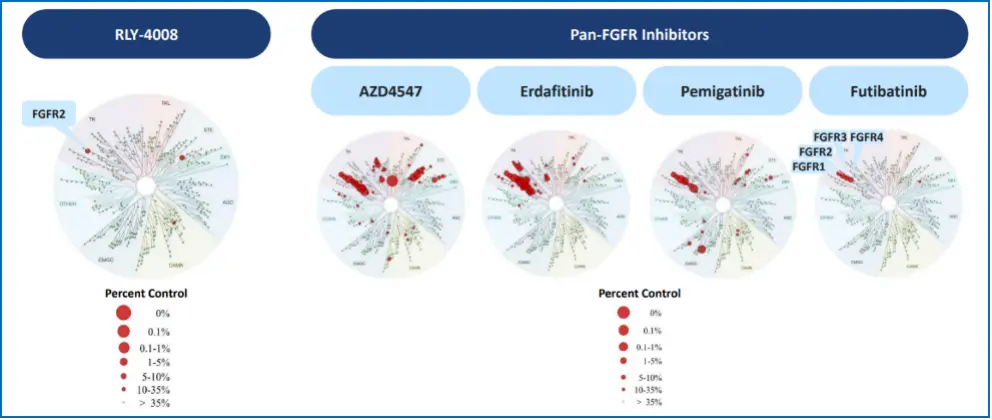
▲图 1 RLY-4008具有非常高的FGFR2特异性 资料来源:Relay Company Presentation 2022
2.2 以毒攻毒,免疫疗法得力助手溶瘤病毒值得关注
目前,国药集团中国生物所属中生复诺健生物科技(上海)有限公司研发的一类创新药VG161正处于临床Ⅱ期,用于治疗晚期肝内胆管癌。VG161是一款溶瘤病毒产品,溶瘤病毒是肿瘤免疫治疗手段之一,溶瘤病毒是天然的或经人工改造的能选择性在肿瘤组织中复制,从而杀伤肿瘤细胞,但对正常组织无杀伤作用的一类病毒。除直接杀伤肿瘤细胞外,溶瘤病毒可参与到抗肿瘤免疫的多个阶段中,发挥其抗肿瘤活性,溶瘤病毒可以诱导强力的免疫应答,增强机体的抗肿瘤反应。
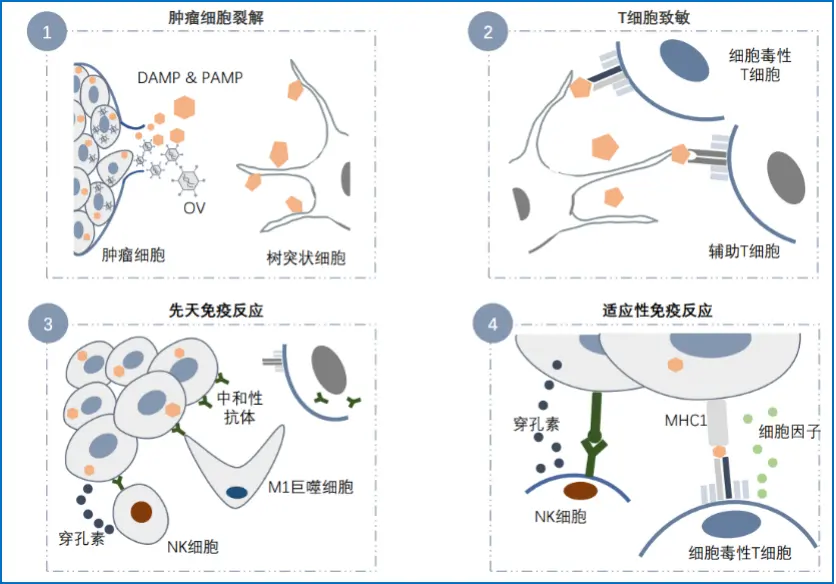
▲图 2 溶瘤病毒原理 资料来源:沙利文
VG161同时携带IL12、IL15/15RA(IL15和IL15受体α亚基)和PD-L1阻断肽(PDL1B)的基因。VG161通过瘤内注射进入肿瘤组织,病毒在肿瘤细胞内复制和溶解肿瘤细胞的同时,携带的4个免疫刺激因子均被有效表达,实现了溶瘤活性与免疫刺激的协同。同时,病毒所表达的4个免疫刺激因子之间也发生进一步的协同增效,从而把抗病毒免疫反应转化为特异性的抗肿瘤免疫反应。自2015年全球首款产品获批至今,已有四款溶瘤病毒产品获FDA批准上市,适应症涉及黑色素瘤、头颈部肿瘤、神经胶质瘤”(其中两款产品的适应症同为黑色素瘤),这标志着对溶瘤病毒的技术成熟度和对其治疗癌症的认可。目前,溶瘤病毒技术主要被用于治疗难治性实体瘤,除了肝内胆管癌,未来溶瘤病毒或将为胰腺癌、胶质母细胞瘤等恶性肿瘤患者带来治疗新希望。
2.3 新靶点涌现:PPT1,Sk2,HER2…
今年9月,Genoscience Pharma公司在研新药GNS561获FDA授予的孤儿药资格,用于治疗肝内胆管癌。在晚期肝内胆管癌中,自噬会在肿瘤细胞中被激活从而加速肿瘤发展。而孤儿药GNS561是一种PPT-1(棕榈酰蛋白硫酯酶-1)抑制剂,通过与PPT1相互作用抑制晚期自噬和扩大溶酶体的剂量依赖性积聚,从而阻断癌细胞增值。根据GNS561的I期临床研究数据显示,在经过GNS561治疗一个月后,恶性肝组织中的PPT1表达减少。GNS561的有效性将在未来的临床试验中有待进一步验证,目前来看,GNS561是一个极具潜力的候选药物。
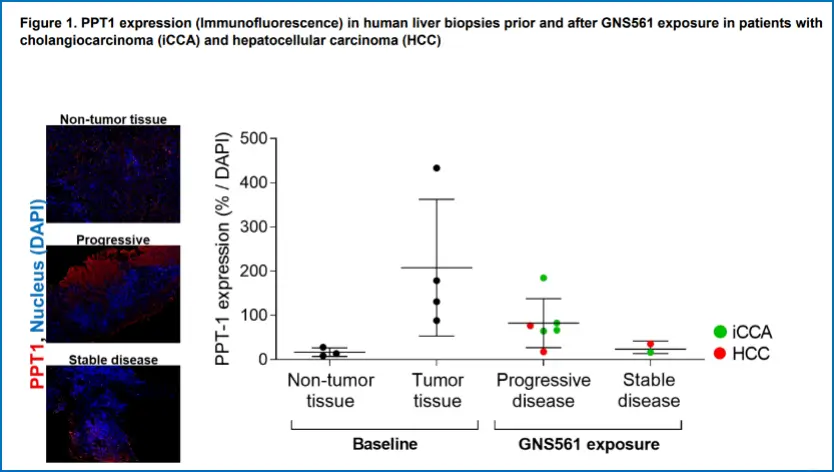
▲图 3 PPT-1表达情况 资料来源:First-In-Human Effects of PPT1 Inhibition Using the Oral Treatment with GNS561/Ezurpimtrostat in Patients with Primary and Secondary Liver Cancers
ABC294640是一款鞘氨醇激酶2(Sphk-2)抑制剂。Sphk可以将具有促凋亡作用的鞘氨醇(Sphingosine,Sph)代谢为具有促进增殖作用的1-磷酸鞘氨醇(Sphingosine-1-phosphate,S1P)。研究发现,Sphk在很多肿瘤中过表达,并且具有促进肿瘤发生发展的作用,是肿瘤治疗的新靶点。Sphk有两种异构体,即Sphk1和Sphk2,Sphk2在胆管癌细胞中的表达较高。ABC294640是一种新型的Sphk2小分子抑制剂,具有特异性强、口服吸收性好、副作用小等优点,目前已经进入Ⅱ期临床试验。
ZW25(Zanidatamab)是一种双特异性HER2靶向抗体。2020年11月,ZW25获得FDA的突破疗法认定。在2021 ASCOGI会议上公布了该药的I期临床数据,研究纳入的21名胆道癌患者的客观缓解率为40%,疾病控制率为65%,中位缓解持续时间为7.4个月。
结语
肝内胆管癌存在巨大的临床未满足需求,由于在肝内胆管癌中具有较高检出率,FGFR2相关药物被寄予了厚望,近年来取得重大突破,发展飞速。未来,还有更多的机制研究、靶点将被挖掘,为肝内胆管癌患者的治疗带来希望。此外,作者认为,目前肝内胆管癌的检测手段非常有限,目前的检测方式均存在痛点。穿刺不适合术前患者和早期诊断,影像学检查存在误诊或漏诊的风险,肿瘤标志物诊断性能差等问题,伴随着肝内胆管癌机制研究的深入,不仅仅是治疗环节的飞跃,更有望开发出具有明确病理机制的诊断产品,届时,肝内胆管癌诊断—治疗产业链也将被重塑。
【参考资料】
1.Clinical Trial,药物临床试验登记与信息公示平台
2.《治疗胆管癌,创新精准疗法获FDA加速批准》,药明康德,2022年10月
3.《肝内胆管细胞癌的诊治现状及进展》,《国际外科学杂志》,2020年第6期
4.《群雄逐鹿!2021年胆管癌靶向治疗,潜在靶点开启新胆管癌靶向药物新赛道》,六日行研社,2021年
5.《2021 ASCO GI | 肝癌、胆管癌领域重磅研究盘点》,医脉通,2021年
6.《中国生物首个溶瘤病毒产品VG161获得临床试验批件》,生物制品圈,2020年
7.《中国溶瘤病毒产业发展白皮书》,沙利文,2021年
8.《溶瘤病毒3.0,复诺健半年吸金超1.4亿美元,首款产品已进临床》,健康界,2021年
9.Harding JJ, Awada A, Roth G, etal. First-In-Human Effects of PPT1
Inhibition Using the Oral Treatment with GNS561/Ezurpimtrostat in Patients with
Primary and Secondary Liver Cancers. Liver Cancer. 2022 Feb
15;11(3):268-277.
10.《精准治疗胆管癌,高特异性FGFR2抑制剂初步临床结果积极》,药明康德,2021年

![转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析 6 转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析](https://medfind.link/wp-content/uploads/2026/05/b5eabf912ca30af172ff43ee330147e8.jpg)