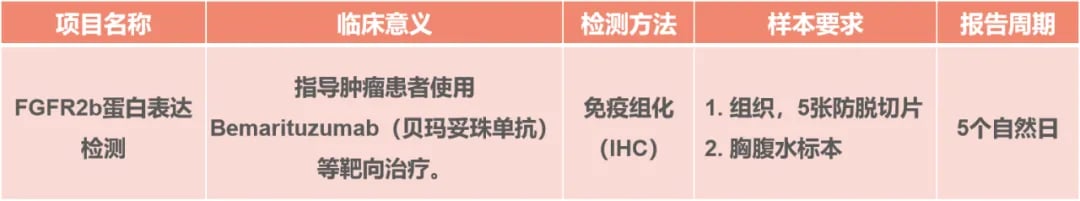
FGFR2b阳性胃癌治疗新希望
对于FGFR2b过表达的晚期或转移性胃癌及胃食管结合部癌(G/GEJC)患者而言,一线治疗选择有限且效果不尽人意。FGFR2b过表达与肿瘤的侵袭性强、预后差密切相关。在这一背景下,靶向FGFR2b的首创单克隆抗体贝玛妥珠单抗(Bemarituzumab, BEMA)应运而生,为这类患者带来了新的治疗希望。近期公布的III期临床试验FORTITUDE-101的最新数据,为我们揭示了贝玛妥珠单抗联合化疗的真实疗效与挑战。更多关于胃癌的前沿资讯,请关注MedFind抗癌资讯板块。

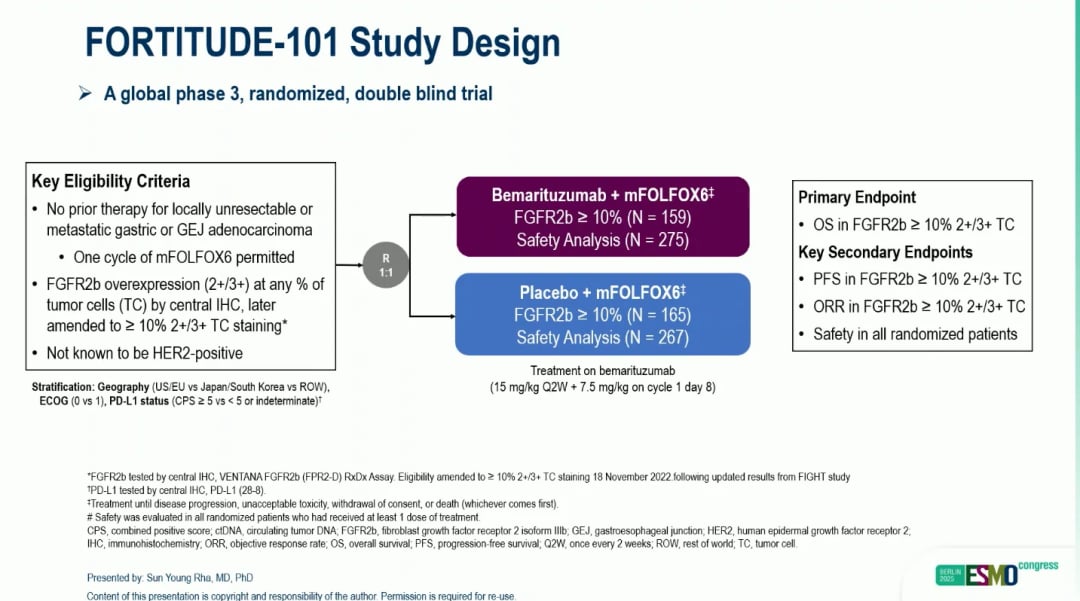
FORTITUDE-101研究设计概览
FORTITUDE-101是一项全球性的III期临床研究,旨在评估在标准化疗方案mFOLFOX6的基础上,加入贝玛妥珠单抗能否为FGFR2b过表达(定义为≥10%的肿瘤细胞表达)、HER2阴性的晚期G/GEJC患者带来生存获益。研究共纳入547名患者,随机分为两组:
- 试验组:贝玛妥珠单抗联合mFOLFOX6化疗
- 对照组:安慰剂联合mFOLFOX6化疗
研究的主要终点是总生存期(OS),关键次要终点包括无进展生存期(PFS)和客观缓解率(ORR)。
关键研究结果:生存获益的动态变化
该研究的结果呈现出一个值得关注的动态变化过程,从初期的显著获益到长期随访的获益减弱。
1. 中期分析:令人鼓舞的初步数据
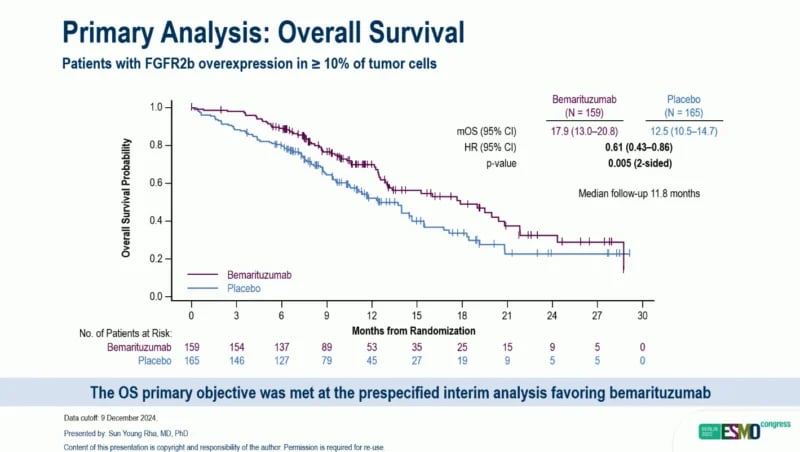
在2024年12月进行的中期分析中(中位随访11.8个月),结果显示出统计学和临床上的双重显著改善:
- 总生存期(OS):贝玛妥珠单抗组的中位OS达到了17.9个月,而安慰剂组仅为12.5个月,死亡风险显著降低了39%(HR=0.61, P=0.005)。
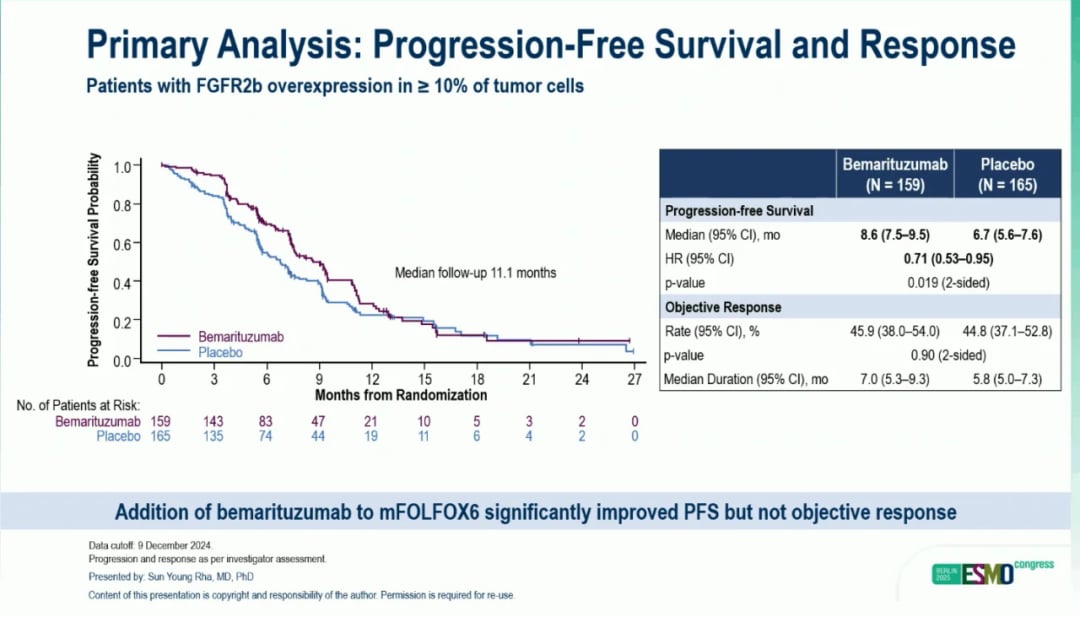
- 无进展生存期(PFS):贝玛妥珠单抗组的中位PFS为8.6个月,优于安慰剂组的6.7个月(HR=0.71, P=0.019)。
这一初步结果无疑是振奋人心的,表明早期介入贝玛妥珠单抗能为患者带来明确的生存优势。
2. 最终分析:长期疗效有所减弱
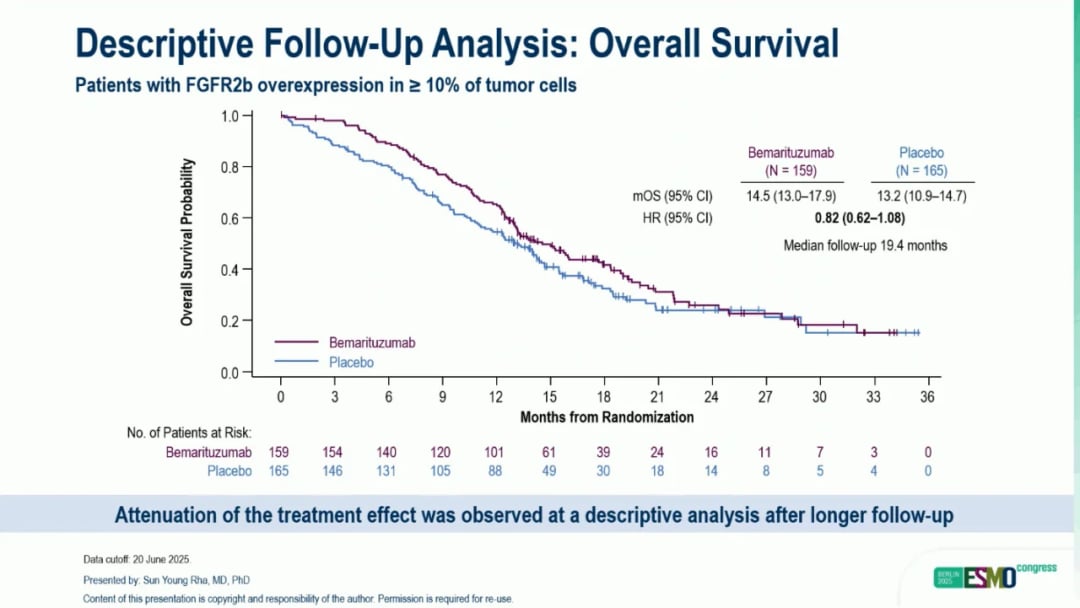
然而,在2025年6月更新的随访数据中(中位随访19.4个月),此前观察到的生存获益幅度有所收窄:
- 总生存期(OS):贝玛妥珠单抗组的中位OS为14.5个月,而安慰剂组为13.2个月(HR=0.82)。尽管仍观察到获益趋势,但已不再具有统计学显著性。
这种获益随时间减弱的现象可能与后续治疗、疾病进展等多种复杂因素有关,提示了在临床应用中需要更深入地理解其长期效果。对于复杂的治疗选择,患者可以寻求专业意见,例如通过MedFind的AI问诊服务获取初步参考。
安全性与副作用分析
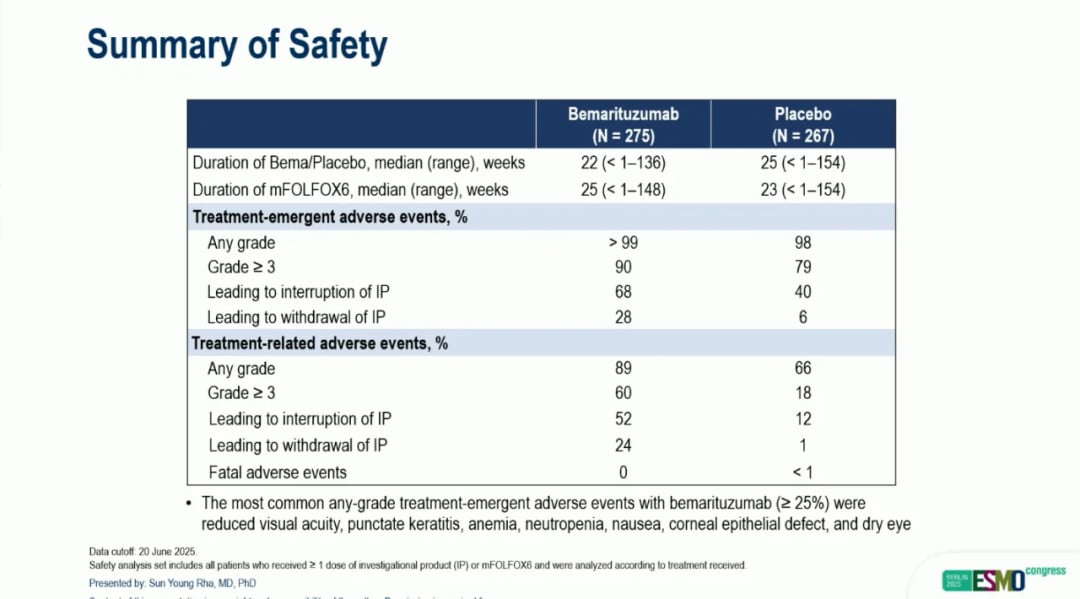
贝玛妥珠单抗的安全性是临床应用的关键考量。研究显示,其副作用谱是可预测且总体可控的。最常见的不良事件主要集中在眼部毒性,包括:
- 视力下降(33%)
- 点状角膜炎(26%)
- 角膜上皮缺损(14%)
值得庆幸的是,这些眼部不良事件大多是可逆的。数据显示,90%的3级或更高级别的角膜不良事件可缓解至1级或以下。虽然角膜事件的消退时间较长(中位17周),但视力恢复相对较快(中位8周)。这表明通过积极的眼科管理,可以有效控制贝玛妥珠单抗的眼部副作用,保障患者的治疗依从性和生活质量。
研究结论与未来展望
FORTITUDE-101试验成功验证了FGFR2b是胃癌和胃食管结合部癌中一个重要的、可行的治疗靶点。尽管长期随访中总生存期的获益幅度有所减弱,但研究初期和无进展生存期的显著改善,仍然证实了贝玛妥珠单抗联合化疗在一线治疗中的临床价值。该药物的安全性特征,特别是可逆的眼部毒性,也为其未来的临床应用奠定了基础。作为首个靶向FGFR2b的抗体药物,贝玛妥珠单抗有望改变FGFR2b过表达胃癌患者的治疗格局。如果您想了解更多关于胃癌靶向治疗药物的最新信息,包括药物价格和购买渠道,可以访问MedFind全球靶向药代购平台。