在癌症治疗领域,评估新疗法(尤其是靶向药和免疫治疗)的有效性至关重要。临床试验使用一系列“终点指标”来衡量治疗效果,这些指标直接影响着药物审批和医生的治疗决策。对于患者而言,理解这些指标如OS、PFS、ORR等,有助于更清晰地认识治疗方案的潜在获益。本文将依据NMPA和FDA等权威机构的审评标准,为您系统梳理十大关键临床终点指标及其在抗癌药选择中的价值。
一、核心临床终点指标详解与权重分析
1. 总生存期 (Overall Survival, OS):评估疗效的“金标准”
定义:指从患者随机接受治疗开始,到因任何原因导致死亡为止的时间长度。
决策价值:OS是衡量治疗是否能延长患者生命的最终指标,具有最高决策权重。然而,评估OS需要大规模研究和长期随访,且结果可能受到后续治疗(如换药)的影响。
实例:某款靶向药物若能将晚期肺癌患者的中位OS延长数月,这通常是其获得批准上市的关键证据。
2. 无进展生存期 (Progression-Free Survival, PFS):衡量疾病控制的关键指标
定义:指从治疗开始,到影像学等检查确认肿瘤发生进展或患者因任何原因死亡为止的时间。
决策价值:PFS常作为OS的替代指标,能更快地反映药物抑制肿瘤生长的能力,尤其在需要加速审批的情况下非常重要。但需要注意,PFS的改善并不总能转化为OS的延长。
应用:在某些癌症的二线或后线治疗中,PFS的显著改善(例如中位数延长数月)常被用作支持药物有条件批准的依据。
3. 客观缓解率 (Objective Response Rate, ORR):反映肿瘤缩小的“快照”
定义:指肿瘤体积缩小达到预设标准(如RECIST 1.1)且维持一定时间(通常至少4周)的患者比例,包括完全缓解(CR)和部分缓解(PR)。
决策价值:ORR在评估药物的直接抗肿瘤活性方面很有价值,尤其是在早期临床试验或单臂试验中。但高ORR不一定意味着长期生存获益,需结合缓解持续时间(DOR)来看。
注意:某些免疫治疗可能出现“假性进展”后才缓解,评估时需特别注意。
4. 无病生存期 (Disease-Free Survival, DFS):衡量根治性治疗后复发风险
定义:主要用于评估手术或放疗等根治性治疗后的辅助治疗效果,指从根治性治疗完成开始,到疾病复发或患者因任何原因死亡为止的时间。
决策价值:在辅助治疗场景(如早期乳腺癌的内分泌治疗或靶向治疗)中,DFS的延长意味着降低了复发风险,通常预示着更好的长期生存。
意义:DFS的改善是评估辅助治疗方案价值的重要依据。
5. 完全缓解率 (Complete Response Rate, CR):追求“治愈”的目标
定义:指所有可见的肿瘤病灶完全消失,且无新病灶出现,并维持至少4周。
决策价值:CR是最佳的治疗反应,尤其在血液肿瘤(如白血病)的治疗中意义重大。在实体瘤中,CR率通常较低,但仍是衡量深度缓解的重要指标。
展望:随着联合治疗策略的发展,提高实体瘤的CR率是重要的研究方向。
6. 免疫治疗客观缓解率 (iORR):适应免疫疗法特点的评估
定义:基于特殊的免疫相关反应评价标准(如irRC或iRECIST)评估的ORR,旨在更准确地捕捉免疫治疗独特的反应模式(如延迟反应、假性进展)。
决策价值:在评估PD-1/PD-L1抑制剂等免疫治疗药物时,iORR被认为能更好地反映其临床获益,并与OS有较好的相关性。
趋势:随着免疫治疗应用的普及,iORR及其评估标准日益重要。
7. 疾病控制率 (Disease Control Rate, DCR):衡量病情稳定的指标
定义:指肿瘤缩小(CR+PR)加上肿瘤稳定(Stable Disease, SD)的患者比例。
决策价值:DCR反映了治疗能使多少患者的病情得到控制(包括缩小和稳定)。虽然权重相对较低,但在某些情况下(如维持治疗)仍有参考价值。
应用:对于一些生长缓慢的肿瘤或晚期患者,维持疾病稳定也是重要的治疗目标。
8. 缓解持续时间 (Duration of Response, DOR):评估疗效持久性
定义:指从首次确认肿瘤缓解(CR或PR)开始,到首次确认疾病进展或患者因任何原因死亡为止的时间长度。
决策价值:DOR是ORR的重要补充,反映了治疗效果能维持多久。长DOR意味着患者能从治疗中获得更持久的获益。例如,某些靶向药如奥希替尼(Osimertinib)在特定肺癌患者中展现了较长的DOR。
评估:DOR通常与ORR结合分析,全面评估药物的缓解效果。
9. 至进展时间 (Time To Progression, TTP):排除死亡因素的进展指标
定义:指从治疗开始到影像学确认肿瘤进展的时间,与PFS不同的是,TTP不将死亡作为事件终点。
决策价值:TTP主要用于评估药物延缓肿瘤生长的纯粹效果,在非肿瘤死亡风险较高的患者群体(如老年患者)中有一定应用价值,但整体权重较低。
10. 患者报告结局 (Patient-Reported Outcome, PRO):关注生活质量
定义:通过标准化问卷(如EORTC QLQ-C30)由患者直接报告的健康状况、症状(如疼痛、疲劳)和生活质量。
决策价值:PRO越来越受到重视,因为它直接反映了治疗对患者主观感受的影响。改善生活质量是癌症治疗的重要目标之一。FDA已批准过基于PRO数据改善卵巢癌患者生活质量的药物,如奥拉帕利(Olaparib)。
意义:良好的PRO数据可以增强患者对治疗的信心和依从性。
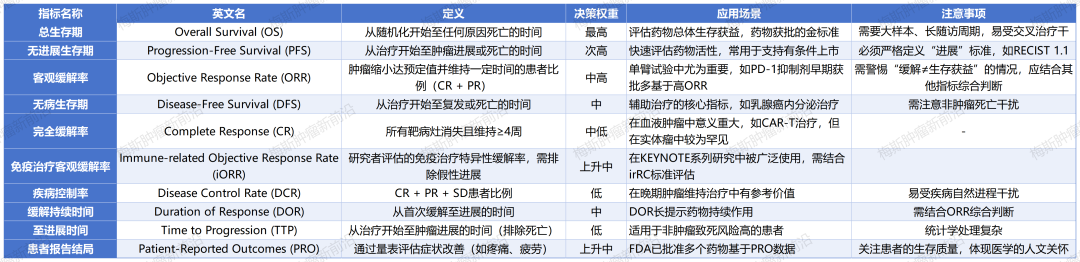
二、终点选择的决策逻辑与审评考量
监管机构(如NMPA和FDA)在审批新抗癌药时,会根据治疗线数、药物类型和临床需求紧急程度来权衡不同的终点指标:
1. 分层决策:
- 一线治疗:通常要求提供OS数据,以证明相比标准疗法有明确的生存优势。
- 后线治疗:可接受PFS或ORR作为主要终点,尤其是在缺乏有效治疗手段的领域。
- 突破性疗法/孤儿药:对于满足重大未满足医疗需求的药物,有时会基于令人信服的ORR和DOR数据给予加速批准或有条件批准,如DS-8201(Trastuzumab deruxtecan)的早期获批。
2. 证据要求:
- 确证性临床试验通常需要OS或高质量的PFS数据。
- 若使用PFS/ORR作为替代终点,需要证明其与OS存在良好的相关性。
3. 审评灵活性:
- 监管机构在审评中会体现一定的灵活性,综合考虑疗效、安全性、患者生活质量(PRO)以及临床需求的迫切性。
了解这些临床终点指标,有助于患者及其家属更深入地理解医生推荐的治疗方案以及新药的临床试验结果。当考虑不同的治疗选择,包括靶向药、免疫治疗或其仿制药时,这些数据是评估潜在获益和风险的重要依据。如果您在获取特定抗癌药(如海外新药或仿制药)方面遇到困难,或想了解更多关于靶向药代购的信息和价格,可以关注相关可靠渠道。对于复杂的病情和治疗选择,利用AI问诊服务进行初步咨询或查阅抗癌资讯获取更多专业信息,或许能为您提供有价值的参考。
参考文献
国家药品监督管理局. 《抗肿瘤药物临床试验技术指导原则》. 2022.
Eisenhauer EA, et al. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1). Eur J Cancer. 2009.
FDA. Guidance for Industry: Patient-Reported Outcome Measures. 2023.
中国临床肿瘤学会. 《肿瘤免疫治疗疗效评价标准》. 2024.
Nature Reviews Clinical Oncology. “Evolving landscape of clinical endpoints in oncology”. 2025.