CD70:淋巴瘤靶向治疗的新兴希望与挑战
对于淋巴瘤患者及其家属而言,寻找高效、精准的治疗方案是抗癌过程中的核心目标。随着靶向治疗的飞速发展,越来越多的分子靶点被发现并应用于临床。其中,CD70作为肿瘤坏死因子(TNF)超家族的重要成员,因其在多种血液系统恶性肿瘤(特别是淋巴瘤)中高表达,且与免疫逃逸、疾病进展和不良预后密切相关,被视为一个极具前景的治疗靶点。
然而,要成功实施CD70靶向治疗,前提是必须精准识别出CD70阳性的患者,并了解其全身病灶的CD70表达情况。传统的检测方法存在诸多限制,难以满足精准医疗的需求。近日,上海交通大学医学院附属仁济医院血液科刘婷婷教授和核医学科魏伟军教授团队在核医学权威期刊《Journal of Nuclear Medicine》上发表了一项突破性研究,证实了基于单域抗体(sdAb)的CD70免疫PET/CT显像方法,能够实现对淋巴瘤患者CD70表达的非侵入性、全身性评估,为未来的CD70靶向治疗提供了强大的影像学支持。
这项研究不仅为淋巴瘤的精准诊断和治疗筛选提供了新的工具,也为患者了解最新的药物信息、治疗方案解读、临床研究与指南资讯开辟了新的途径。
什么是CD70?为何成为重要靶点?
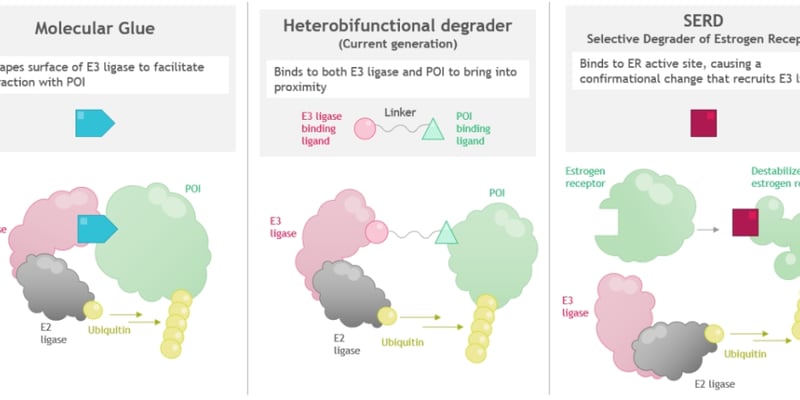
CD70(Cluster of Differentiation 70)是一种跨膜蛋白,通常在活化的T细胞和B细胞上短暂表达。但在许多血液系统恶性肿瘤,如弥漫性大B细胞淋巴瘤(DLBCL)、霍奇金淋巴瘤、多发性骨髓瘤等中,CD70会持续且高水平表达。CD70与配体CD27结合后,会促进肿瘤细胞的增殖、存活,并帮助肿瘤细胞逃避免疫系统的监视(即免疫逃逸)。因此,针对CD70的靶向药物,如抗体药物偶联物(ADC)或双特异性抗体,被设计用于特异性杀伤表达CD70的肿瘤细胞。
传统CD70检测的局限性
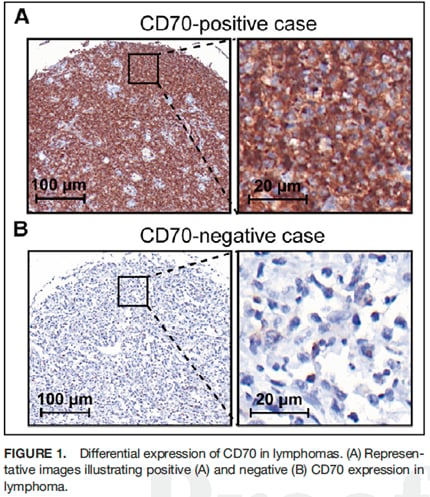
目前,临床上评估CD70表达主要依赖于免疫组化(IHC)检测,即通过活检获取肿瘤组织样本,在显微镜下观察CD70蛋白的表达情况。尽管IHC是金标准,但它存在以下几个关键局限性:
- 取样局限性(Sampling Bias):IHC只能检测活检部位的CD70表达。由于淋巴瘤往往是多灶性的,且不同病灶之间、甚至同一病灶内部都可能存在CD70表达的异质性(即表达水平不一致),单次活检的结果可能无法代表全身肿瘤的真实情况。
- 无法动态监测:IHC是一种侵入性操作,无法频繁重复进行,因此难以用于治疗过程中CD70表达的动态变化监测。
- 无法反映全身异质性:如果患者体内存在多个病灶,且只有部分病灶表达CD70,IHC无法提供全身性的“地图”,这对于需要全身性治疗的淋巴瘤来说是巨大的挑战。
为了克服这些挑战,研究人员迫切需要一种非侵入性、全身性、可重复的影像学方法来精准评估CD70的表达,从而指导靶向药物的使用。
上海仁济医院的突破性研究:CD70免疫PET/CT技术解析
仁济医院团队开发并验证的CD70免疫PET/CT技术,正是为了解决上述局限性而诞生的。该技术利用了一种新型的示踪剂——[¹⁸F]RCCB6,它是一种基于单域抗体(sdAb)的放射性药物。
[¹⁸F]RCCB6示踪剂的工作原理
单域抗体(sdAb),也被称为纳米抗体,具有体积小、穿透性强、清除快的特点。这些特性使其成为PET显像示踪剂的理想载体。[¹⁸F]RCCB6示踪剂通过特异性结合肿瘤细胞表面的CD70抗原,并利用PET/CT的成像能力,将CD70高表达的病灶“点亮”。
与传统的[¹⁸F]FDG(氟代脱氧葡萄糖)PET/CT主要反映肿瘤细胞的代谢活性不同,CD70免疫PET/CT直接反映的是肿瘤细胞表面的分子靶点表达水平,这是一种更具特异性的分子影像技术。
研究设计与患者群体
该研究首先对154例弥漫性大B细胞淋巴瘤(DLBCL)患者的样本进行了CD70 IHC染色分析,以确定CD70的表达模式。随后,20例经活检证实的淋巴瘤患者(入组前瞻性临床试验NCT06852638)接受了CD70免疫PET/CT显像。
研究的核心目标包括:
- 评估[¹⁸F]RCCB6示踪剂在人体内的生物分布和安全性。
- 比较CD70免疫PET/CT与标准[¹⁸F]FDG PET/CT的诊断效能。
- 分析示踪剂摄取水平(通过SUVmax衡量)与CD70 IHC表达(通过H-score衡量)的相关性。
- 评估CD70免疫PET/CT在治疗反应监测中的潜力。

核心研究结果解读:CD70免疫PET/CT的临床价值
淋巴瘤亚型的CD70表达模式
在154例DLBCL样本中,研究发现CD70阳性率高达63.0%(97/154),其中近一半(48.5%)为高表达。这证实了CD70在DLBCL中作为靶点的广泛适用性。
研究还发现,CD70的表达具有显著的异质性:
- 年龄相关性:CD70表达与患者年龄呈正相关趋势,老年患者的表达水平更高。
- 亚型差异:不同淋巴瘤亚型对示踪剂的摄取水平差异显著。最高的是DLBCL(中位SUVmax 4.4)和粘膜相关淋巴组织淋巴瘤(4.6)。较低的是滤泡性淋巴瘤(2.1)、小淋巴细胞淋巴瘤(2.5)。最低的是霍奇金淋巴瘤(1.3)和NK/T细胞淋巴瘤(1.1)。
影像学诊断效能:全身性、高精准度
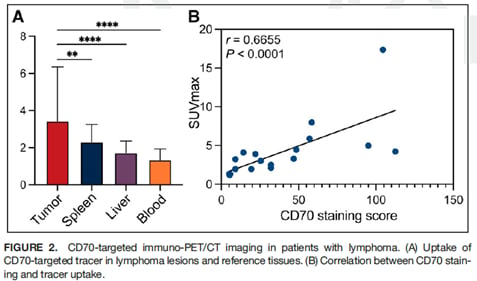
CD70免疫PET/CT在诊断性能上表现出色:
- 背景清晰:示踪剂在肾外正常组织(如肝、脾、血液)的摄取极低,使得病灶与背景之间的对比度高,影像清晰。
- 高检出率:淋巴结病灶的检出率达到98.3%(177/180),结外病灶检出率达到100.0%(9/9),假阴性率极低。
- 与IHC高度相关:病灶的示踪剂最大标准摄取值(SUVmax,衡量PET信号强度的指标)与CD70 IHC染色H-score呈显著正相关(r=0.6655,P<0.0001)。这意味着PET/CT的信号强度能够准确地反映肿瘤组织中CD70蛋白的真实表达水平。
相比传统FDG-PET/CT的独特优势
在总体诊断性能上,CD70免疫PET/CT与临床常用的[¹⁸F]FDG PET/CT相当。然而,CD70靶向显像在特定临床场景中展现出不可替代的特异性优势,这对于淋巴瘤患者的治疗决策至关重要。
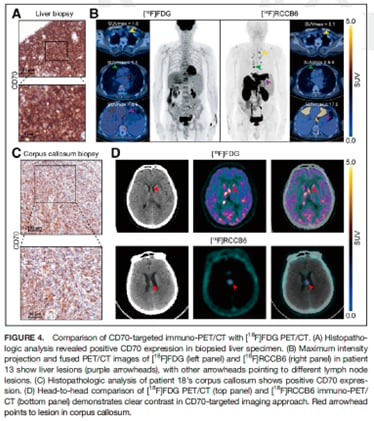
克服脑组织高背景干扰
传统的[¹⁸F]FDG PET/CT在检测颅内病灶时面临巨大挑战。这是因为大脑组织对葡萄糖的生理性摄取极高(即FDG信号强),导致颅内肿瘤病灶(如胼胝体DLBCL)的信号被高背景信号掩盖,难以清晰显示。而[¹⁸F]RCCB6示踪剂在脑实质本底摄取极低,因此CD70靶向显像能够更清晰、准确地显示颅内病灶,这对于中枢神经系统淋巴瘤的诊断和分期具有重大临床意义。
揭示病灶间的异质性
CD70免疫PET/CT能够直观地反映全身病灶之间CD70表达的差异(异质性)。例如,患者的上纵隔淋巴结可能表现出高摄取(CD70高表达),而下纵隔淋巴结可能表现出低摄取(CD70低表达)。这种全身性的“CD70表达地图”是传统单点活检无法提供的。
了解这种异质性,对于指导靶向治疗至关重要。如果患者接受CD70靶向药物治疗,医生可以预判哪些病灶可能对治疗敏感,哪些病灶可能需要结合其他治疗手段,从而优化个体化治疗方案。
CD70免疫PET/CT在个体化治疗中的应用前景
CD70免疫PET/CT技术的成功验证,预示着淋巴瘤个体化诊疗将迈入一个更精准的时代。这项技术有望在以下几个方面发挥核心作用:
治疗前筛选:精准定位阳性患者
对于即将接受CD70靶向药物(如某些正在研发中的ADC药物)治疗的患者,CD70免疫PET/CT可以作为一种非侵入性的筛选工具。它能快速、准确地确定患者是否为CD70阳性,并评估全身病灶的表达水平,确保靶向药物用在最可能受益的患者身上,避免不必要的治疗和副作用。
治疗中监测:早期评估药物疗效
研究结果显示,治疗(化疗)后,病灶的CD70靶向示踪剂摄取显著下降(SUVmax从3.4 ± 1.4降至1.1 ± 0.5,P=0.001)。更重要的是,在某些案例中,示踪剂摄取的快速下降甚至可以在病灶形态学变化(CT上可见的肿瘤大小变化)之前监测到治疗反应。
这种早期、分子水平的疗效监测能力,使得医生能够更迅速地判断治疗方案是否有效,从而及时调整策略,避免患者在无效治疗上浪费时间和资源。患者和家属可以通过AI 辅助问诊服务,结合影像学报告,更深入地理解治疗进展和下一步的治疗选择。
展望:未来CD70靶向药物与诊断的结合
随着医学研究的不断深入,针对CD70的靶向药物正在全球范围内积极开发中。例如,Vadastuximab talirine(SGN-CD70A)等药物曾被用于治疗急性髓系白血病(AML)和非霍奇金淋巴瘤,尽管其临床开发过程充满挑战,但针对CD70的创新疗法从未停止。未来,CD70免疫PET/CT技术将成为这些靶向药物的“伴随诊断”工具,确保药物的精准应用。
对于需要获取海外前沿抗癌药物的患者,了解最新的诊断技术和治疗方案至关重要。MedFind致力于提供抗癌药品代购与国际直邮服务,帮助患者及时获得所需的创新疗法,包括未来可能上市的CD70靶向药物。
总结与患者启示
上海仁济医院团队的这项研究,成功验证了CD70免疫PET/CT显像技术在淋巴瘤中的巨大潜力。它克服了传统IHC检测的局限性,实现了对CD70表达的全身性、非侵入性、高精准度评估。尤其是在检测颅内病灶和揭示病灶异质性方面,该技术展现出优于传统FDG-PET/CT的特异性优势。
对于淋巴瘤患者而言,这项技术意味着:
- 更精准的靶向治疗选择:如果未来有CD70靶向药物上市,这项技术能帮助医生准确判断您是否适合该疗法。
- 更早期的疗效评估:治疗过程中,能够更早地知道治疗是否有效,从而避免无效治疗的延误。
- 更全面的疾病评估:尤其对于中枢神经系统受累风险高的患者,提供了更可靠的诊断工具。
尽管这项技术仍需要在更大样本量的研究中进一步验证和推广,但它无疑是淋巴瘤个体化诊疗领域向前迈出的重要一步,为患者带来了新的希望。