近年来,癌症治疗的进展日新月异,尤其是在精准医疗领域,通过深入了解肿瘤的基因组特性,为患者找到更有效的个性化治疗方案成为可能。对于罕见癌症,如肛门鳞状细胞癌(aSCC),由于其发病率相对较低,相关研究和治疗选择一直有限。然而,一项迄今为止规模最大的aSCC基因组研究,为这种疾病带来了新的希望。这项研究不仅全面描绘了aSCC的分子图谱,更重要的是,它首次大规模证实了液体活检(Liquid Biopsy)在指导aSCC靶向治疗方面的可行性与卓越价值。
肛门鳞状细胞癌:一种被忽视的“HPV相关癌症”
肛门鳞状细胞癌(aSCC)是一种罕见但发病率和死亡率呈上升趋势的恶性肿瘤,它占所有消化道癌症的比例不足3%。根据全球预测,到2030年,肛门癌的新发病例可能达到65500例,死亡病例将达到26900例,这凸显了对aSCC治疗研究的紧迫性。
这种癌症最显著的特点是其与人乳头瘤病毒(HPV)感染的高度相关性,高达80%–85%的aSCC病例是由HPV感染驱动的,其中HPV-16型和HPV-18型最为常见。尽管HPV疫苗已经问世,但由于全球疫苗接种计划的推进缓慢、公众对疫苗接种建议的依从性不高,以及男性人群疫苗接种覆盖率极低(2019年仅为4%),HPV疫苗对aSCC发病率的影响仍然有限。
目前,放化疗是aSCC的主要治疗手段,但仍有10%–40%的患者会出现复发。对于复发患者,仅约20%适合接受挽救性治疗,其余患者则需要接受针对转移性疾病的全身治疗。不幸的是,约10%–20%的患者在初诊时就已是转移性疾病,或后续发生远处转移,这些患者的预后往往较差,5年生存率仅为36%。
长期以来,姑息性化疗一直是转移性aSCC的主要治疗选择,但其证据级别有限。近年来,随着医学的进步,一些新的治疗方案也开始崭露头角。例如,紫杉醇-卡铂方案已在一项2期临床试验中被确立为局部晚期或转移性aSCC的标准一线治疗方案。此外,免疫检查点抑制剂(ICIs)联合化疗作为一线治疗也取得了令人鼓舞的结果,但其总生存期(OS)数据仍在等待公布。在二线治疗中,尽管治疗选择有限,但对于一线治疗未使用过ICIs的患者,指南推荐可考虑使用该类药物。然而,在实际临床中,这些创新药物的可及性在许多情况下仍然受限,使得患者面临巨大挑战。
在这样的背景下,深入探究aSCC的基因组特征,寻找潜在的靶向治疗和免疫治疗生物标志物,开发更个体化的治疗策略,成为了刻不容缓的需求。
基因组“寻宝图”:揭示aSCC深层秘密
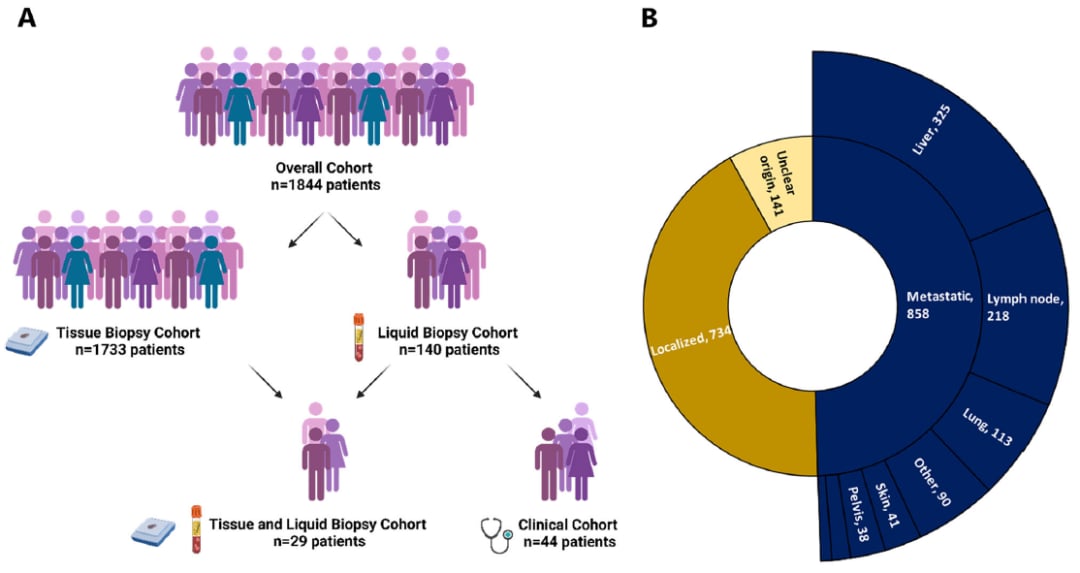
为了更好地理解aSCC的分子基础并寻找新的治疗靶点,一项迄今为止最大规模的aSCC基因组研究应运而生。该研究纳入了来自美国和法国的1844例患者,对他们的组织活检和/或液体活检样本进行了基因组谱分析。这项研究不仅规模空前,更采用了先进的FoundationOne®CDx或FoundationOne® Liquid CDx检测技术,这些技术能够全面覆盖约324个与实体瘤相关的基因,为深入解析aSCC的分子特征奠定了坚实基础。
最大规模研究概览
这项回顾性分析共纳入1844例经组织学证实的aSCC患者,其中1733例接受了组织样本基因谱分析,140例接受了液体样本基因谱分析,29例同时接受了两种检测。研究发现,在绝大多数(86.6%)的病例中检测到了HPV感染,其中HPV-16型最为常见,占75.6%。
研究还发现,17.1%的患者存在高肿瘤突变负荷(TMB-H,≥10 mut/Mb),这预示着一部分患者可能对免疫检查点抑制剂治疗有更好的反应。然而,微卫星不稳定性(MSI)的发生率较低,仅为1.7%。这些数据为aSCC的精准治疗提供了重要的生物标志物信息。
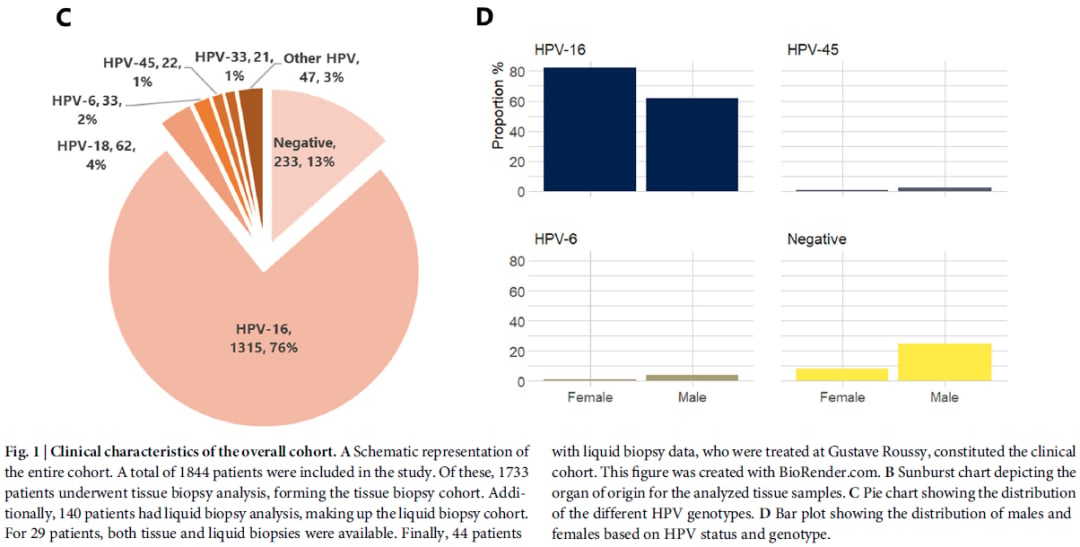
关键基因突变与染色体变异
研究深入分析了aSCC患者的基因组图谱,发现了一些反复出现的基因突变和染色体变异,这些变异可能是aSCC发生发展中的关键驱动因素,也是潜在的治疗靶点:
- PIK3CA:这是aSCC中最常见的突变基因,突变率高达34.5%。其中,第10外显子的E545K和E542K突变,以及PIK3CA基因扩增是主要的变异形式。PIK3CA是PI3K/AKT/mTOR信号通路的关键成员,该通路在细胞生长、增殖和存活中发挥核心作用,其异常激活常与肿瘤的发生发展密切相关。
- KMT2D和EP300:这些是表观遗传修饰基因,突变率分别为18.0%和7.2%。表观遗传修饰在基因表达调控中扮演重要角色,其异常可能导致肿瘤的发生。
- 抑癌基因:包括PTEN(13.1%)、FBXW7(12.9%)、TP53(12.0%)和CDKN2A(6.9%)。这些基因的失活(如纯合缺失)是肿瘤发展中的常见事件,它们通常负责抑制细胞生长和分裂,或修复DNA损伤。一旦这些基因失去功能,肿瘤细胞便可能失控生长。
- TERT启动子区:端粒酶逆转录酶(TERT)启动子区变异的发生率为7.3%,这与肿瘤细胞的“永生化”能力有关。
- 染色体变异:最常见的染色体臂扩增是3q(67.2%),该区域包含了PIK3CA和SOX2等重要基因。最常见的缺失是11q染色体臂(49.6%),以及包含TP53基因的17p染色体臂(21.3%)。
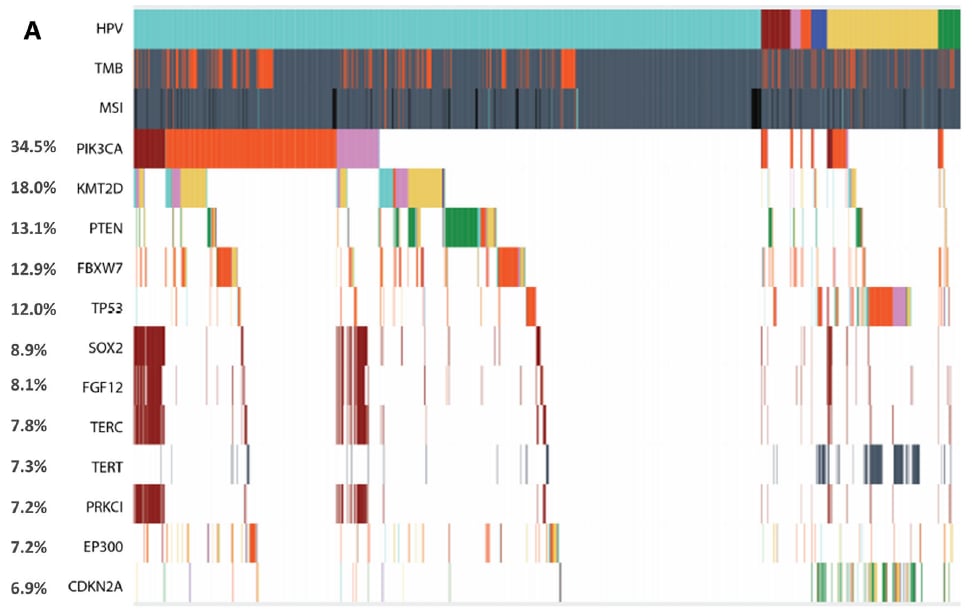
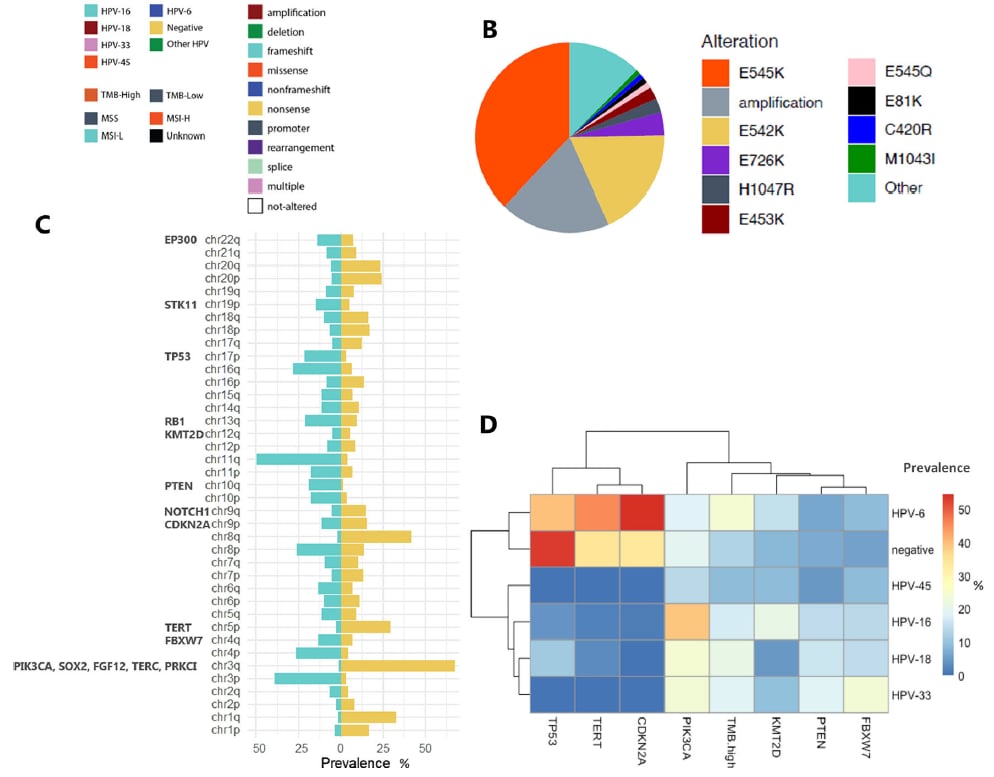

值得注意的是,不同HPV亚型与基因突变模式存在显著差异。例如,HPV阴性病例和低危型HPV-6阳性病例中,TP53、TERT启动子区和CDKN2A的变异更为常见;而最常见的HPV-16型病例中,PIK3CA突变率较高。这提示我们,针对不同HPV状态的aSCC,可能需要采取不同的精准治疗策略。
潜在“可干预靶点”浮出水面
除了上述常见的基因突变,研究还发现了其他一些具有潜在靶向治疗价值的变异,尽管单个基因的突变率可能低于10%,但它们合计在aSCC患者中占有相当比例,为未来的精准治疗提供了更多可能性。
- 受体酪氨酸激酶(RTKs):包括FGFR3(3.6%)、FGFR2(0.5%)和EGFR(2.5%)基因的变异。这些受体在细胞信号传导中起关键作用,其异常激活常常导致肿瘤的生长和转移。例如,FGFR3的S249C突变,可以促进受体的活化,而针对FGFR的抑制剂已在其他癌症中显示出良好疗效。
- MAPK信号通路相关基因:如KRAS(2.4%)、NRAS(0.7%)和BRAF(1.0%)。MAPK通路是细胞内重要的信号传导通路,参与细胞的增殖、分化和凋亡。这些基因的突变(如KRAS G12D、BRAF V600E)是多种癌症的常见驱动因素,目前已有针对这些靶点的药物上市或在研发中。
- DNA修复相关基因:如BRCA1(3.1%)和BRCA2(2.6%)。这些基因在DNA损伤修复中扮演重要角色,其致病性变异会导致DNA修复缺陷,使肿瘤细胞对PARP抑制剂等药物更敏感。
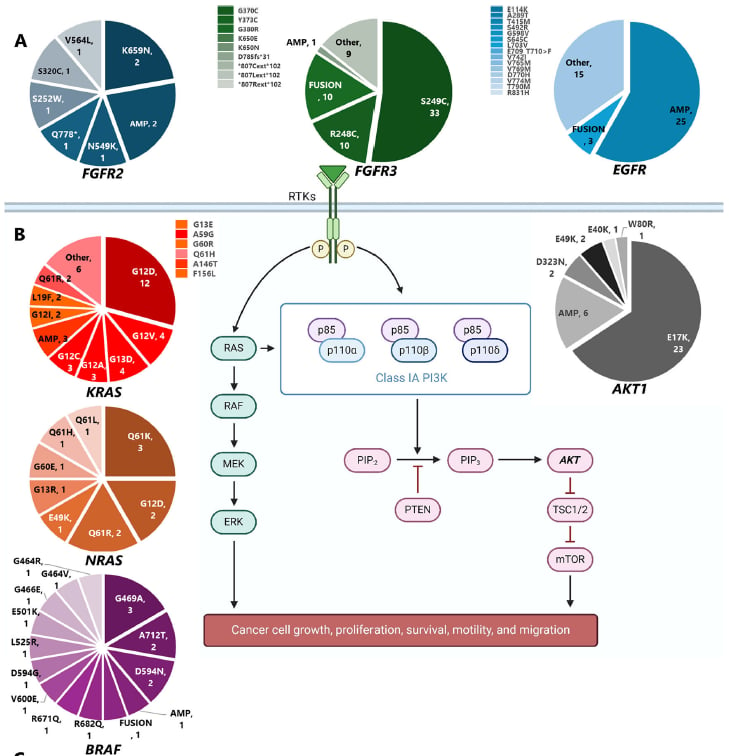
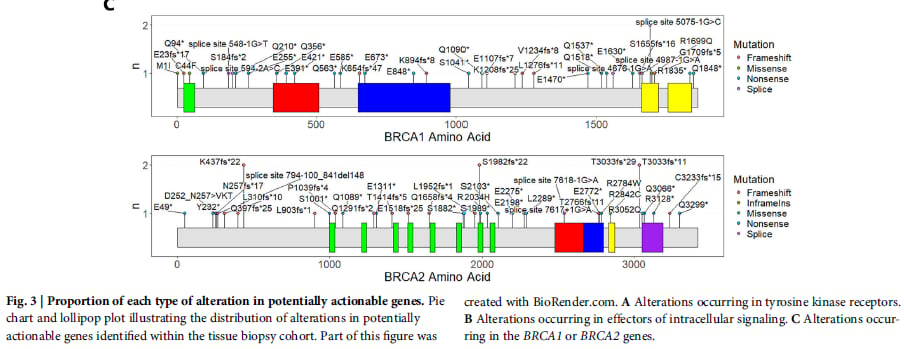
为了评估这些分子变异的临床可干预性,研究采用了改良的ESCAT和OncoKB分类系统。这些系统根据变异在不同癌症类型中的临床证据和治疗反应,将其分为不同级别,以指导临床医生为患者选择最合适的治疗方案。研究发现,近20%的变异属于ESCAT 1C类,这意味着无论肿瘤起源如何,基于篮式试验证据,针对这些变异的临床抑制都应被视为标准治疗,这为aSCC患者带来了实实在在的治疗希望。
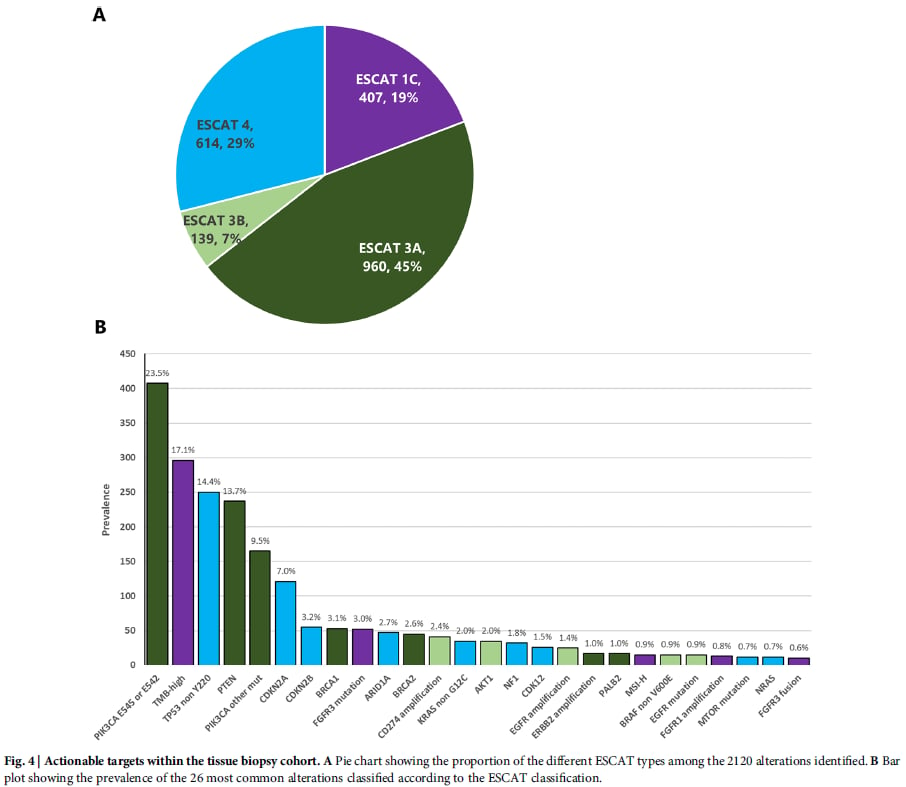
“无创精准导航”:液体活检的革命性价值
传统的肿瘤基因组检测主要依赖于组织活检,但组织活检具有侵入性、操作复杂、且有时难以获取足够样本的局限性。而液体活检(Liquid Biopsy),通过检测血液中的循环肿瘤DNA(ctDNA)来获取肿瘤基因信息,因其微创、便捷、可重复取样等优势,在精准医疗领域备受关注。
液体活检与组织活检的高度一致性
这项aSCC研究最重要的发现之一是,液体活检在检测基因组变异、可干预靶点和HPV感染状态方面,与组织活检的结果显示出高度一致性。这意味着,通过简单的抽血,医生就可以获得与肿瘤组织样本同样可靠的基因组信息,从而指导治疗决策。
具体来说,液体样本中PIK3CA的突变率(35.0%)与组织样本(34.5%)非常接近,FBXW7的突变率也高度一致。虽然液体活检中TP53、KMT2D和PTEN的突变率略高,这可能与液体活检对亚克隆突变的检测灵敏度更高,以及TP53参与克隆性造血有关(克隆性造血是指与年龄相关的造血干细胞克隆扩增,这些克隆可能获得体细胞突变,并可在ctDNA中被检测到,但并非都来源于肿瘤)。尽管存在这些细微差异,但总体而言,液体活检在识别主要驱动基因和可干预靶点方面,表现出卓越的准确性。
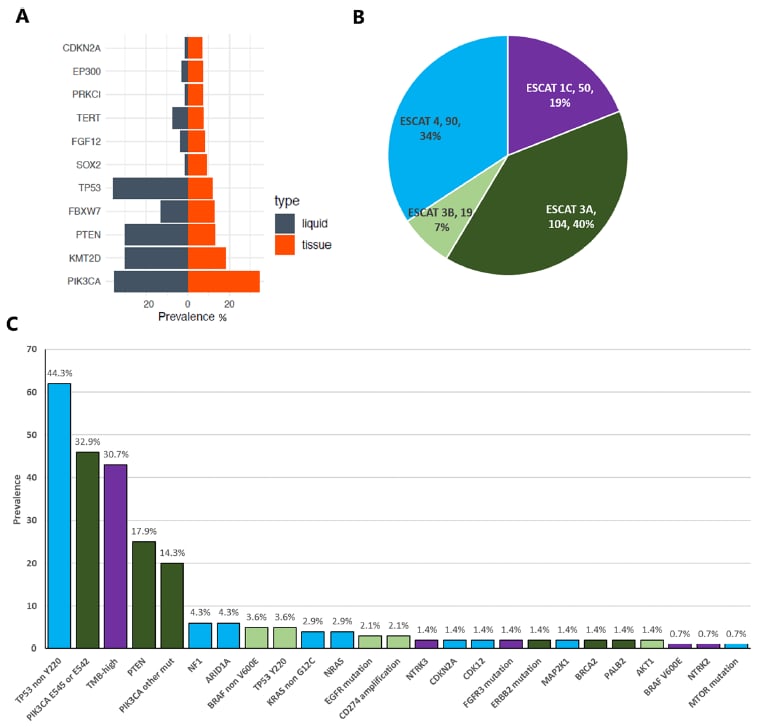
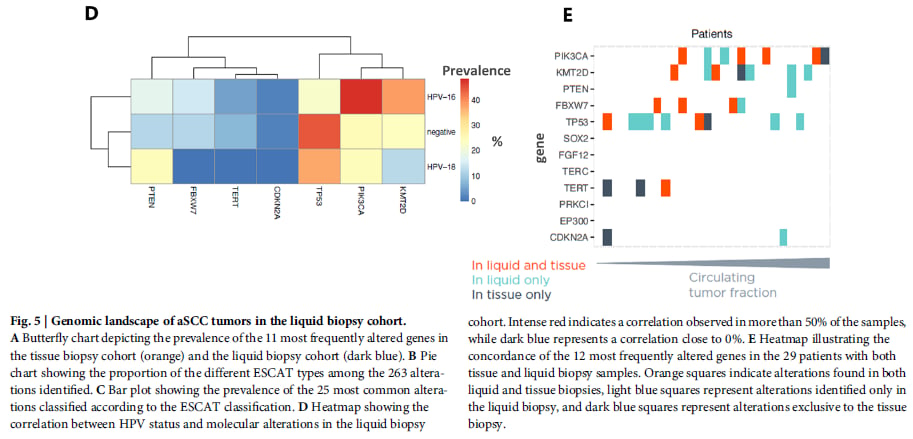
更令人振奋的是,对于29例同时接受两种活检的患者,在组织活检无诊断价值的情况下,液体活检仍能提供独特的分子信息,这大大拓宽了那些难以进行组织活检或活检失败患者的治疗选择。
真实世界应用案例解析
研究通过4个真实的临床案例,生动地展示了液体活检在aSCC患者个体化治疗中的巨大潜力:
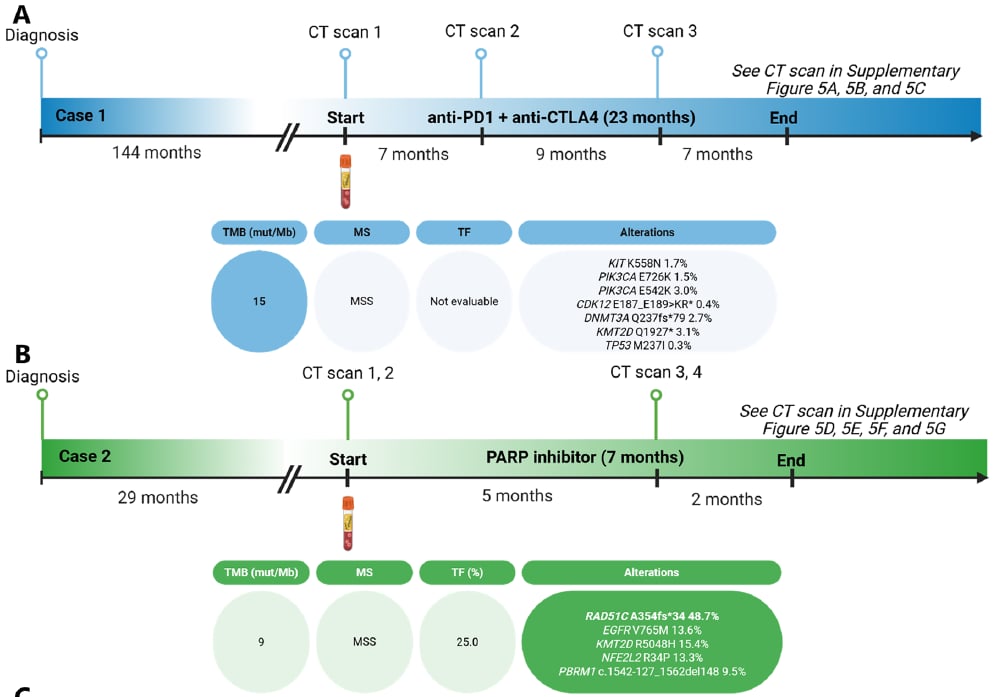
- 案例1:高TMB助力免疫治疗奇效一位60多岁女性患者,aSCC复发且多次治疗后进展。液体活检显示其血液肿瘤突变负荷(bTMB)高达15 mut/Mb,并伴有KIT K558N和两个PIK3CA突变。基于高bTMB,患者入组了PD-1抑制剂联合CTLA-4抑制剂的临床试验。经过23个月治疗,肿瘤体积显著缩小72%(根据RECIST标准)甚至92%(根据iRECIST标准),并达到部分代谢缓解,目前无病生存。这个案例充分说明了高TMB作为免疫治疗生物标志物在aSCC中的价值。
- 案例2:PARP抑制剂为BRCA相关突变患者带来希望一名59岁女性aSCC肝转移患者,液体活检发现RAD51C A354fs*34胚系突变。RAD51C是DNA修复相关基因,其突变常导致DNA修复缺陷,使细胞对PARP抑制剂敏感。患者因此入组了PARP抑制剂和ICIs的临床试验,获得6个月的无进展生存期(PFS),肿瘤体积缩小21%,病情稳定。这为携带DNA修复基因突变的aSCC患者提供了新的治疗方向。
- 案例3:FGFR抑制剂的成功与耐药性分析一位62岁局部晚期aSCC女性患者,放化疗后复发进展。液体活检发现FGFR2 K659N突变,入组FGFR抑制剂(FGFRi)的1期临床试验。尽管患者的最佳客观疗效为病情稳定,PFS达4个月,提示疾病存在原发性耐药。研究者进一步分析发现,在同一份液体样本中还存在NF1和PTEN突变,这可能是导致治疗效果不佳的原因。这个案例不仅展示了靶向治疗的潜力,也强调了通过液体活检动态监测基因突变,分析耐药机制的重要性。
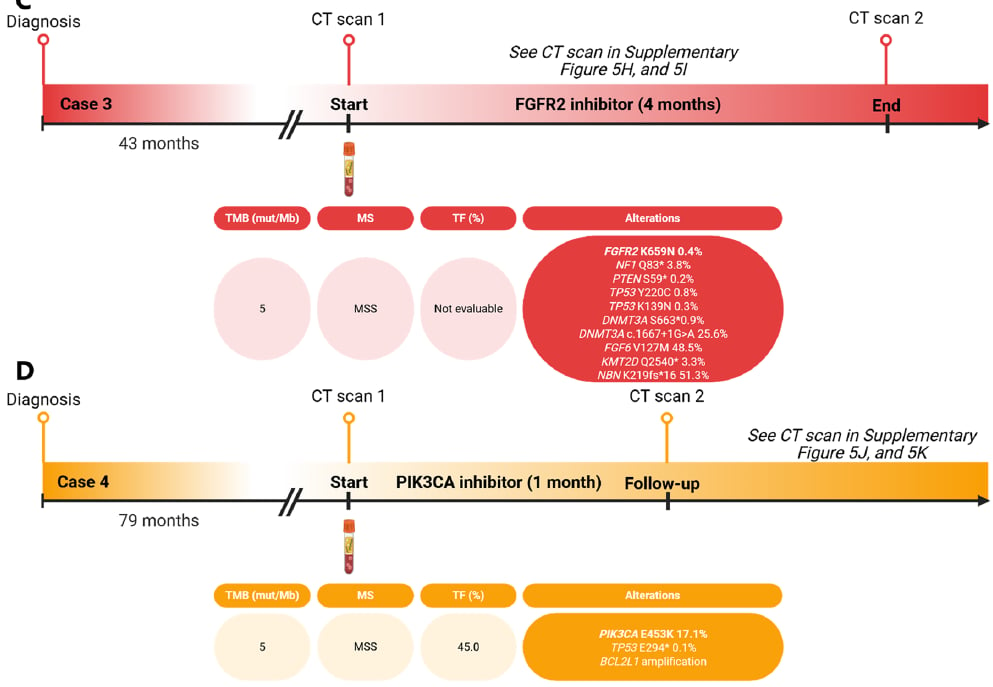
- 案例4:PIK3CA抑制剂的初步成功一名63岁转移性aSCC女性患者,在拒绝进一步化疗后,液体活检发现PIK3CA E453K突变。患者随后入组了PIK3CA抑制剂的临床试验。治疗两个月后,CT扫描显示患者病情稳定,且药物耐受性良好,目前仍在接受治疗。这为携带PIK3CA突变的aSCC患者带来了新的治疗选择。

这些案例充分说明了液体活检在真实世界中指导aSCC患者个体化治疗的巨大价值。它不仅能帮助患者发现潜在的可干预靶点,还能助力患者及时入组临床试验,从而获得最新的创新治疗方案。
液体活检的独特优势与局限性
这项研究首次大规模证实了液体活检在检测aSCC基因组变异中的价值,其优势在于:
- 微创便捷:仅需抽取少量血液,避免了侵入性组织活检的风险和不适。
- 克服取样困难:对于无法进行组织活检、肿瘤部位难以触及或身体状况不允许的患者,液体活检提供了唯一的基因检测途径。
- 反映肿瘤异质性:液体活检能够捕获来自不同转移灶的肿瘤DNA,更全面地反映肿瘤的整体基因组特征。
- 动态监测:可重复取样,有助于实时监测肿瘤演变、评估治疗反应和发现耐药机制。
然而,液体活检也存在一定的局限性。例如,它对循环肿瘤DNA(ctDNA)的释放水平有要求,可能在某些情况下对拷贝数变异的检测灵敏度略低于组织活检。此外,克隆性造血(一种与年龄相关的良性造血干细胞突变)可能导致一些非肿瘤来源的突变信号,从而干扰结果的解读。尽管如此,随着技术的不断发展和算法的优化,这些局限性正在逐步克服。
精准医疗:aSCC患者的未来与希望
这项迄今为止最大规模的aSCC基因组研究,为aSCC的精准医疗发展奠定了坚实基础。它不仅揭示了该疾病的分子“指纹”,更重要的是,为患者的个性化治疗指明了方向。
靶向治疗前景广阔
研究中发现的大量可干预靶点,预示着aSCC的靶向治疗前景广阔:
- PARP抑制剂:鉴于近6%的aSCC患者存在BRCA1/2等DNA修复基因的致病性变异,PARP抑制剂有望成为这类患者的重要治疗选择。这些药物已在卵巢癌、乳腺癌、胰腺癌和前列腺癌等多种癌症中获批应用。
- PIK3CA抑制剂:PIK3CA是aSCC中最常见的突变基因,其突变在多种实体瘤中均常见。针对PIK3CA的抑制剂,如阿培利司(Alpelisib)、伊那利塞(Inalixept)和卡帕塞替尼(Capivasertib),已在乳腺癌中取得成功。本研究的案例也为这些药物在aSCC中的应用带来了希望。
- FGFR抑制剂:针对FGFR2/3基因变异的FGFR抑制剂,已在其他癌症中显示出良好疗效。尽管本研究案例中存在耐药情况,但也提示了联合治疗和动态监测的重要性。
- KRAS G12C抑制剂:随着KRAS G12C抑制剂在非小细胞肺癌和结直肠癌中的成功应用,本研究中发现的KRAS基因变异,尤其是G12C突变,提示这类药物也应在aSCC患者中进行评估。此外,新型泛KRAS抑制剂的研发也将为更多KRAS突变患者带来福音。
目前,专门针对aSCC靶向治疗的临床试验相对较少,但本研究结果强烈呼吁将aSCC患者纳入更广泛的、针对这些靶点的“篮式试验”或其他临床试验中,以评估这些靶向疗法的潜在疗效。
免疫治疗的精准化探索
除了靶向治疗,免疫检查点抑制剂(ICIs)也已成为aSCC的治疗选择之一。本研究发现17.1%的aSCC患者具有高肿瘤突变负荷(TMB-H)。高TMB与ICIs在多种实体瘤中的疗效提升相关,提示这部分aSCC患者可能从ICIs治疗中获益更多。未来的研究应进一步探索如何通过TMB等生物标志物,更精准地筛选出对免疫治疗敏感的aSCC患者。
MedFind助力您获取前沿疗法
面对aSCC这种罕见且治疗选择有限的疾病,获取最新的药物信息和治疗方案至关重要。作为癌症患者家属发起的平台,MedFind致力于为癌症患者及其家庭提供全面、及时、可信赖的抗癌资讯、诊疗指南和药物信息。我们的核心服务包括抗癌药品的跨境直邮,旨在协助患者突破地域限制,获取国内尚未上市但已在国际上显示出良好疗效的创新药物,如文章中提及的各种靶向抑制剂。同时,MedFind还提供AI辅助问诊服务,帮助患者更好地理解复杂的医学信息,辅助您做出明智的治疗决策。
结语
这项迄今为止规模最大的肛门鳞状细胞癌基因组研究,为aSCC的精准诊断和治疗开启了新的篇章。它首次大规模证实了液体活检在指导个体化治疗中的强大潜力,并揭示了aSCC中丰富的可干预靶点。虽然挑战犹存,但研究者倡导将肿瘤基因谱分析作为常规检查,并积极整合临床试验机会。MedFind相信,通过国际合作和持续的研究,未来的aSCC患者将有更多、更精准的治疗选择,从而改善预后,重获健康与希望。如果您或您的家人正在与aSCC抗争,请不要放弃希望,积极了解最新的治疗进展,MedFind将一路相伴。
参考文献:
Smolenschi, C., Sisoudiya, S.D., Hollebecque, A. et al. Comprehensive molecular landscape of anal squamous cell carcinoma: analysis of tissue and liquid biopsies from 1844 patients. npj Precis. Onc. 9, 404 (2025). https://doi.org/10.1038/s41698-025-01181-4





