弥漫性中线胶质瘤(DMG),尤其以H3K27M改变为表观遗传学特征的类型,是一种高度恶性的脑肿瘤,起源于脑桥、丘脑和脊髓等中线结构。由于其侵袭性强且治疗选择有限,患者预后极差,急需新的治疗策略。长期以来,神经元活动与胶质瘤增殖之间的复杂关系备受关注,而近期一项突破性研究为我们揭示了潜在的靶向治疗新方向。
2025年6月24日,由斯坦福大学Michelle Monje教授和“光遗传学之父”Karl Deisseroth教授联合领导的团队在国际顶尖期刊《Cell》上发表重磅文章,深入阐明了中脑胆碱能环路如何以活性依赖方式促进胶质瘤细胞增殖的分子和环路机制。这一发现为攻克弥漫性中线胶质瘤带来了新的曙光。

中脑胆碱能投射:精准调控胶质瘤增殖的关键
研究团队发现,外背侧被盖核(LDT)和脑桥被盖核(PPT)的胆碱能神经元对脑桥和丘脑区域存在特异性投射。通过光激活LDT脑区的胆碱能神经元,可特异性促进丘脑区域的少突胶质细胞前体细胞和胶质瘤细胞增殖;同样,激活PPT脑区的胆碱能神经元,则能引起脑桥区域的少突胶质细胞前体细胞和胶质瘤细胞增殖。这种调控呈现出高度的环路依赖性,即对特定脑区的胶质瘤增殖产生影响,而不影响其他区域。
更重要的是,在携带H3.3-K27M DMG患者来源肿瘤的动物模型中,抑制LDT胆碱能神经元到丘脑的投射,或抑制PPT胆碱能神经元到脑桥的投射,均能显著减少相应区域胶质瘤细胞的增殖。这表明,精准干预这些胆碱能通路有望成为抑制弥漫性中线胶质瘤生长的有效策略。
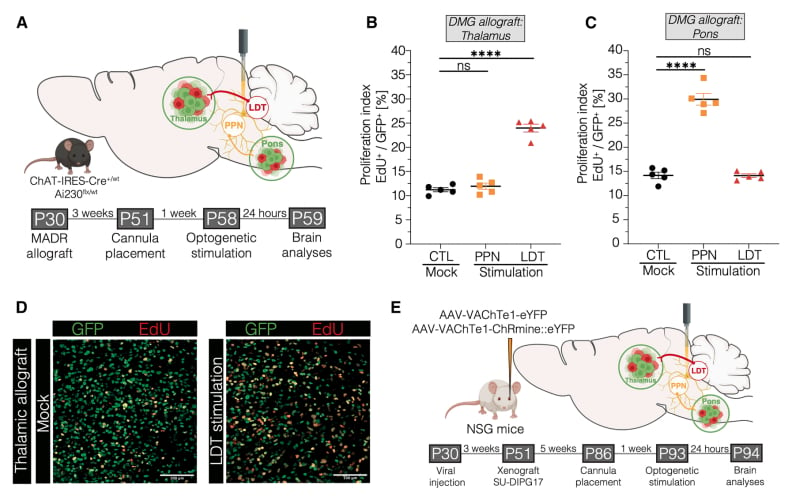
图1、中脑胆碱能投射以环路依赖方式调控胶质瘤细胞的增殖
毒蕈样乙酰胆碱受体M1R与M3R:潜在的靶向治疗突破口
进一步研究揭示,胆碱能神经元促进胶质瘤细胞增殖的作用,主要依赖于毒蕈样乙酰胆碱受体,而非烟碱型受体。离体实验证实,乙酰胆碱能以剂量依赖方式促进胶质瘤细胞增殖,且这一作用可被毒蕈样乙酰胆碱受体阻滞剂有效阻断。
单细胞测序分析显示,DMG患者大脑组织中富集表达M1型毒蕈样乙酰胆碱受体(CHRM1)和M3型毒蕈样乙酰胆碱受体(CHRM3)基因。令人振奋的是,单独使用M1R拮抗剂或M3R拮抗剂效果不明显,但联合使用M1R和M3R拮抗剂,则能显著抑制光激活胆碱能神经元所诱导的胶质瘤细胞增殖。敲除CHRM1和CHRM3基因也产生了类似的效果,这强烈提示M1R和M3R是弥漫性中线胶质瘤极具潜力的靶向治疗靶点。对于正在寻找前沿抗癌资讯和诊疗指南的患者,可以访问MedFind抗癌资讯平台获取更多信息。
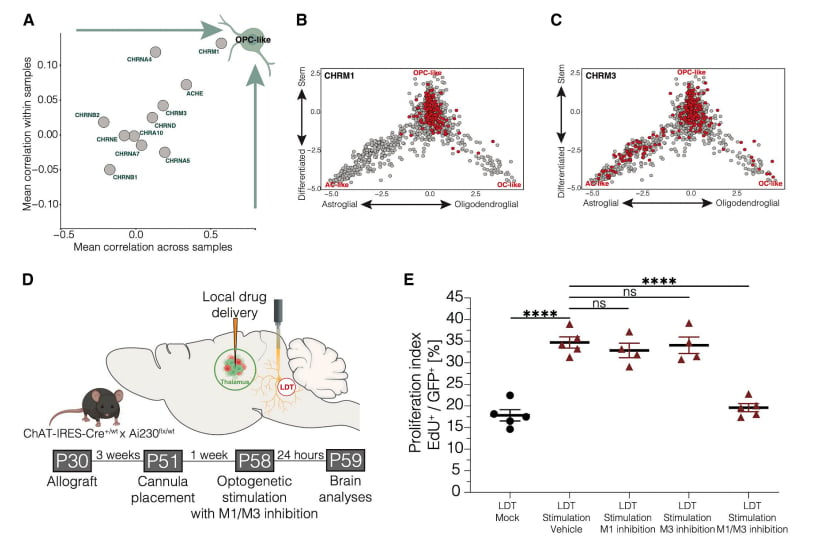
图2、中脑胆碱能神经元依赖毒蕈样乙酰胆碱受体调控胶质瘤细胞增殖
胶质瘤与胆碱能神经元的“双向对话”
研究还发现,胶质瘤细胞与胆碱能神经元之间存在复杂的交互调控作用。当胶质瘤细胞被移植到小鼠丘脑或脑桥后,LDT和PPT脑区的胆碱能神经元活性显著增加,乙酰胆碱释放增多,兴奋性突触后电流增强。这表明胶质瘤并非被动受体,它能反过来影响神经元的活动,形成一个恶性循环,进一步促进肿瘤生长。
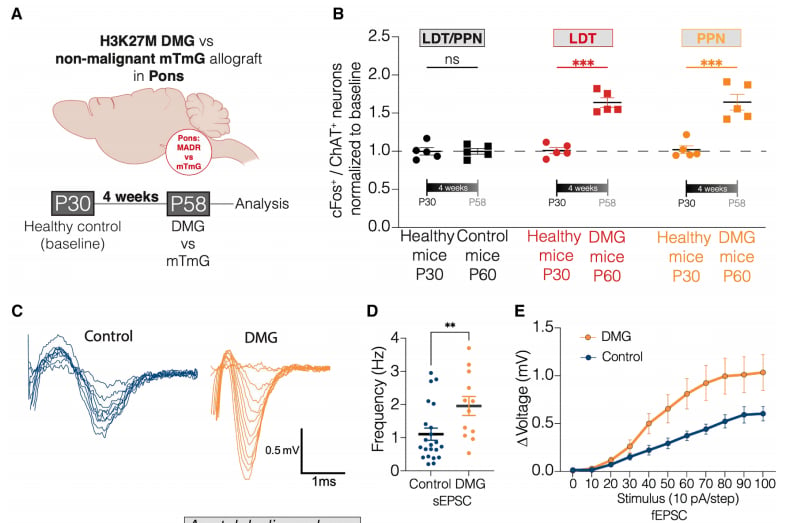
图3、中脑胶质瘤细胞和胆碱能神经元存在交互调控作用
总结与展望:H3K27M弥漫性中线胶质瘤靶向治疗的新篇章
这项Cell研究的重大意义在于,它首次清晰地揭示了中脑胆碱能神经元以环路依赖方式,通过毒蕈样乙酰胆碱受体M1R和M3R促进弥漫性中线胶质瘤增殖的机制。这一发现不仅加深了我们对H3K27M弥漫性中线胶质瘤生物学行为的理解,更为开发针对胆碱能通路的创新性靶向药物提供了坚实的理论基础。
对于面临H3K27M弥漫性中线胶质瘤挑战的患者而言,这一研究无疑带来了新的希望。未来,针对M1R和M3R的联合靶向治疗策略,有望成为改善患者预后的关键。如果您正在寻找海外前沿靶向药物或需要专业的AI问诊服务,欢迎访问MedFind海外靶向药代购平台和MedFind AI问诊服务,我们致力于为癌症患者提供全球最新的治疗选择和个性化支持。





