嵌合抗原受体T细胞(CAR-T)疗法作为一种革命性的免疫治疗手段,近年来在癌症治疗领域取得了举世瞩目的成就。尤其在急性白血病和非霍奇金淋巴瘤等血液系统恶性肿瘤的治疗中,CAR-T细胞疗法展现出显著疗效,为无数患者带来了长期缓解乃至临床治愈的希望。然而,这项前沿技术仍在不断演进,以克服实体瘤治疗的挑战和提高疗效持久性。
CAR-T疗法的核心在于通过基因工程改造患者自身的T细胞,使其表达特异性嵌合抗原受体(CAR),从而精准识别并杀伤癌细胞。尽管其在血液肿瘤中表现出色,但在实体瘤治疗中,CAR-T细胞疗法却面临着肿瘤微环境复杂、细胞渗透性差、抗原异质性以及潜在毒副作用等重重挑战。此外,部分患者在接受治疗后仍可能面临复发,如何提升CAR-T细胞的持久性和抗衰老能力,成为当前研究的焦点。
CAR-T细胞疗法前沿研究进展一览
1. “即插即用”CAR-T:实体瘤治疗的新策略
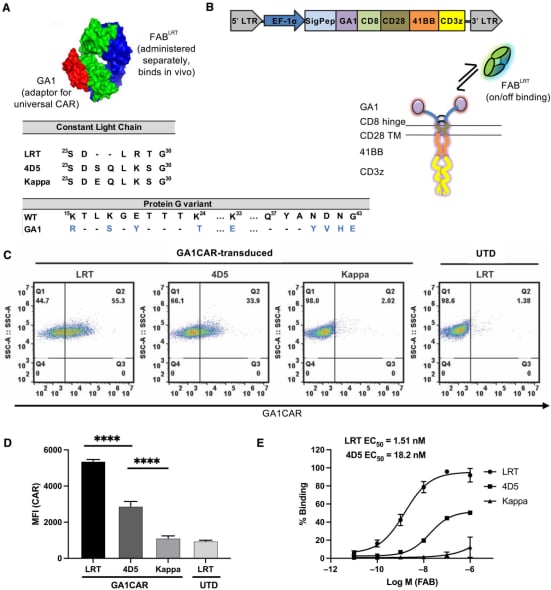
针对实体瘤治疗的困境,芝加哥大学科研团队开发出一种变革性的“通用型”嵌合抗原受体(CAR)平台——GA1CAR。这项发表在《科学进展》(Science Advances)杂志上的研究,创新性地将抗原识别元件与CAR-T细胞内的信号传导机制分离,采用模块化“分离式”设计。通过更换短效抗体片段(Fab),临床医生可以根据患者肿瘤的具体情况,灵活调整CAR-T细胞的靶向性,实现精准打击,同时降低毒副作用,为实体瘤治疗带来新的曙光。
2. 揭示CAR-T疗法复发机制:细胞衰老与共刺激域差异
尽管CAR-T细胞疗法在血液系统恶性肿瘤中取得了显著疗效,但超过60%的患者在1-2年内复发,长期缓解率仅维持在30%-40%。《Molecular Cancer》杂志上的一项研究指出,细胞衰老可能是CAR-T疗法失败的“隐形杀手”。研究发现,CAR结构中的“共刺激域”差异,直接决定了CAR-T细胞是否容易陷入衰老状态。目前临床常用的两种共刺激域:4-1BB-CD3ζ(BBζ)和CD28-CD3ζ(28ζ),在面对反复激活时,其“衰老抵抗力”截然不同,这一发现为优化CAR-T疗法、延长疗效持久性开辟了全新路径。

3. 基于iPSCs的CAR-NK细胞疗法:治疗系统性硬化症的潜力
系统性硬化症是一种致死率极高的自身免疫疾病,传统治疗效果不佳。中国人民解放军海军军医大学长征医院等机构的研究人员在《细胞》(Cell)杂志上发表了一项突破性研究,开发出一种基于人类诱导性多能干细胞(iPSCs)的现成细胞疗法——QN-139b。通过基因编辑iPSCs,使其靶向CD19和BCMA等靶点,并分化为自然杀伤细胞系,成功缓解了一名严重弥漫性皮肤型系统性硬化症女性患者的致命性皮肤和器官瘢痕。这项研究为自身免疫疾病和癌症治疗提供了新的思路。

4. “特洛伊木马”策略攻克胶质母细胞瘤
胶质母细胞瘤(GBM)素有“脑癌之王”之称,治疗难度极大。意大利圣拉斐尔-泰莱顿基因治疗研究所等机构在《科学转化医学》(Science Translational Medicine)上发表研究,巧妙利用基因疗法将肿瘤相关巨噬细胞(TEMs)改造成“特洛伊木马”。通过改造TIE2表达的TEMs,使其在肿瘤局部特异性释放免疫刺激因子干扰素-α(IFN-α)和工程化白细胞介素-2(oIL-2),成功激活CAR-T细胞,显著抑制了胶质母细胞瘤的生长,延长了小鼠的生存期。这一策略有望破解实体瘤免疫抑制微环境的难题。

5. 双靶点CAR-T细胞有望突破T细胞急性淋巴细胞白血病治疗瓶颈
T细胞急性淋巴细胞白血病(T-ALL)的免疫治疗进展缓慢,主要因恶性T细胞与健康T细胞表面抗原高度相似,易导致“自相残杀”。西班牙何塞普-卡雷拉斯白血病研究所等机构在《血液学与肿瘤学杂志》(Journal of Hematology & Oncology)上发表研究,聚焦于两个非泛T抗原——CCR9和CD1a,开发并验证了一种双靶点CAR-T细胞治疗策略。该策略可覆盖86%的T-ALL患者,并在体外实验中展现出强大的活性和特异性,且无明显自相残杀现象,为T-ALL患者带来了新的治疗希望。

6. 体内制备CAR-T细胞:简化癌症和自身免疫疾病治疗
CAR-T细胞疗法虽然有效,但其昂贵的个性化实验室流程限制了普及。卡普斯坦治疗公司(Capstan Therapeutics)研究人员在《科学》(Science)杂志上证实,靶向脂质纳米颗粒(tLNPs)可在体内对CAR-T细胞进行基因改造,无需实验室细胞制造和体外扩增。这种新型脂质纳米颗粒药物L829,一次制备可适用于多名患者,显著降低成本和专业中心依赖。实验显示,在人源化小鼠模型中,单次静脉注射即可诱导近乎完全的B细胞耗竭,并有效清除白血病肿瘤,有望用于治疗B细胞癌症、狼疮、肌炎等疾病。

7. 靶向Eva1的CAR-T细胞在实体瘤治疗中展现巨大潜力
实体瘤治疗一直是CAR-T细胞疗法的难点。名古屋大学医学院等机构在《免疫肿瘤学杂志》(Journal for ImmunoTherapy of Cancer)上发表研究,首次将Eva1(MPZL2)作为CAR-T细胞疗法的靶点,并成功开发了靶向Eva1的CAR-T细胞。Eva1在多种实体瘤中高度表达,但在正常组织中表达较低,使其成为理想的靶点。研究在多种实体瘤模型中展示了其显著的治疗效果,为实体瘤患者带来了新的希望。

8. 西达基奥仑赛(cilta-cel)为多发性骨髓瘤患者带来长期缓解
多发性骨髓瘤(MM)是一种常见的血液系统恶性肿瘤,预后不佳。西奈山伊坎医学院等机构在《临床肿瘤学杂志》(Journal of Clinical Oncology)上发表了一项关于西达基奥仑赛(cilta-cel,Ciltacabtagene Autoleucel)治疗复发/难治性多发性骨髓瘤(RRMM)的长期(≥5年)缓解和生存研究。研究显示,中位随访时间为61.3个月,33%的患者在治疗后≥5年仍保持无进展生存且无需进一步治疗。这项研究揭示了西达基奥仑赛在多发性骨髓瘤治疗中的巨大潜力和长期疗效,为患者重获新生带来了希望。
CAR-T细胞疗法及其衍生技术正以前所未有的速度发展,不断突破癌症治疗的边界。从克服实体瘤的挑战,到提升疗效持久性,再到简化制备流程,这些前沿研究为全球癌症患者带来了新的希望。随着更多创新疗法的涌现,未来癌症治疗将更加精准、高效和可及。
如果您正在寻找海外靶向药,可以访问MedFind的药品代购服务。同时,MedFind还提供专业的AI问诊服务,帮助患者更好地理解病情和治疗方案。更多抗癌资讯和诊疗指南,请查阅MedFind的抗癌资讯平台。





