引言
乳腺癌作为全球女性发病率最高的恶性肿瘤之一,其早期发现对于改善治疗效果和患者生存率具有决定性意义。然而,传统的影像学筛查手段,如乳腺钼靶和超声,常因假阳性率高导致不必要的活检,而血清肿瘤标志物(如CA15-3)在早期乳腺癌检测中的敏感度又显不足。因此,开发一种精准、无创的液体活检技术,用于高风险人群的早期筛查,已成为临床研究的热点。
近期,一项由温州医科大学苏建忠教授团队、中国医学科学院肿瘤医院刘嘉琦教授团队与世和基因合作开展的大型前瞻性多中心队列临床研究——DECIPHER-BRCA,取得了突破性进展。该研究利用世和MERCURY cfDNA多组学早筛技术,构建了基于cfDNA片段组学特征的cfFrag模型,不仅成功实现了对早期乳腺癌的精准识别,还能预测新辅助治疗的反应。更重要的是,研究提出的cfFrag-影像联合模型,进一步提高了早期乳腺癌的检出效能。这项重要成果已发表于国际期刊《Genomics, Proteomics & Bioinformatics》。

研究核心亮点
1. 大规模前瞻性验证:
研究纳入了613名女性参与者,通过多中心前瞻性设计,有力证实了基于MERCURY cfDNA多组学技术的cfFrag模型在区分早期乳腺癌与良性结节方面的有效性。
2. 性能超越传统方法:
cfFrag模型在鉴别乳腺结节良恶性方面展现出高准确性,尤其对于难以诊断的小结节,其表现优于传统的乳腺钼靶和超声检查,有助于减少不必要的侵入性活检。
3. 预测新辅助治疗疗效:
该模型能够预测乳腺癌患者接受新辅助治疗后的反应,区分达到病理完全缓解(pCR)和未达到(Non-pCR)的患者,为个体化治疗决策提供了新的生物标志物。
4. 多组学联合优势:
研究表明,cfDNA片段组学方法的准确性与甲基化方法相当,但成本更低、操作更简便。将cfDNA多组学信息(片段组学+甲基化)结合,或将片段组学与影像学数据结合,能显著提升早期乳腺癌的诊断效能(AUC可达0.96甚至0.97)。
研究设计与方法
这项前瞻性多中心临床研究共纳入613名女性受试者(见图1)。研究设计包括:
- 探索队列(烟台):包含91名乳腺癌患者和102名良性乳腺结节患者,用于训练cfFrag模型。
- 多中心验证队列:包括北京队列(209例乳腺恶性可疑病变患者)、杭州队列(40例乳腺癌和13例良性结节患者)、外部筛查队列(119名无症状健康女性)、新辅助化疗队列(33例化疗后乳腺癌患者)和稳健性队列(3例乳腺癌和3例良性结节患者)。
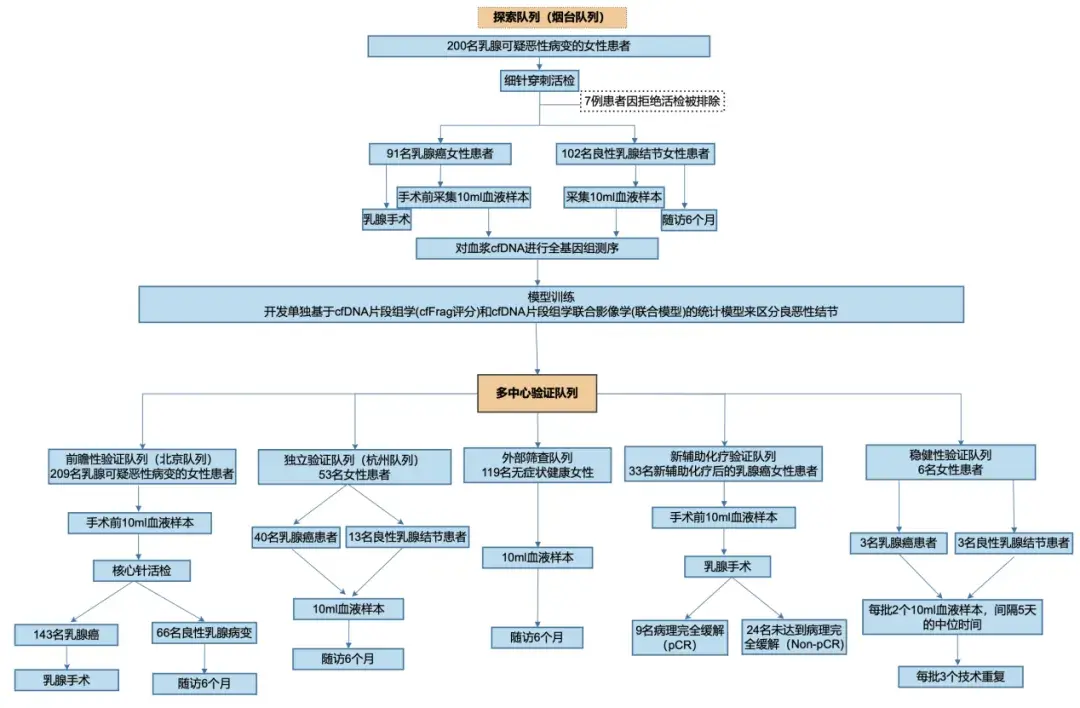
图1. 研究设计流程图
主要研究结果
1. cfFrag模型精准区分早期乳腺癌与良性结节
研究基于cfDNA的片段大小比率(FSR)、片段大小分布(FSD)和拷贝数变异(CNV)构建了cfFrag模型。结果显示,该模型在训练集(烟台队列)和前瞻性验证集(北京队列)中区分乳腺癌与良性结节的曲线下面积(AUC)分别为0.82和0.81(图2B)。在独立的杭州验证队列中,AUC更是高达0.95(图2C),证实了其优异的鉴别能力。
在设定85%的敏感性时,模型在训练集和前瞻性验证集中的特异性分别为65.7%和60.6%。在无症状健康女性队列中,特异性达到94.1%(图2D),显示出其在乳腺癌早期筛查中的巨大应用潜力。
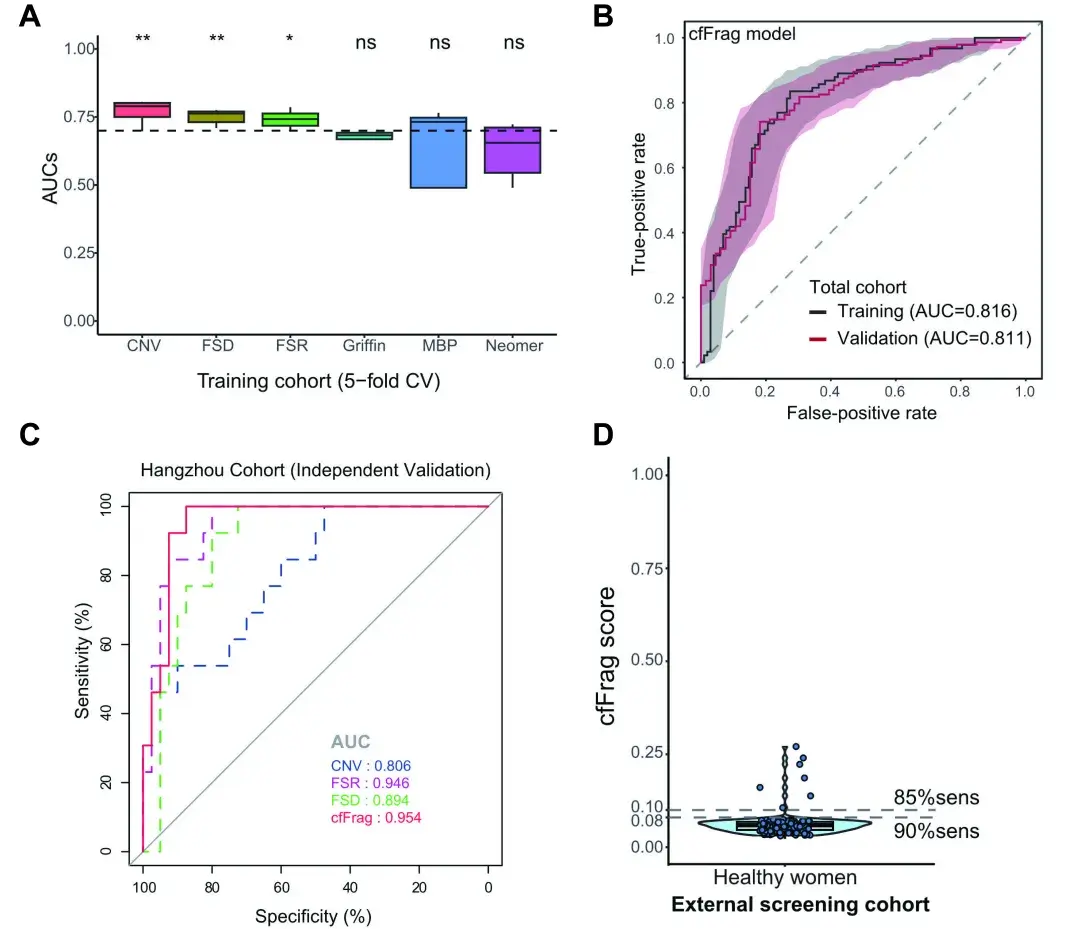
图2. cfFrag模型在早期乳腺癌预测及良性结节鉴别中的性能比较
2. 片段组学技术在乳腺小结节检测中优于传统筛查
考虑到年龄因素可能带来的偏倚,研究进行了倾向评分匹配分析。在年龄匹配的子集中,cfFrag模型依然保持了优异的预测能力(AUC均为0.82,图3A)。
进一步分析表明,cfFrag模型在不同临床亚组(如结节大小、分期、组织学类型、激素受体状态)中均表现稳定。特别是在小结节(≤1cm)亚组中,前瞻性验证集的AUC达到0.83(图3B)。与传统检查方法(乳腺钼靶AUC=0.64,超声AUC=0.80)相比,cfDNA片段组学模型展现出更优越的性能(图3C、D),有望减少对小结节患者的不必要活检。
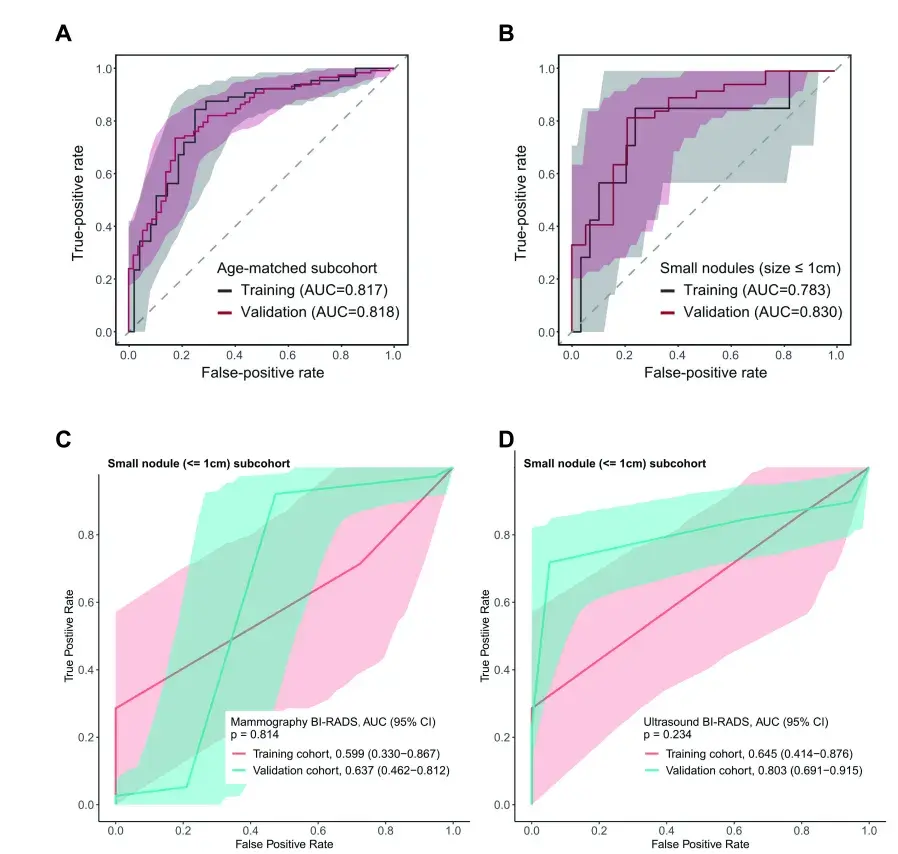
图3. cfFrag模型对乳腺小结节的预测能力优于传统检查方法
3. 片段组学特征稳健可靠,可预测新辅助治疗反应
为了评估技术的经济性和临床实用性,研究在稳健性验证队列中使用了降采样数据。结果显示,即使测序深度降至3×,cfFrag模型的预测能力也未显著下降(p>0.05,图4A),表明该技术具有良好的成本效益潜力。
重复性测试也证实了cfDNA片段组学特征(CNV、FSR、FSD)的高度稳定性(图4B),支持了cfFrag模型在临床推广的可行性。
此外,该研究发现cfFrag模型能有效区分接受新辅助化疗后达到pCR与未达到(Non-pCR)的乳腺癌患者,AUC达到0.82(图4C、D)。这提示cfDNA片段组学在预测治疗反应和监测微小残留病灶(MRD)方面具有潜在价值。
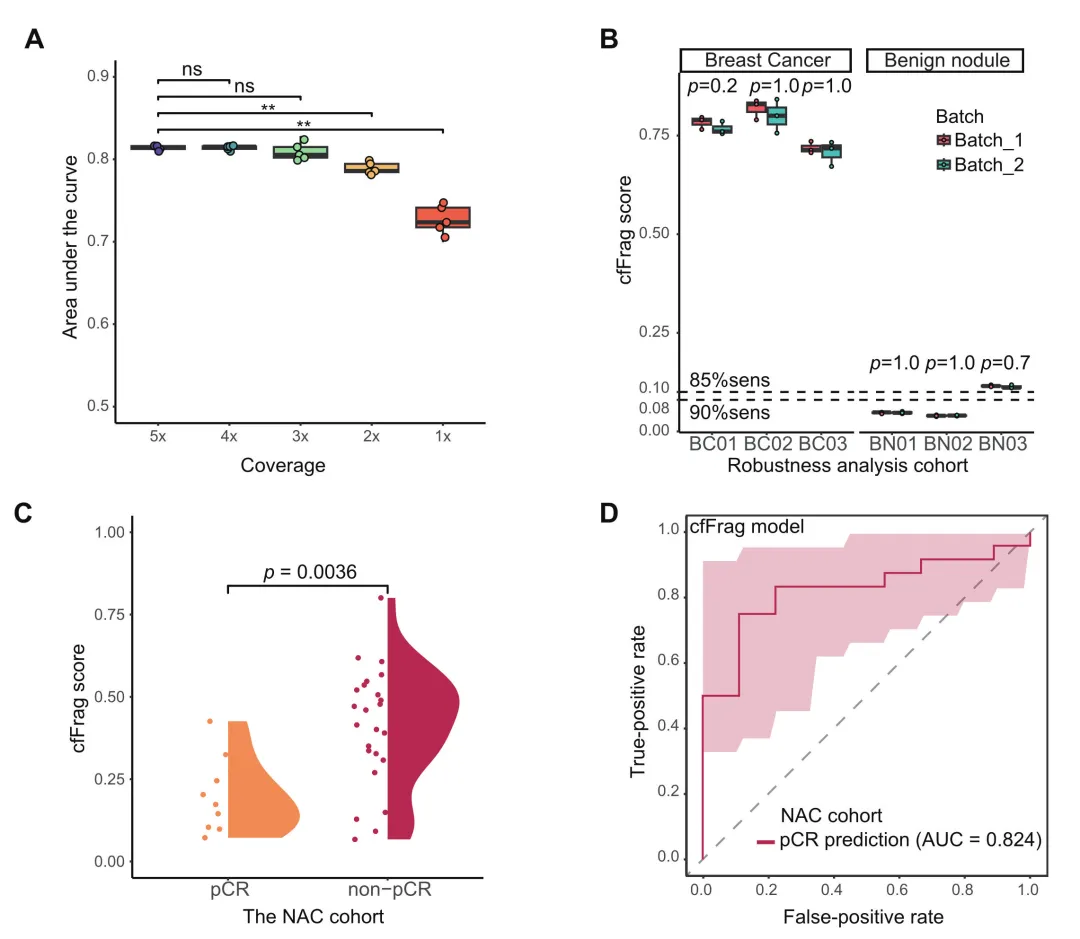
图4. cfFrag模型的性能稳定,能预测新辅助治疗反应
4. 多组学联合策略进一步提升诊断效能
研究比较了基于WGS(全基因组测序)的cfDNA片段组学模型(cfFrag)和基于WGBS(全基因组亚硫酸氢盐测序)的甲基化模型(cfMeth)在区分乳腺癌与良性结节方面的性能。结果显示两者性能相当,但cfDNA片段组学成本更低、操作更简便。
重要的是,将cfFrag与cfMeth联合(AUC=0.96),或将cfFrag与影像学数据(X光和超声的BI-RADS评分)联合,均能显著提升诊断准确性(图5B、C、D)。特别是cfFrag-影像联合模型,在训练集和验证集的AUC分别达到0.90和0.93。
临床价值评估模型预测,应用cfFrag-影像联合模型有望将中国I期乳腺癌的检测率从18%提升至93%,预计可使5年生存率提高14%(图5E);在美国,预计可将I期检测率提升至95%,5年生存率提高8%(图5F)。这表明联合模型不仅能提高诊断准确性,还能显著改善乳腺癌的分期,带来潜在的生存获益。
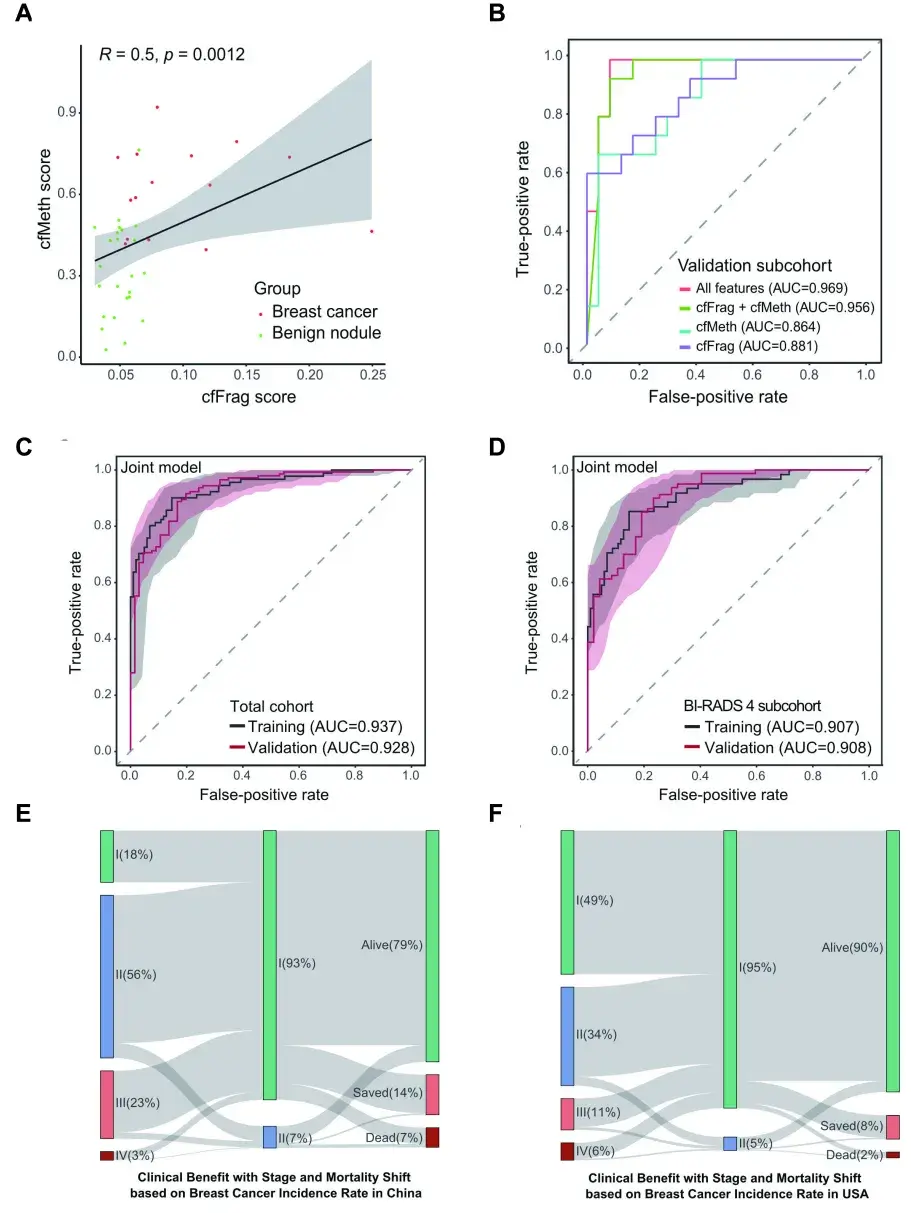
图5. cfFrag与cfMeth模型的性能及多组学联合诊断模型的性能
结论与展望
这项大型前瞻性多中心临床研究系统地评估了cfDNA片段组学作为乳腺癌无创生物标志物的巨大潜力。基于MERCURY cfDNA多组学早筛技术构建的cfFrag模型,在区分早期乳腺癌与良性结节、预测新辅助治疗反应方面均表现出色。特别是cfFrag-影像联合模型,显著提高了早期乳腺癌检测的准确性,有望优化当前的筛查策略,改善临床结局。
了解最新的癌症检测和治疗进展对于患者至关重要。如果您对乳腺癌的治疗方案或靶向药、仿制药代购信息感兴趣,可以参考MedFind抗癌资讯获取更多信息,或尝试使用MedFind AI问诊进行初步咨询。
参考文献:
1. Hubbell E, Clarke CA, Aravanis AM, Berg CD. Modeled reductions in late-stage cancer with a multi-cancer early detection test. Cancer Epidemiol Biomarkers Prev 2021;30:460-8.
2. Jiaqi Liu, Yalun Li, Wanxiangfu Tang, Tianyi Qian, Lijun Dai, Ziqi Jia, Heng Cao, Chenghao Li, Yuchen Liu, Yansong Huang, Jiang Wu, Dongxu Ma, Guangdong Qiao, Hua Bao, Shuang Chang, Dongqin Zhu, Shanshan Yang, Xuxiaochen Wu, Xue Wu, Hengyi Xu, Hongyan Chen, Yang Shao, Xiang Wang, Zhihua Liu, Jianzhong Su, Cell-free DNA Fragmentomics Assay to Discriminate the Malignancy of Breast Nodules and Evaluate Treatment Response, Genomics, Proteomics & Bioinformatics, 2025;, qzaf028.





