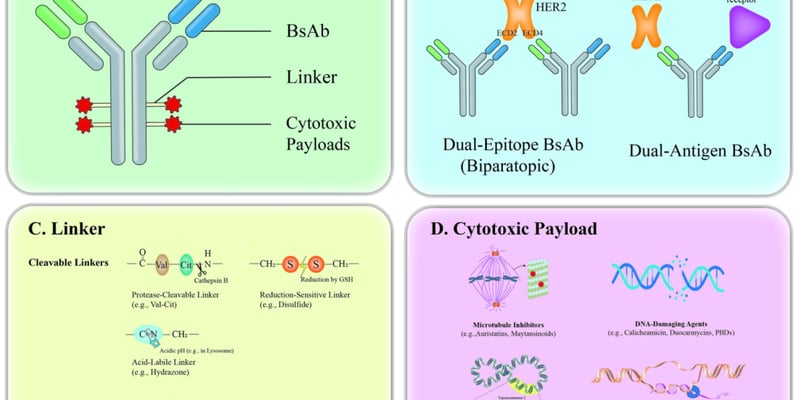
达雷妥尤单抗耐药的元凶:MYC激活
达雷妥尤单抗(Daratumumab)作为一种抗CD38单克隆抗体,已成为治疗浆细胞骨髓瘤(PCM)的重要药物。然而,临床实践中一个棘手的问题是,许多患者在初见疗效后最终会产生耐药性并复发。近期,一项发表于《Leukemia》的中国多中心研究为我们揭示了这一耐药现象背后的关键机制。如果您想了解达雷妥尤单抗的更多信息或海外代购渠道,可以访问MedFind海外靶向药代购平台。
研究团队通过对治疗前后患者的骨髓样本进行深入分析,发现MYC基因的激活是导致达雷妥尤单抗获得性耐药的核心驱动因素。有趣的是,这种激活与骨髓的免疫微环境密切相关。

骨髓微环境的变化揭示耐药线索
研究人员利用单细胞测序等先进技术,描绘了耐药发生时骨髓免疫生态系统的动态变化,主要包括:
- CD8+ T细胞功能耗竭:在耐药后,尽管释放干扰素-γ(IFN-γ)的CD8+ T细胞比例增加,但它们也表现出高表达TIGIT、LAG3等耗竭标志物的特征。持续的IFN-γ释放反而刺激了浆细胞中MYC的激活,促进了免疫逃逸。
- NK细胞功能失调:具有抗体依赖性细胞介导的细胞毒性(ADCC)功能的CD16+ NK细胞数量减少,而抑制性NK细胞增加,削弱了达雷妥尤单抗的杀伤效果。
- 肿瘤性浆细胞的演变:耐药的浆细胞不仅下调了药物靶点CD38的表达,还激活了与细胞增殖和代谢相关的通路,而这些通路均受到MYC的调控。
逆转耐药的新希望:靶向MYC治疗
基于以上发现,研究团队提出了一个大胆的设想:抑制MYC是否能逆转耐药?
随后的体外和动物模型实验证实了这一猜想。结果显示:
- 恢复药物敏感性:使用MYC抑制剂(MYC1975)能够显著恢复达雷妥尤单抗介导的ADCC和补体依赖的细胞毒性(CDC)效应。
- 抑制肿瘤生长:在小鼠模型中,达雷妥尤单抗与MYC抑制剂的联合使用,展现出强大的协同抗肿瘤效果,有效抑制了肿瘤的生长。
这一发现为临床治疗提供了新的思路。对于面临耐药困境的患者,及时了解最新的治疗方案至关重要。您可以通过MedFind AI问诊服务,获取个性化的前沿资讯和治疗建议。

研究总结与未来展望
这项研究系统地阐明了骨髓免疫微环境在浆细胞骨髓瘤对达雷妥尤单抗产生获得性耐药过程中的关键作用。它指出,由免疫压力驱动的MYC激活是连接免疫逃逸和肿瘤细胞代谢重编程的核心环节。
更重要的是,该研究为克服达雷妥尤单抗耐药提供了明确的治疗靶点和潜在策略。未来,随着更多研究的深入,靶向MYC的药物有望为浆细胞骨髓瘤患者带来更多有效的治疗选择。关注MedFind抗癌资讯,我们将持续为您带来最新的抗癌研究进展。