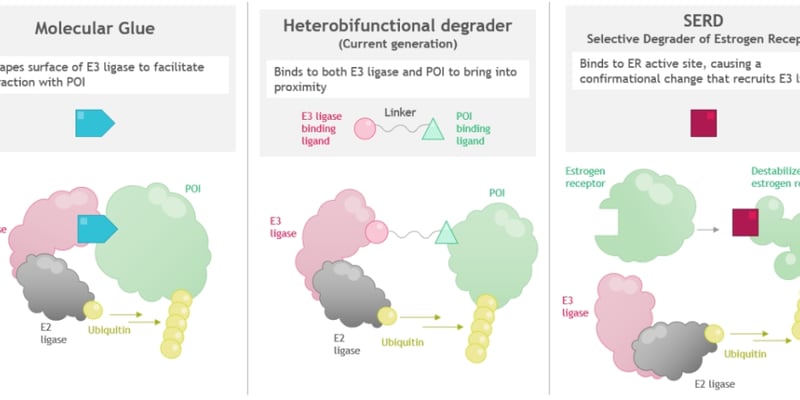
化疗耐药后的小细胞肺癌(SCLC)还有没有更“精准”的办法?当肿瘤普遍存在RB1与TP53失活、导致G1-S检查点崩溃时,能否反过来利用这种“先天缺陷”,把癌细胞推向自毁?围绕E2F活性失调与细胞周期调控,一类可口服的细胞可渗透环状肽(cyclin A/B RxL inhibitors,简称cyclin A/Bi)提出了新的解题路径:不是直接“堵死”E2F,而是通过阻断RxL介导的关键结合界面,制造癌细胞无法承受的细胞周期压力并诱导死亡。
为什么SCLC难治:检查点失守与E2F被“踩油门”
SCLC侵袭性强、进展快,临床上常见问题是:初治对化疗敏感,但复发后容易耐药,且长期缺乏成熟有效的靶向治疗选择。生物学层面,SCLC中常见RB1和TP53功能缺失性突变,这会破坏G1-S检查点,使细胞在不该进入复制阶段时也“硬闯”S期,并引发E2F转录因子活性失调。
不止SCLC,其他肿瘤也可通过CDKN2A缺失或细胞周期蛋白D/细胞周期蛋白E扩增等方式破坏G1-S检查点,最终都指向同一个结果:E2F活性过强。
E2F是把“双刃剑”:过强会把肿瘤推向凋亡
E2F的激活对细胞周期推进很重要,但当它被过度激活时,会触发细胞应激并促进细胞凋亡,从而形成一种可被治疗利用的“脆弱点”。关键挑战在于:如何在不伤及正常细胞基本增殖需要的前提下,让高E2F依赖的肿瘤细胞先崩溃。
“不可成药”的原因:RxL底物界面难以用小分子卡住
细胞周期蛋白(cyclin)会通过一个保守的疏水区域与带有短线性RxL基序的底物结合。这种“蛋白-蛋白相互作用”界面往往较平坦、缺少适合小分子嵌入的口袋,因此长期被视为难以靶向。
研究指出,细胞周期蛋白A可通过依赖RxL的相互作用抑制E2F;当这种相互作用被破坏时,E2F会被“放飞”,出现过度激活。基于这一逻辑,如果能用一种分子去阻断cyclin与RxL底物的结合,就可能把已处在高压力边缘的肿瘤细胞“推波助澜”到死亡阈值。

研究图示:通过抑制RxL介导的底物结合来干预细胞周期调控
cyclin A/Bi是什么:可口服、可入细胞的环状肽抑制剂
cyclin A/Bi是一类环状肽,特点包括:细胞可渗透、口服生物可利用,并能抑制细胞周期蛋白通过与底物的RxL介导相互作用而完成结合。它的定位更像是“阻断关键握手”,从而改变下游细胞周期与检查点信号。

机制模式图:cyclin A/Bi触发检查点压力并诱导有丝分裂期死亡
选择性杀伤的关键:高E2F活性肿瘤更“扛不住”
研究结论强调,cyclin A/Bi能够选择性杀死SCLC细胞以及其他具有高E2F活性的癌细胞。对患者而言,“选择性”的含义是:并非所有肿瘤都同等敏感,敏感性可能与其是否存在G1-S检查点受损、E2F被长期推高有关。
它如何把细胞推向死亡:从相互作用阻断到检查点致死
基因筛选提示,cyclin A/Bi通过依赖细胞周期蛋白B与CDK2的纺锤体组装检查点激活来诱导凋亡。机制链条可概括为:
- 阻断细胞周期蛋白A-E2F相互作用:使E2F被过度激活。
- 阻断细胞周期蛋白B-MYT1相互作用:导致细胞周期蛋白B相关通路被过度激活。
- 促进新的细胞周期蛋白B-CDK2复合物形成:该复合物能够驱动纺锤体装配检查点激活,最终引发有丝分裂期细胞死亡。
这套机制的直观理解是:肿瘤本来就“闯红灯”进入细胞周期,cyclin A/Bi再把关键制动/协调环节打乱,导致细胞在分裂阶段出现不可逆的灾难性错误,从而死亡。
对“化疗耐药SCLC”意味着什么:动物模型显示抗肿瘤活性
研究在化疗耐药的SCLC患者来源异种移植模型(PDX)中观察到:口服给药的cyclin A/Bi显示出强大的抗肿瘤活性。对真实患者来说,这类证据提示其具备进一步开发为临床治疗候选的潜力,但也必须明确:PDX结果不等同于人体疗效,距离“可常规用药”仍需经历临床试验验证(疗效、剂量、毒性谱、与化疗/免疫/放疗联用策略等)。
患者最关心的落地问题:哪些人可能更相关?如何与医生讨论
可能更相关的疾病特征(用于问诊沟通)
- SCLC,尤其是复发/耐药后治疗选择有限者。
- 肿瘤呈现G1-S检查点受损特征(如RB1/TP53相关通路异常)并伴随E2F活性偏高的生物学背景(具体需依赖研究级检测或临床试验入组标准)。
- 其他被认为存在E2F驱动特征的肿瘤类型(是否适用取决于未来试验设计与适应症开发,现阶段不要自行推断为“都能用”)。
与主管医生沟通的4个关键问题
- 我当前分期/复发线数/耐药状态下,标准治疗还有哪些选择?是否有可入组的临床试验?
- 是否做过或需要补做关键分子检测(例如RB1/TP53相关信息、增殖指标等),以评估是否属于“检查点受损/高增殖压力”人群?
- 如果未来有相关试验,常见入组门槛可能包括哪些(器官功能、既往治疗、脑转移控制情况等)?
- 若考虑海外试验或海外已上市药物(若未来出现),用药可及性、物流、处方与随访如何解决?
居家管理:SCLC系统治疗期间最实用的“保底策略”
即便新机制药物仍在开发,很多患者正在经历化疗、放疗、免疫治疗或后线方案。居家管理做得好,往往能直接决定能否按计划完成疗程。
血象与感染风险:最需要提前准备
- 体温管理:出现发热(尤其伴寒战、咳嗽加重、尿痛)要尽快就医排查感染与中性粒细胞减少风险。
- 口腔与皮肤护理:保持口腔清洁、避免破溃;皮肤破口及时处理,减少感染入口。
- 人群与环境:血象低时减少去密闭人群场所;家人出现呼吸道症状要戴口罩并尽量隔离。
营养与体重:把“吃得下”当成治疗一部分
- 高蛋白、少量多餐:鸡蛋、鱼、瘦肉、奶制品、豆制品等优先;吃不下时用营养补充饮品作为过渡。
- 恶心呕吐:遵医嘱规律使用止吐药,不要等到吐得厉害才补救;清淡、温凉食物更容易入口。
- 便秘/腹泻:根据症状调整纤维与水分摄入,必要时在医生指导下使用通便/止泻药。
情绪与睡眠:避免“熬”成二次打击
- 把不确定性写下来:将最担心的3件事列成清单,分别对应“能做什么”“谁能帮我”“何时复诊问医生”。
- 规律作息:睡眠差会放大疼痛、恶心与焦虑;必要时让医生评估是否需要短期助眠。
药物可及性与现实痛点:前沿不等于立刻用得上
cyclin A/Bi属于新机制候选治疗方向,当前信息重点在研究层面的机制与模型疗效。对患者来说,常见的现实问题包括:
- 是否已获批上市:研究阶段药物往往尚未在任何国家/地区形成常规处方可及性。
- 如何获取可靠信息:需要持续跟踪权威期刊、临床试验注册与指南更新,避免被“夸大疗效”的信息误导。
- 当治疗窗口很短:很多SCLC患者等不起信息滞后,往往需要同时评估“标准治疗优化”“临床试验机会”“海外可及药物”三条路径。
把前沿真正变成行动:什么时候需要MedFind介入
对SCLC家庭而言,最难的不是“知道一个新方向”,而是把它落到可执行方案:哪里能做进一步评估、下一步治疗怎么衔接、药物与方案如何获得且保证可信。
- 如果你正在为复发/耐药后的方案选择发愁,可以使用MedFind的辅助问诊:把病理、分期、既往治疗、影像与检验关键指标梳理成医生能快速判断的要点,帮助你更高效地和主管医生讨论“下一步最优路径”(标准治疗/试验/海外方案)。
- 如果你已明确需要某些海外已上市、国内暂未覆盖或可及性差的抗癌药,且具备合规处方与随访条件,MedFind可提供跨境直邮支持,减少信息差与时间差带来的延误风险。
真正的希望来自两件事:一是把肿瘤的“弱点”变成可验证的治疗策略;二是让你在关键时间点,拿到可信、可执行、可追踪的治疗选择。
【参考文献】
Targeting G1–S-checkpoint-compromised cancers with cyclin A/B RxL inhibitors. Nature. https://www.nature.com/articles/s41586-025-09433-w