近日,美国宾夕法尼亚大学癌症护理创新中心胸部和头颈医学肿瘤科主任、精准肿瘤学创新主任Aggarwal医生,在第18届纽约肺癌研讨会上,介绍了ctDNA液体活检技术对肺癌的重要作用。
1.Aggarwal医生表示,更早使用循环肿瘤DNA检测(ctDNA)技术,可帮助新确诊患者缩短治疗时间(医生更容易给出治疗决策),并可能提高生存率。
2.发表在国际权威期刊JAMA Oncology的文章显示,同时采用组织检测和血液ctDNA检测的患者,有更高比例被发现可靶向治疗的基因突变。
Aggarwal表示,循环肿瘤DNA检测(ctDNA)技术,为改善肺癌患者分子检测状况提供了帮助。比如在早期进行ctDNA检测,可帮助患者缩短治疗时间,提高生存率。
“我们正在实施一些策略,努力推动ctDNA成为长期有效的肿瘤实时生物标志物。”Aggarwal表示。
Aggarwal指出,肺癌中针对多种基因突变的靶向疗法,大幅改善了患者的生存状况。如EGFR三代药奥希替尼,根据3期FLAURA临床试验的数据,该药一线治疗EGFR阳性非小细胞肺癌患者,给他们带来了38.6个月的平均总生存期。
又比如ALK二代药艾乐替尼,在3期ALEX试验中治疗ALK阳性非小细胞肺癌患者表现也非常亮眼。
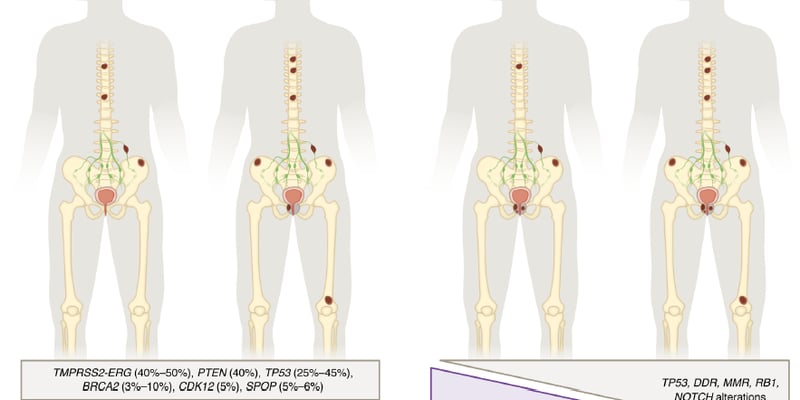
*下面这些肺癌基因突变,大约存在于50%的非鳞非小细胞肺癌当中,具体包括:
“我们应该记住,KRAS G12C以及HER2突变目前在肺癌二线治疗中是可以立即指导治疗行动的,估计很快这两个靶点的治疗会进入一线(成为初始治疗方案),因为新试验的结果即将出炉。”Aggarwal补充说。
个性化的肺癌靶向治疗,依赖于新一代基因检测(NGS)技术,如果不能及时得到相应检测结果,则患者很难通过靶向治疗得到收益。
患者通过基因检测获取分子检查结果,可以帮助实现个性化治疗、改善治疗结果以及降低非必要的治疗毒性。在临床上,ctDNA被用来为肺癌患者提供初步诊断信息,指导治疗计划的制定,还可监测靶向治疗和免疫治疗的效果以及预估长期预后。
将血液NGS与组织活检同时整合到临床实践中,已经被证实可提高NSCLC的基因检测能力,也改善了患者的靶向治疗可及性。例如,发表在国际权威期刊《JAMA Oncology》上的研究结果显示,进行了组织和血液NGS的患者中,有35.8%的患者被发现具有可靶向的靶点,而只进行了组织活检的患者中,这一比例为20.5%。
Aggarwal补充说,用新确诊肺癌患者的血液进行ctDNA检测,然后再进行组织活检,是完全没问题的。不过有时组织获取并不那么充足。
她还反思了一项关于新确诊的IV期非鳞状非小细胞肺癌患者的实际队列研究,研究人员分析了组织和ctDNA NGS同时进行对患者的综合影响。数据显示,进行全基因检测(包括EGFR、ALK、BRAF、ROS1、MET、RET和NTRK)的患者,其总生存期得到了改善。
总之,在开展一线治疗前,帮患者更快获取基因检测结果,与患者生存期的提高相关。
“这对那些不适合靶向治疗的患者同样适用,这可能是因为我们可以用更好的方式为患者排序治疗,”Aggarwal说。“例如,如果患者携带KRAS G12C突变,我们有信心能够基于其PD-L1状态提供化疗+免疫疗法或单免疫疗法。”
Aggarwal认为,在患者确诊后的早期阶段,将ctDNA的NGS检测整合到诊疗中,可改善患者治疗,缩短治疗时间。
在一项2022年的回顾性研究中,研究人员研究了初次活检时就做了ctDNA的非小细胞肺癌患者。结果显示,74%的患者在初次就诊时,就做出了治疗决策,而历史数据只有46%。而且这样做的患者,治疗时间也减少了。
“进行ctDNA液体活检的肺癌患者,在初次诊断时,由于信息更多,具体的治疗建议也更容易获取,”Aggarwal指出。“他们来到办公室,然后我就可以告诉他们‘我会给你免疫疗法’,因为我已经知道他们的PD-L1表达符合标准,且携带KRAS G12C突变。”
除了改善治疗、提高患者生存之外,ctDNA还可以用于检测正在靶向治疗的患者。临床医生可以观察他们的耐药性突变,以及一些患者接受免疫治疗时预估治疗反应的标志物。
美国宾夕法尼亚大学计划进行的一项研究,将用来评估ctDNA检测是否可以作为停止免疫疗法的指导。Aggarwal说,假设NSCLC患者通过长期ctDNA检测,发现指标没有风险,他们将预测患者在6个月内肿瘤不会复发进展,此时就可以停药了。
https://www.onclive.com/view/early-use-of-ctdna-may-accelerate-time-to-treatment-and-improve-survival-in-nsclc