铁死亡与免疫疗法:前景与挑战并存
近年来,一种名为铁死亡(Ferroptosis)的细胞死亡方式,作为一种新兴的抗肿瘤策略备受关注。它通过诱导肿瘤细胞内的脂质过氧化,破坏细胞膜,从而直接杀死癌细胞。更重要的是,铁死亡过程能释放特定分子,激活人体的免疫系统,尤其是T细胞,来共同攻击肿瘤,这被称为免疫原性细胞死亡(ICD)。
因此,将铁死亡诱导剂与免疫检查点抑制剂(ICB)疗法相结合,被认为是极具潜力的癌症协同治疗方案。然而,临床实践中面临一个巨大障碍:大多数实体瘤内部存在严重的缺氧微环境。这种缺氧状态不仅会抑制铁死亡的发生效率,还会上调肿瘤细胞表面的PD-L1蛋白,帮助癌细胞逃避免疫系统的追杀,从而大大削弱了联合治疗的效果。
创新纳米重塑剂:为肿瘤“供氧”,双重增效
为了攻克这一难题,沈阳药科大学与深圳大学的科研团队合作,在《细胞报告医学》(Cell Reports Medicine)上发表了一项突破性研究。他们成功开发出一种氟化前药工程化纳米重塑剂,巧妙地将铁死亡诱导剂索拉非尼(Sorafenib)与PD-L1抑制剂JQ1整合在一起。

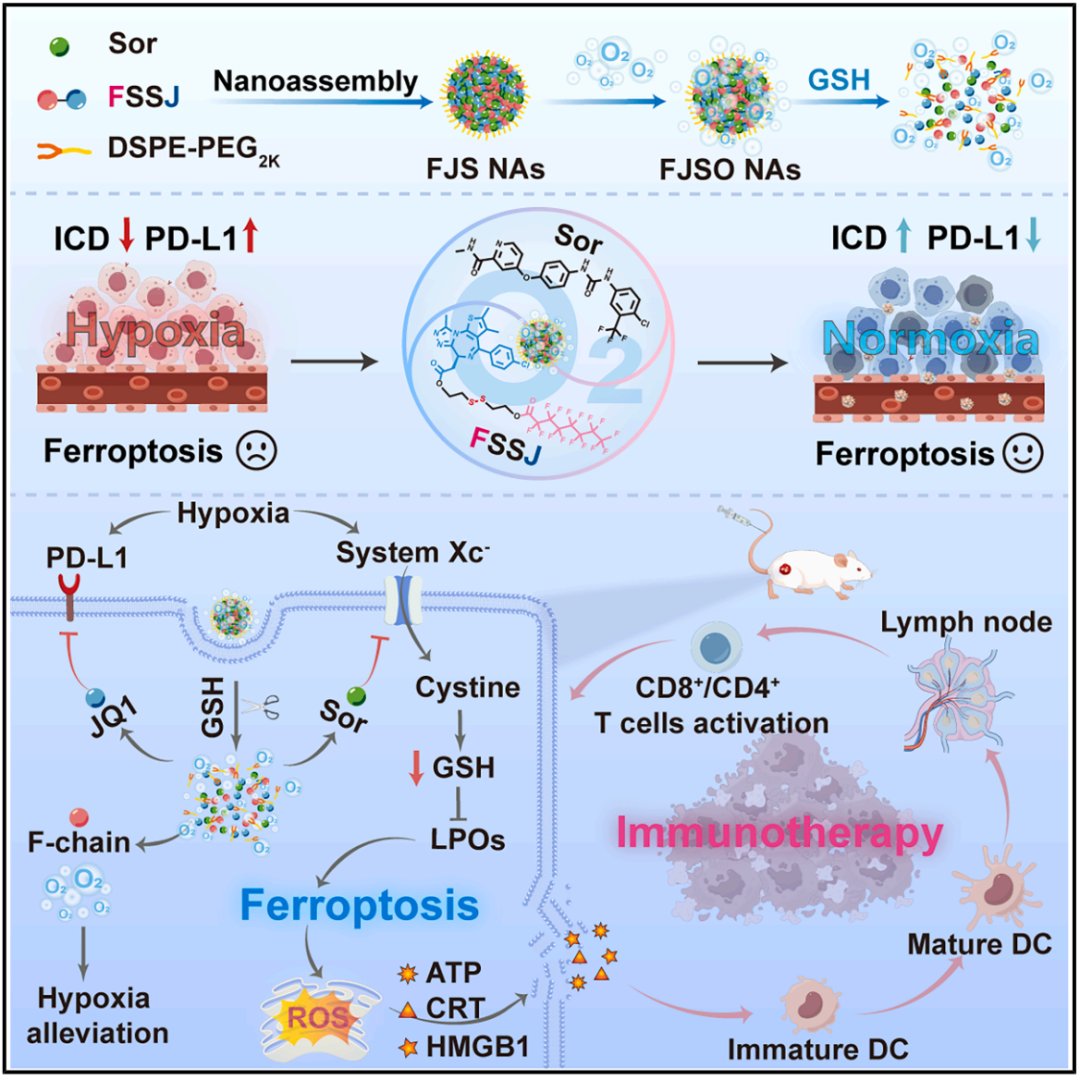
这种纳米制剂的核心优势在于其独特的氟化结构,使其具有高效的氧气溶解和携带能力。当纳米药物到达肿瘤部位后,会因为肿瘤内部的低氧环境而释放出氧气,从而精准地缓解肿瘤的缺氧状态。这一过程带来了两大协同效应:
- 增强铁死亡效率:充足的氧气显著提升了索拉非尼诱导铁死亡的杀伤效果。
- 增强免疫治疗效果:氧气供应下调了肿瘤细胞的PD-L1表达,而同步释放的JQ1则进一步阻断了PD-L1通路,双管齐下地解除了免疫抑制,使免疫细胞能更有效地识别和清除癌细胞。
如果您对该疗法或相关药物有任何疑问,可以咨询MedFind的AI问诊服务获取专业解答。
研究成果与临床前景
实验结果令人振奋,在多种实体瘤动物模型中,这种新型纳米重塑剂展现出强大的肿瘤抑制能力,并且未观察到明显的毒副作用,显示出良好的安全性。
这项研究不仅为“铁死亡-免疫联合疗法”开辟了新的方向,也为克服实体瘤治疗耐药性提供了创新的解决方案。通过重塑肿瘤微环境来增强现有疗法的效果,预示着未来癌症治疗将更加精准和高效。若您需要了解更多前沿抗癌药物信息或有购药需求,欢迎访问MedFind全球药房,我们将为您提供专业的支持与服务。





