脑胶质瘤手术切除的困境与挑战
脑胶质瘤是中枢神经系统中最常见的恶性肿瘤,以其高侵袭性、高复发率和高死亡率而著称。手术切除是治疗脑胶质瘤的首选方案,其切除程度直接关系到患者的生存期和生活质量。然而,脑胶质瘤的一大特点是其侵袭性生长,癌细胞会像树根一样沿着血管和神经纤维束渗透到正常的脑组织中,导致肿瘤与健康组织之间的边界极其模糊。
这一特性为神经外科医生带来了巨大的挑战:如果切除范围过于保守,残留的癌细胞会导致肿瘤迅速复发;而如果切除范围过大,则可能损伤到周围重要的脑功能区,引发失语、偏瘫等严重的神经功能障碍。目前临床上依赖术前磁共振(MRI)成像来规划手术,但在开颅后,“脑漂移”现象会导致影像与实际情况出现偏差。同时,像5-氨基乙酰丙酸(5-ALA)和吲哚菁绿(ICG)这类术中使用的荧光探针,由于缺乏肿瘤特异性,时常产生假阳性或假阴性结果,限制了其应用效果。面对复杂的治疗决策,获取全面的疗法信息至关重要,MedFind抗癌资讯板块为您提供最新的诊疗指南和研究进展。
追踪癌细胞的“蛛丝马迹”:定位边界的新思路
为了攻克这一难题,科学家们提出了一种全新的策略:不再仅仅观察肿瘤的宏观形态,而是去追踪癌细胞在侵袭过程中留下的“分子足迹”。复旦大学药学院李聪团队近期在《Biomaterials》上发表的综述文章,系统性地总结了这一前沿领域。研究指出,胶质瘤细胞在侵袭时,会引起周围微环境发生一系列特征性变化,这些变化可以作为开发新型影像探针的关键生物标志物。
这些标志物涵盖了多个层面:
- 分子层面:肿瘤独特的代谢方式导致局部pH值失调、乏氧、活性氧(ROS)水平升高等。
- 细胞层面:肿瘤侵袭区域的神经元会表现出过度兴奋和异常放电。
- 结构层面:癌细胞浸润会破坏血脑屏障的完整性,并引发脑水肿。
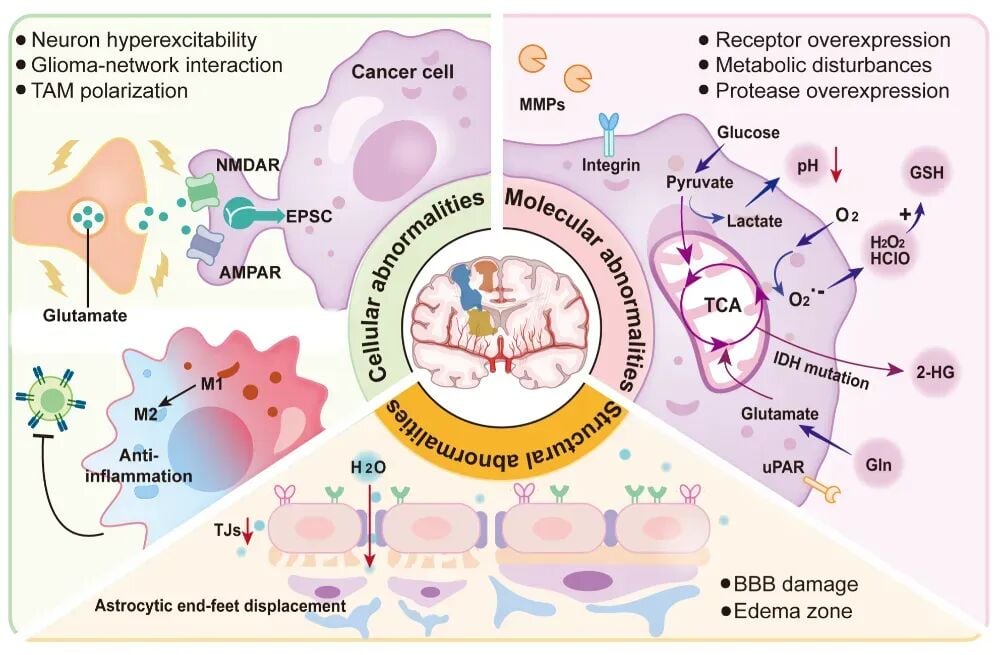
图1. 定位脑胶质瘤边界的生物标志物,跨尺度、多层次反映分子、细胞及结构异常
分子探针:点亮肿瘤边界的“导航灯”
基于上述生物标志物,研究人员正在开发新一代的“智能”分子影像探针。这些探针经过精心设计,能够特异性地识别并结合胶质瘤侵袭前沿的分子靶点,如同高精度的“导航灯”,在手术中实时点亮肉眼难以分辨的肿瘤边界。通过优化探针材料,可以显著提升其穿透血脑屏障的能力、在体内的稳定性和药代动力学特性,从而获得高灵敏度、高信噪比的成像效果,帮助医生实现更精准的切除。对于脑胶质瘤这样复杂的疾病,个体化的治疗方案尤为重要。如果您对自己的病情或治疗方案有疑问,可以尝试MedFind的AI问诊服务,获取专业的参考意见。
未来展望:从实验室到手术台的挑战与机遇
尽管分子探针在术中导航方面展现出巨大潜力,但其从实验室走向临床应用仍面临挑战。未来的研究需要克服肿瘤异质性带来的困难,例如可以发展针对多个靶点的协同成像策略。此外,将人工智能(AI)技术与多模态影像数据相结合,有望实现对肿瘤边界的动态实时重构,进一步提升手术决策的精准度。
最终,通过多学科的交叉合作,不断优化探针的生物相容性与安全性,推动其临床转化,这些高精度影像探针有望成为实现脑胶质瘤“最大范围安全切除”的关键工具,为广大患者带来新的希望。随着医学的进步,未来将有更多创新疗法问世。对于需要海外靶向药的患者,MedFind代购服务致力于提供便捷、可靠的购药渠道。