胰腺癌,因其早期症状隐匿、侵袭性强,长期以来被视为预后极差的“癌症之王”。面对有限的治疗选择和不尽如人意的疗效,患者和家属们常常感到无助。然而,随着精准医学时代的到来,基因检测为晚期癌症患者带来了新的希望。通过深入分析肿瘤的分子特征,医生能够为患者量身定制更有效的治疗方案。
胰腺癌的挑战与精准医疗的曙光
传统的胰腺癌治疗手段,如手术、化疗和放疗,虽然能在一部分患者中取得效果,但对于晚期伴有转移的患者,其疗效往往有限。在这种背景下,分子肿瘤委员会(MTB)应运而生。MTB由多学科专家组成,通过解读复杂的基因检测数据,识别可靶向的基因突变,并推荐个性化的精准治疗方案,从而显著提升治疗效果。
病例回顾:一位晚期胰腺癌患者的治疗历程
本文将详细介绍一位45岁男性晚期胰腺癌患者的治疗案例。该患者最初因黄疸就诊,被诊断为胰头肿块伴肝转移。在接受了包括吉西他滨、白蛋白结合型紫杉醇、尼妥珠单抗及质子放疗在内的多模式初始治疗后,病情曾一度稳定。然而,疾病最终进展,促使患者寻求更深层次的分子评估。
基因检测揭示新希望:BRCA2突变与HRD阳性
在疾病进展后,患者进行了全面的基因检测。结果令人振奋:检测显示其存在同源重组修复缺陷(HRD)阳性(评分为58分),并携带致病性BRCA2突变(p.T3033fs)。这些分子标志物的发现,强烈提示患者可能对PARP抑制剂和铂类药物治疗敏感。对于寻求海外靶向药代购的患者,了解这些关键的基因突变信息至关重要,因为它们直接关系到药物的选择和疗效。您可以通过MedFind海外靶向药代购服务获取所需药品。
多维度联合治疗策略:奥拉帕利、免疫疗法与HAIC
基于基因检测结果,MTB为患者制定了创新的联合治疗方案。患者开始接受PARP抑制剂奥拉帕利(Olaparib)治疗,并联合免疫治疗(替雷利珠单抗、阿替利珠单抗)以及肝动脉灌注化疗(HAIC,采用FOLFOX方案:5-氟尿嘧啶+亚叶酸钙+奥沙利铂)。这种多维度、协同作用的治疗策略,旨在从不同层面攻击肿瘤细胞,最大化治疗效果。
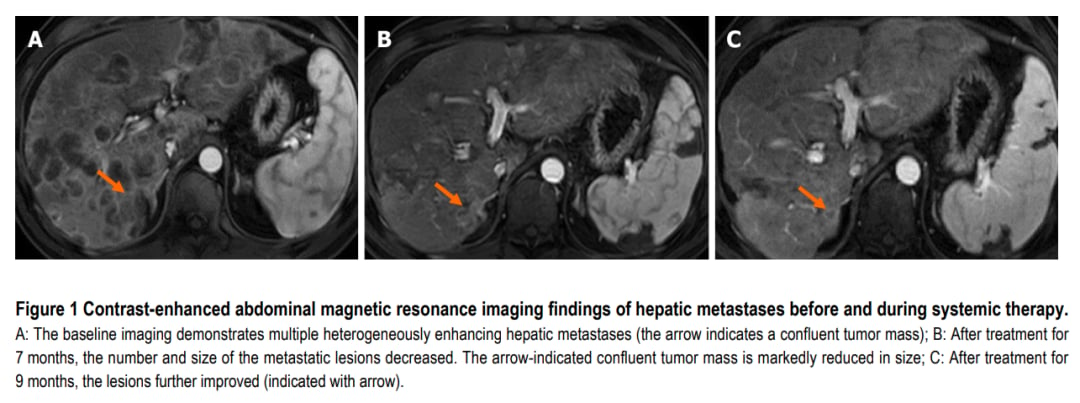
▲图1 系统治疗前及治疗期间肝转移灶增强腹部磁共振成像
显著的临床获益与讨论:治疗效果与机制探讨
在接受奥拉帕利联合免疫治疗及HAIC后,患者的肝转移灶获得了进一步的稳定并部分缩小。影像学检查显示,肝病灶显著缩小,肿瘤标志物水平也得到了有效控制。这一显著的临床获益,不仅延长了患者的无进展生存期,也为晚期胰腺癌的治疗提供了宝贵的经验。
研究表明,BRCA1/2突变会导致同源重组修复缺陷(HRD),使肿瘤细胞对PARP抑制剂(如奥拉帕利、尼拉帕利)高度敏感,通过“合成致死”机制诱导肿瘤细胞死亡。此外,BRCA2突变还可能增强肿瘤的免疫原性,提高对免疫检查点抑制剂(ICIs)的应答。PARP抑制剂与PD-L1抑制剂的联合使用,已被证实能增强抗肿瘤效果。HAIC则能局部高浓度作用于肝转移灶,进一步提升局部控制率。这种多管齐下的策略,正是患者获得成功的关键。
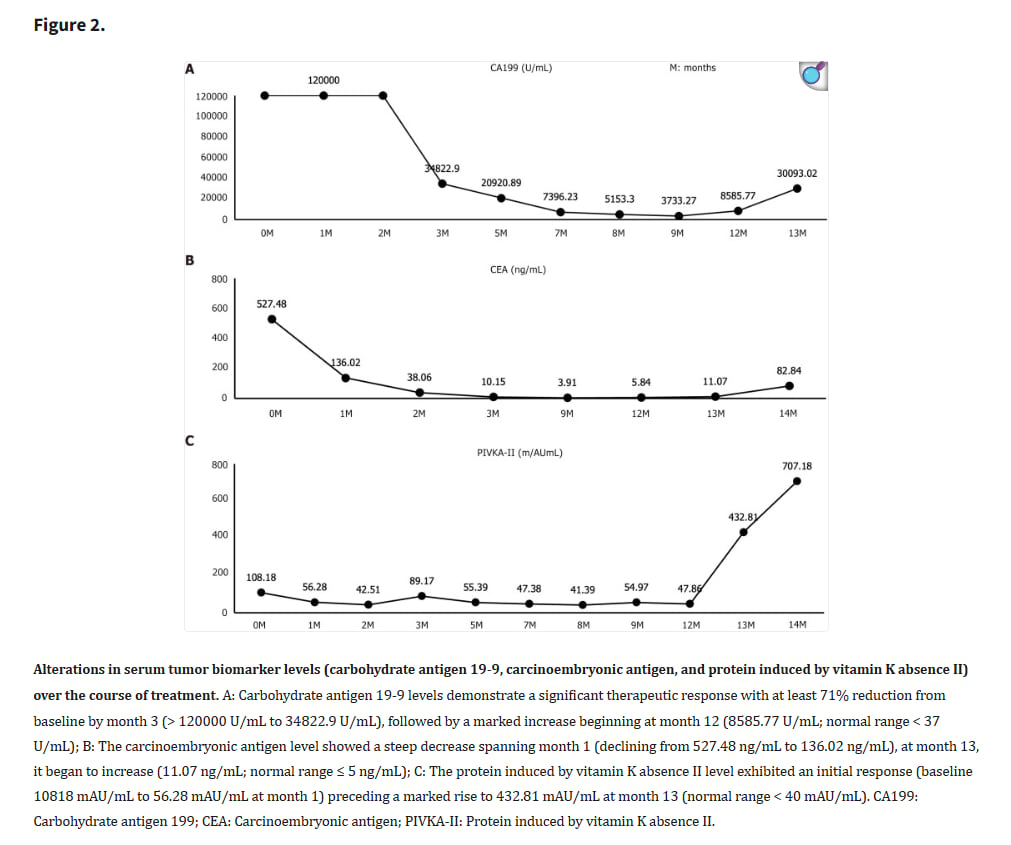
▲图2 治疗过程中血清肿瘤生物标志物水平(碳水化合物抗原 19-9、癌胚抗原和维生素 K 缺乏诱导蛋白II)的变化
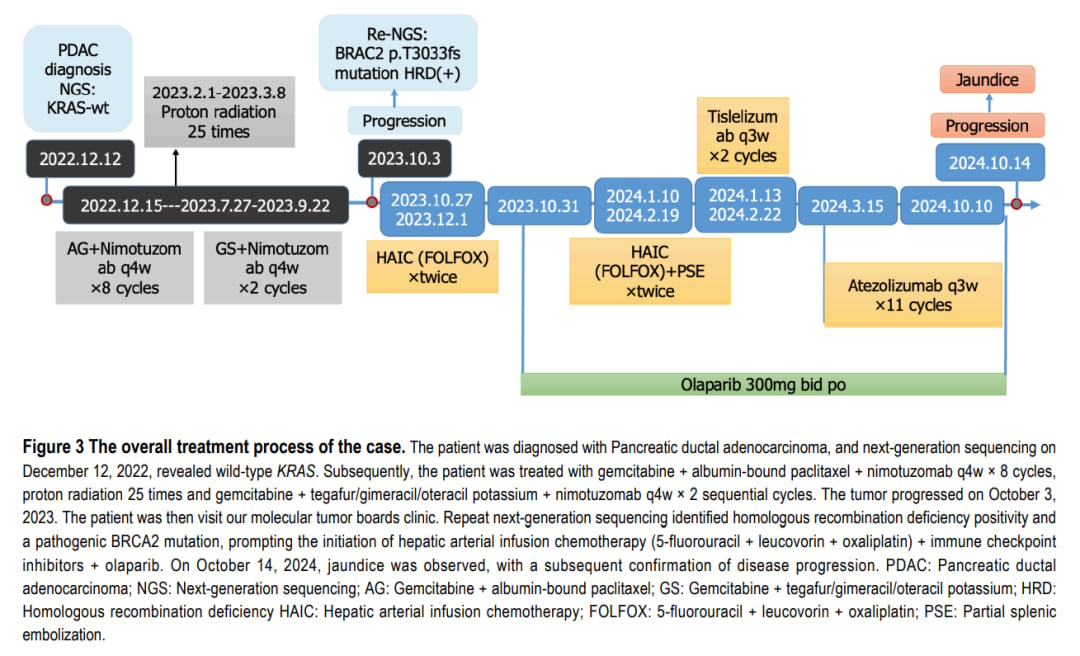
▲图3 患者整体治疗经过
分子肿瘤委员会(MTB)的关键作用
本病例再次强调了分子肿瘤委员会(MTB)在晚期胰腺癌管理中的不可替代作用。MTB通过整合基因组学见解与临床决策,为患者提供了超越传统治疗模式的个性化方案。在患者初始治疗进展后,MTB建议进行第二轮基因组测序,并巧妙地利用外周血NGS联合原始活检组织肿瘤微环境分析,克服了临床取样难题,成功发现了新的治疗机会。如果您对自己的病情有疑问,可以尝试MedFind的AI问诊服务,获取初步的专业建议。
展望未来:精准肿瘤学的挑战与机遇
尽管本病例取得了令人鼓舞的成果,但仍需认识到,多种治疗的序贯使用使得临床获益难以完全归因于单一干预措施,且治疗间的协同或拮抗作用仍需进一步研究。未来的工作应致力于扩大MTB的可及性,并在更大规模的患者队列中验证其疗效,以建立精准肿瘤学的标准化框架。同时,获取最新的药物信息和诊疗指南对于癌症患者至关重要,MedFind抗癌资讯可以为您提供帮助。





