2025年8月,国际顶尖科学期刊《细胞》(Cell)再次发布了一系列令人瞩目的研究成果,涵盖了从神经科学、病毒学到基因编辑和癌症治疗的多个前沿领域。这些突破性发现不仅加深了我们对生命奥秘的理解,更预示着未来医学和生物技术发展的无限可能。对于正在寻求最新治疗方案的癌症患者及家属而言,了解这些前沿进展至关重要。MedFind致力于为患者提供全面的抗癌资讯,包括药物信息、诊疗指南等,帮助您把握最新的科学动态。
2025年8月《细胞》期刊精选研究亮点
1. 大脑发育“分子刹车”:多发性硬化症治疗新希望
在一项开创性研究中,科学家们揭示了大脑发育中一个关键的分子“刹车”机制。这种机制控制着少突胶质细胞的成熟时机,而该细胞对修复多发性硬化症(MS)造成的神经损伤至关重要。研究发现,在MS患者体内,这个名为SOX6蛋白的“刹车”似乎停留时间过长,阻碍了脑细胞的自我修复。这项发表于《细胞》的研究为修复多发性硬化症及类似神经系统疾病的损伤提供了潜在的再生医学方法,有望“开启大脑自身的修复程序”。

2. 猴痘病毒防护:新型单克隆抗体展现强大潜力
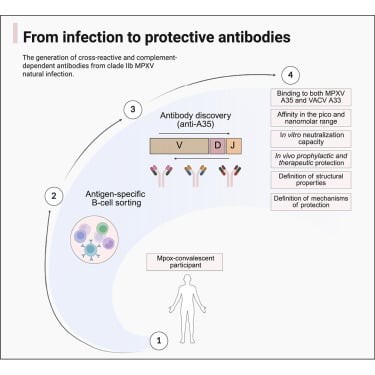
西奈山伊坎医学院的研究团队从猴痘病毒感染者体内成功分离出三种强效单克隆抗体。这些抗体特异性靶向猴痘病毒蛋白A35,在体外实验中有效阻断了病毒传播,并在动物模型中完全预防了死亡和严重疾病。这项发表在《细胞》上的研究指出,这些抗体不仅在正痘病毒家族中高度保守,且不易发生突变逃逸,预示着它们有望成为预防或治疗猴痘病毒感染的候选药物,为应对此类病毒威胁提供了新的免疫疗法策略。
3. 植物免疫新发现:番茄植物的天然防御平衡器
来自图宾根大学和霍恩海姆大学的研究团队在番茄植物中发现了一种前所未有的天然Systemin拮抗剂——antiSys。信号肽Systemin是番茄植物抵御食草动物的关键防御信号,但过度激活会影响植物生长。研究表明,antiSys能有效抑制Systemin受体SYR1,防止防御系统过度反应,从而维持植物生长与防御之间的精妙平衡。这项发表于《细胞》的研究,通过CRISPR/Cas9技术培育的突变体证实了antiSys的重要性,拓展了我们对植物免疫机制的认知。

4. “X光眼”透视器官:中国科学家实现组织透明化革命
中国清华大学生物医学工程学院团队研发的“基于离子液体溶剂的玻璃化跨尺度生物结构体积检测”(VIVIT)技术,实现了让大脑、心脏等复杂器官像玻璃一样透明,同时完整保留其精细组织结构。这项发表于《细胞》的突破性技术,利用特殊的离子液体进行玻璃化处理,解决了传统组织透明化方法中样本皱缩、荧光信号损耗等难题,实现了形变幅度在1%以内的跨尺度观测,为生物医学研究提供了前所未有的“X光眼”。

5. 基因治疗新纪元:新型RNA编辑工具降低风险
基因治疗在校正致病基因错误方面前景广阔,但DNA的永久性改变存在风险。耶鲁大学研究人员开发出一种新型RNA编辑工具家族——R-IscB和R-Cas9,它们从广为人知的CRISPR-Cas9基因编辑工具中“发掘”出靶向RNA的活性。这项发表于《细胞》的研究表明,在信使RNA(mRNA)层面进行编辑,可避免DNA的永久性改变,显著降低风险。这些“RNA编辑的瑞士军刀”有望用于干扰mRNA功能、切割销毁目标mRNA或修正编码错误,为更安全的基因治疗开辟了道路。

6. AI机器人赋能农业:基因组编辑加速杂交育种
中国科学院遗传与发育生物学研究所的科学家们,通过基因编辑技术与人工智能机器人相结合,开发出“基于人工智能机器人的基因组编辑系统”(GEAIR)。这项发表于《细胞》的研究,通过CRISPR-Cas9靶向调控花器发育基因(如番茄中的GLO2),成功培育出适合机器人授粉的新型花朵,解决了杂交育种中人工授粉耗时耗力的瓶颈。这一“作物-机器人协同设计”新模式,有望大幅提升农业效率,加速高产、强壮作物的培育。

7. 精准基因组编辑里程碑:百万碱基规模DNA操纵
中国科学院遗传与发育生物学研究所高彩霞教授团队,开发出两种新型基因组编辑技术——可编程染色体工程技术(PCE系统)。这项发表于《细胞》的研究,在高等生物(尤其是植物)中实现了从千碱基到兆碱基规模的多类型精准DNA操纵。通过创新性地改造Cre-Lox系统,包括非对称Lox位点设计、AiCErec重组酶工程以及Re-pegRNA无疤痕编辑策略,该团队克服了长期限制,为基因组研究和育种带来了革命性突破。

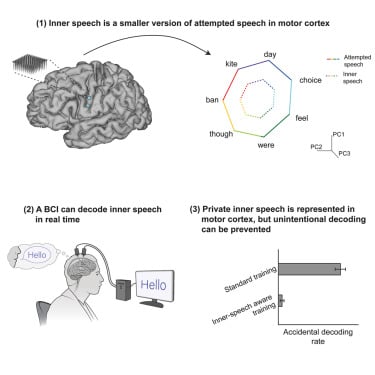
8. 脑机接口新突破:默念即可“说话”,守护内心隐私
一项发表于《细胞》的最新研究,在脑机接口(BCI)领域取得重大突破。科学家们不仅精准定位了大脑中负责“内部言语”(inner speech)的区域,还成功解码了人们默念时的脑活动,最高准确率达74%,甚至能从12.5万个词汇中解读出想象的句子。更重要的是,该系统具备“心理隐私”保护功能。这项技术对肌萎缩侧索硬化症(ALS)或中风导致严重瘫痪的患者意义重大,使他们仅凭“想”就能实现更轻松、自然的交流。
9. 癌症恶病质新机制:阻断脑-肝通讯或可逆转体重下降
癌症相关恶病质(CAC)是一种导致近三分之一癌症相关死亡的代谢综合征,表现为严重的体重减轻和肌肉耗竭。魏茨曼科学研究所和MD安德森癌症中心的研究人员在《细胞》上发表研究,发现癌症恶病质的一个重要原因是大脑与肝脏之间的通讯被破坏。当迷走神经活动失调时,会导致肝脏代谢受损,进而引发恶病质。通过对右颈迷走神经进行干预,可减弱CAC进展,改善小鼠健康状况和生存率。对于面临癌症恶病质等复杂并发症的患者,及时获取专业的AI问诊服务,或寻求海外靶向药代购服务,可能为治疗带来新的希望。

10. AI驱动蛋白质设计:增强T细胞免疫疗法效能
一篇发表于《细胞》期刊的论文重点介绍了研究人员如何利用基于人工智能(AI)的计算蛋白质设计,创造出一种新型合成配体来激活Notch信号通路。Notch信号是T细胞发育和功能的关键驱动因素。哈佛医学院的研究团队利用Rosetta蛋白质设计工具,成功设计出可溶性Notch激动剂,有效促进了T细胞的生产。这些发现为优化临床T细胞免疫疗法生产和推进癌症免疫治疗开发提供了广阔前景。