以顺铂(CDDP)为基础的化疗是晚期胆管癌的主要治疗方法,但临床疗效常受限于耐药性的产生。近日,吉林大学樊钟琦团队在《Journal of Hepatology》发表了一项重要研究,揭示了胆管癌细胞对顺铂产生耐药性的新机制,为开发更有效的治疗策略提供了新的方向。
该研究题为“Cisplatin-induced Disruption of Mitochondrial Divisome Leads to Enhanced Cisplatin Resistance in Cholangiocarcinoma”,发表于2025年4月4日。研究团队发现,顺铂会破坏线粒体分裂体(MD),而线粒体分裂体是调节线粒体分裂的关键结构。这种破坏导致了胆管癌细胞对顺铂的耐药性增强。
研究表明,顺铂(CDDP)会显著破坏多种MD成分,例如增加F-肌动蛋白的外周聚合,降低内质网(ER)与线粒体的共定位,以及INF2的降解。这些变化促进了线粒体融合,从而导致胆管癌细胞对顺铂产生抵抗。研究进一步发现,INF2在CDDP耐药中起着关键作用,其降解主要通过蛋白酶体途径和SEC62介导的吞噬作用发生。抑制这些通路可以增加胆管癌细胞对顺铂的敏感性。这一发现提示,靶向INF2可能是克服胆管癌顺铂耐药性的一个潜在策略。

胆管癌(CCA)是一种起源于胆管上皮细胞的恶性肿瘤,其发病率和死亡率在全球范围内呈上升趋势。晚期胆管癌患者的五年生存率较低。目前,顺铂联合吉西他滨是晚期胆管癌的标准一线化疗方案。然而,由于胆管癌肿瘤微环境的特殊性,免疫检查点抑制剂的疗效有限。克服顺铂耐药性是提高胆管癌治疗效果的关键。
该研究的独特之处在于,它关注了药物暴露后肿瘤细胞的适应性变化。线粒体在细胞凋亡中起着重要作用,在应激条件下会发生动态形态重塑。研究发现,顺铂会在耐药的胆管癌细胞中诱导线粒体融合,而抑制线粒体融合可以使这些细胞对顺铂重新敏感。这表明线粒体融合是顺铂耐药的重要机制。
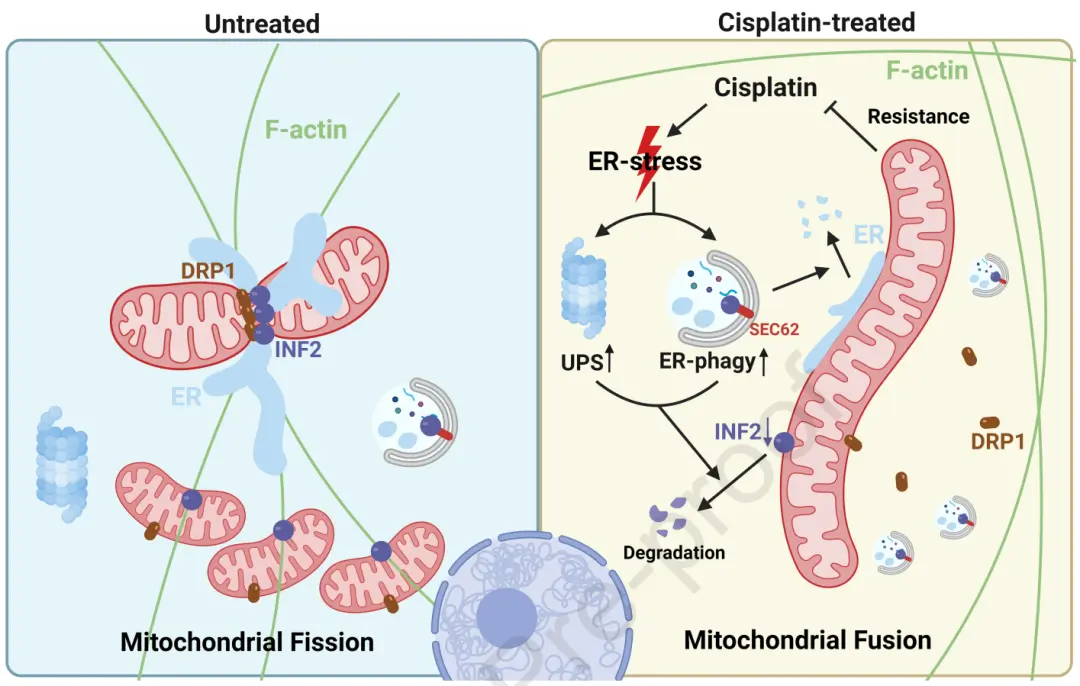
机理模式图(图源自Journal of Hepatology)
线粒体分裂体(MD)是一个复杂的多组分系统,负责控制线粒体分裂。该系统以动力蛋白相关蛋白1 (DRP1)及其外膜受体为核心。细胞骨架元件、内质网(ER)和肌动蛋白结合蛋白(如INF2)也参与了线粒体分裂的调控。研究发现,顺铂不仅会形成DNA加合物,还会破坏细胞骨架,从而改变MD的功能,促进线粒体融合,导致耐药性。
该研究还发现,基线INF2表达水平高的胆管癌患者预后较差。顺铂诱导的INF2降解通过蛋白酶体和SEC62介导的ER吞噬是胆管癌细胞中线粒体超融合和化疗耐药的关键驱动因素。这些发现为克服化疗耐药性提供了新的策略,即靶向线粒体形态。此外,该研究强调,在治疗过程中,应关注肿瘤蛋白或细胞器功能的动态变化,而不是仅仅分析静态的肿瘤状态。这项工作为针对胆管癌和其他具有类似耐药机制的恶性肿瘤的线粒体靶向治疗方法奠定了基础。
正在寻找胆管癌靶向药或仿制药? MedFind 提供海外药品代购服务,帮助您获取更多治疗选择。您还可以通过 MedFind AI问诊 获得个性化的医疗建议,并浏览 MedFind抗癌资讯 了解最新的药物信息和诊疗指南。
参考信息:
https://www.journal-of-hepatology.eu/article/S0168-8278(25)00219-3/fulltext