癌症治疗的新前沿:新表位预测与个性化免疫疗法
随着癌症治疗进入精准医学时代,免疫疗法,尤其是基于患者个体特征的个性化癌症免疫治疗,正成为攻克肿瘤的关键方向。这种疗法的核心在于识别癌细胞特有的“身份标记”——新表位(Neoepitope),并利用这些标记来训练或激活患者自身的免疫系统,从而精准打击癌细胞。然而,从海量的基因突变数据中准确筛选出真正能激活免疫反应的有效新表位,一直是生物信息学和临床研究中的巨大挑战。
本文将深入解读清华大学张学工和魏磊团队在《Genome Medicine》上发表的最新研究成果:一种名为NeoGuider的新型生物信息学预测方法。NeoGuider通过引入先进的特征转换技术,显著提高了新表位预测的准确性和效率,为癌症患者的个性化治疗方案设计,如新抗原疫苗和T细胞疗法,提供了更可靠的技术支撑。对于正在寻求前沿治疗方案的癌症患者及其家属而言,了解这类技术进展,有助于把握未来治疗的方向和选择。
一、理解新表位与新抗原:免疫治疗的“靶点”
要理解NeoGuider的价值,首先需要明确新表位和新抗原的概念:
1. 新抗原(Neoantigen)的产生
癌细胞由于基因组不稳定,会发生大量的基因突变。这些突变可能导致细胞产生异常的蛋白质。当这些异常蛋白质被分解成小片段的多肽时,它们被称为新抗原。这些新抗原是癌细胞独有的,在正常细胞中不存在。
2. 新表位(Neoepitope)的作用
新抗原多肽随后会与细胞表面的主要组织相容性复合体(MHC,在人类中称为HLA)结合,并将这些多肽片段呈递到癌细胞表面。这些被呈递的、能够被宿主免疫系统(特别是T细胞)识别的多肽片段,就是新表位。
理论上,一旦免疫系统中的T细胞识别出这些新表位,就会启动免疫反应,杀死携带这些标记的癌细胞。然而,在实际的肿瘤微环境中,这种天然的免疫刺激往往不足以清除肿瘤,导致癌症进展。个性化免疫疗法(如新抗原疫苗)的目的,就是通过人工手段,将最有效的、免疫原性最强的新表位注射回患者体内,以“教育”和“增强”T细胞的杀伤力。
二、个性化免疫治疗的基石:精准预测的挑战
设计个性化免疫疗法的第一步,是利用患者的肿瘤测序数据(如全外显子组测序WES和RNA测序RNA-seq),识别出所有潜在的新表位候选序列。然而,这一过程面临两大核心挑战,也是现有预测方法准确性有限的主要原因:
挑战一:非线性问题(Non-linearity)
新表位的“免疫原性”(即它能多大程度地激活T细胞)受到多种复杂特征的影响,包括它与MHC分子的结合强度、结合稳定性、在细胞内的表达量,以及T细胞受体(TCR)的识别能力等。这些特征与最终免疫原性之间的关系往往是非线性的,传统的线性模型难以准确捕捉这种复杂关系。
挑战二:分类不平衡问题(Classification Imbalance)
在数以万计的突变多肽中,真正具有高免疫原性、能有效激活T细胞的“有效新表位”(正例)是极少数的。即使是大型数据集,正例样本也极其稀少。这导致机器学习模型在训练时很容易过度拟合这些稀少的正例数据,从而在面对新患者数据时,预测准确性大幅下降。
三、NeoGuider:基于先进特征转换技术的突破
为了解决上述两大挑战,清华大学团队开发了NeoGuider生物信息学框架。NeoGuider的核心创新在于其采用了一种监督特征转换方法,旨在将复杂的原始特征转化为更具解释性和预测力的免疫原性对数概率。
1. 核心机制:监督特征转换
NeoGuider的核心转换过程包括两个关键步骤:
- 概率估计(基于核密度估计): 首先,NeoGuider使用自定义的核密度估计方法,对每个原始特征(如MHC结合强度)进行概率估计,评估该特征值出现在免疫原性新表位中的可能性。
- 中心保序回归(Centered Isotonic Regression): 随后,通过中心保序回归技术,将每个原始特征值映射到一个免疫原性的对数概率上。
这种转换的精妙之处在于,它将原本复杂的、非线性的特征关系,转化成了可以输入到传统机器学习分类器(如逻辑回归)中的、更易于处理的概率值。这不仅解决了非线性问题,还通过概率转换,有效缓解了分类不平衡导致的模型过度拟合。
NeoGuider默认使用5个关键的免疫原性相关特征进行预测,包括:肽类主要组织相容性复合体(pMHCs)的结合强度、结合亲和力、结合稳定性、含量以及TCR识别能力。但其灵活的设计也允许用户根据需要输入其他特征进行优先排序。

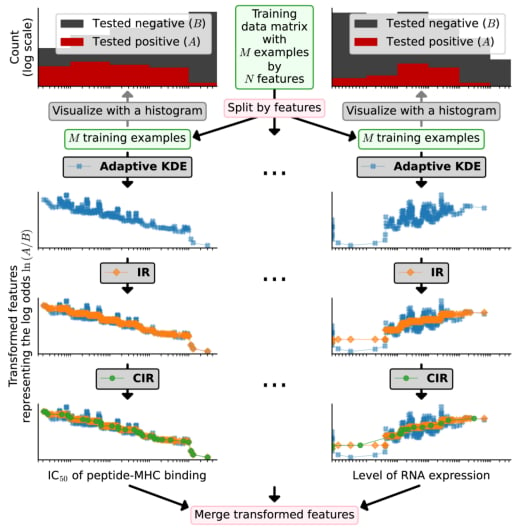
图1. 将特征转换为相应的对数概率的可视化。
2. NeoGuider的工作流程
NeoGuider被设计为一个完整的生物信息学工作流,它能够接受多种类型的测序数据(如FASTQ、FASTA和表格文件),并自动完成从原始测序数据到最终新表位候选序列优先排序的全过程。这使得研究人员和临床机构能够更便捷地应用这一先进的预测工具。
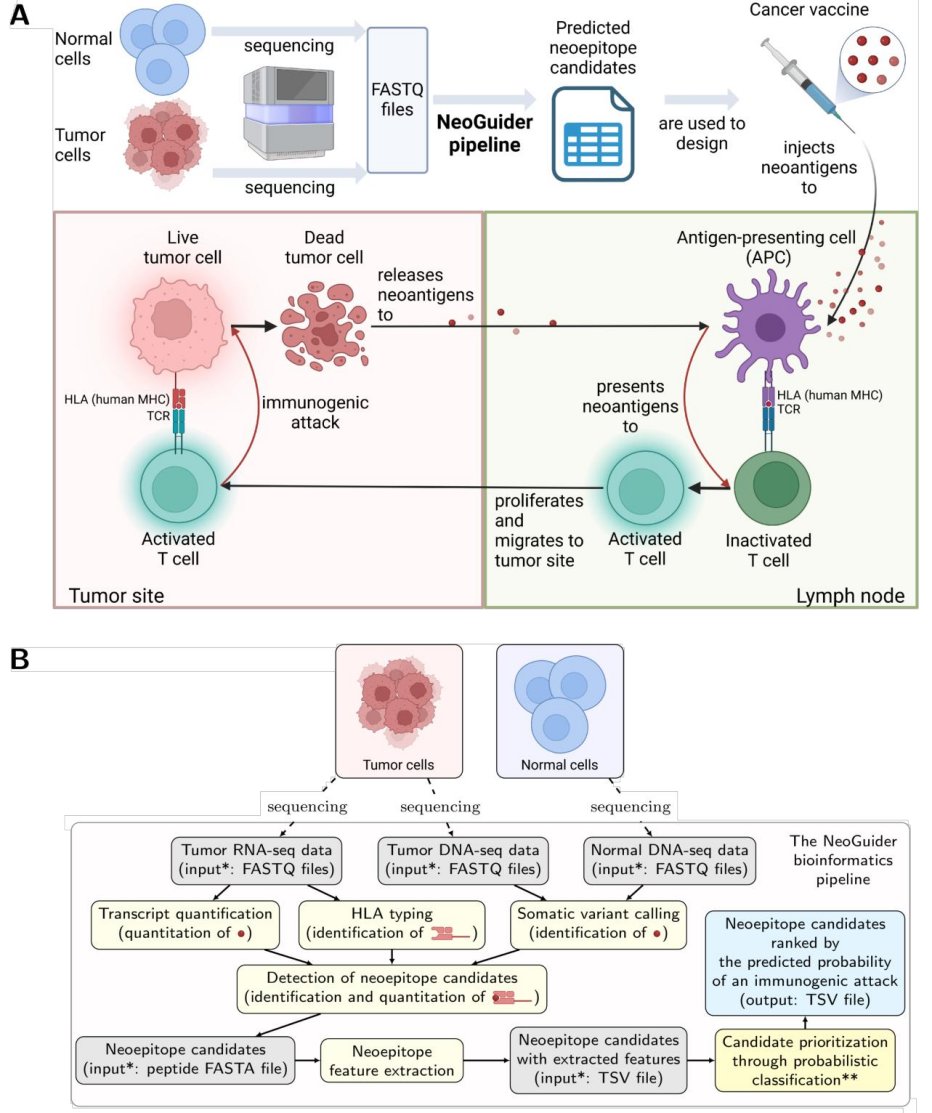
图2. NeoGuider新表位预测流程概述。
四、性能验证:NeoGuider优于现有主流方法
研究团队在多个独立的、权威的验证数据集上对NeoGuider的性能进行了严格的基准测试,并将其与目前最先进的新表位预测方法(如TESLA团队的方法、MuPeXI、DeepHLApan、MixMHCpred、netMHCpan等)进行了对比。
1. 在新表位检测和优先排序任务中的优势
在从测序数据中检测和优先排序新表位候选物的任务中,NeoGuider在TESLA(Tumor Antigen Selection Alliance)数据集上的表现显著优于TESLA联盟中的其他团队。研究结果显示,NeoGuider的TFA-mean(综合评估指标,包括前20名免疫原性分数TTIF、分数排序FR、精密度-召回曲线下面积AUPRC的平均值)普遍高于其他方法。
特别是在与TSNAD v2.0的比较中,NeoGuider在多名患者中表现出显著提升,获得了更高的True值和准确性,这表明NeoGuider能够更有效地从复杂的基因组数据中“捞出”真正的有效抗原。
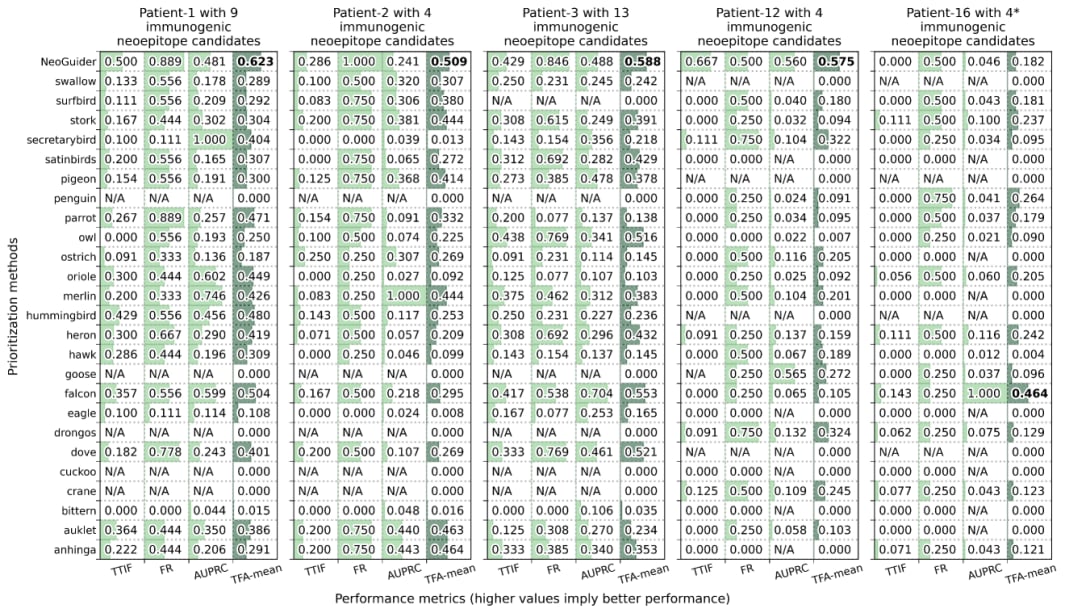
图3. NeoGuider在TESLA研究中的新表位候选序列检测和优先排序表现。
2. 在已检测候选序列优先级排序中的强劲表现
在针对已检测到的新表位候选序列进行优先级排序的独立评估中,NeoGuider同样展示了强劲的性能。在AUC-ROC(受试者工作特征曲线下面积)这一衡量分类器性能的关键指标上,NeoGuider的表现均优于MuPeXI 1.2和DeepHLApan等主流工具。
AUC-ROC值越高,意味着该方法在区分“免疫原性新表位”和“非免疫原性多肽”方面的能力越强。NeoGuider的优越性证明了其特征转换技术在提升预测准确性方面的核心价值。
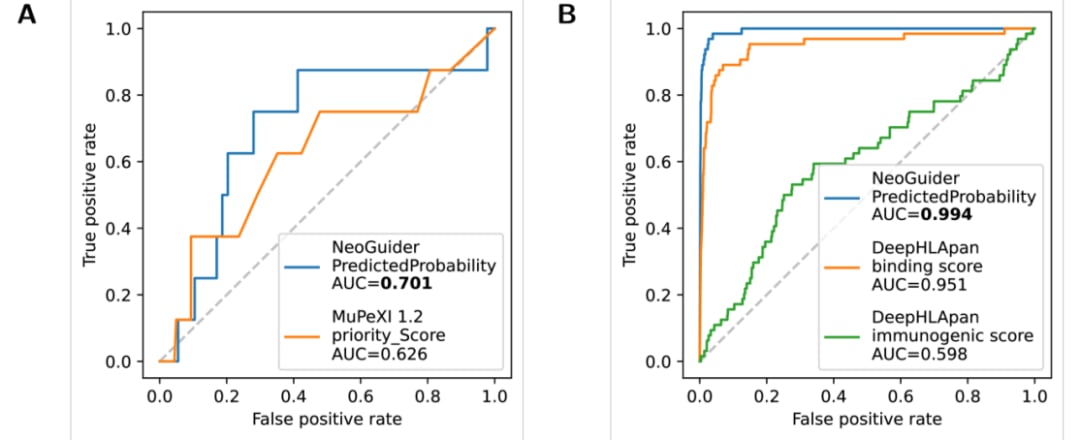
图4. NeoGuider与MuPeXI 1.2和DeepHLApan的AUC-ROC比较。
3. 特征转换技术的普适性
研究还强调,NeoGuider所采用的特征转换技术不仅对NeoGuider自身的模型有效,还能显著提升多种传统机器学习分类器(如逻辑回归LR)在筛选新表位时的性能。这种性能提升在TESLA和HiTIDE等完全独立的队列中都得到了验证,表明该转换方法具有良好的普适性和推广性,可以应用于更广泛的生物信息学分析场景。
五、NeoGuider对癌症患者的临床意义
NeoGuider这类先进的生物信息学工具,虽然是幕后技术,但其进步对癌症患者的治疗选择具有深远的临床意义:
1. 提高新抗原疫苗的成功率
新抗原疫苗是目前个性化免疫治疗中最受关注的领域之一。疫苗的有效性直接取决于其所包含的新表位是否真正具有免疫原性。NeoGuider能够更精准地筛选出“最佳”的抗原序列,这意味着未来新抗原疫苗的设计将更加高效,有望显著提高疫苗的临床响应率。
2. 优化T细胞疗法的靶点选择
对于T细胞疗法(如TCR-T细胞疗法),准确识别肿瘤特异性新表位是设计T细胞受体(TCR)的关键。NeoGuider的精确预测可以帮助研究人员和临床医生选择最合适的靶点,从而提高T细胞疗法的特异性和安全性。
3. 推动个性化治疗方案的普及
目前,个性化免疫治疗的成本和时间投入仍然较高。NeoGuider作为一种高效、准确的生物信息学框架,有助于缩短从测序到方案设计的时间,降低计算成本,从而加速个性化治疗方案从实验室走向临床,让更多患者有机会接受最前沿的治疗。
六、如何获取前沿癌症治疗方案与药物?
对于希望了解或参与基于新表位预测的个性化免疫治疗的患者来说,准确的诊断和专业的咨询至关重要。这通常涉及复杂的基因检测(WES/RNA-seq)和生物信息学分析。
- 专业咨询与方案解读: 癌症治疗方案的制定是一个高度个体化的过程。患者需要专业的医学指导来解读复杂的基因检测报告,并了解如NeoGuider这类技术如何影响其潜在的治疗选择。MedFind提供AI辅助问诊服务,帮助患者理解前沿的临床研究和治疗进展,包括个性化免疫治疗的适用性。
- 药物获取渠道: 虽然NeoGuider本身是预测工具,但其最终目的是辅助设计新抗原疫苗或选择免疫检查点抑制剂等药物。许多前沿的抗癌药物,尤其是在海外获批的新药,可能尚未在中国大陆上市。患者可以通过合规的国际渠道获取所需的抗癌药物。
- 关注临床研究进展: 许多基于新表位预测的个性化疫苗或T细胞疗法仍在临床试验阶段。患者应持续关注最新的临床研究信息,以便在第一时间抓住参与试验的机会。
七、总结与展望
清华大学张学工/魏磊团队开发的NeoGuider,代表了新表位预测技术领域的一项重要突破。通过创新的监督特征转换方法,NeoGuider成功解决了现有方法在处理非线性和分类不平衡问题上的局限,显著提高了新表位候选序列检测和优先排序的准确性。
这项研究成果不仅在生物信息学层面具有重要的学术价值,更重要的是,它为改进基于新表位的癌症免疫治疗设计提供了强大的工具。随着NeoGuider等高精度预测工具的普及,未来癌症患者将能够获得更精准、更有效的个性化抗癌方案。对于寻求最新治疗选择的患者,建议通过专业平台如MedFind获取权威药物信息、治疗方案解读与临床研究资讯,确保治疗决策基于最新的科学证据。
(注:NeoGuider的开源代码地址已公开,方便全球研究人员使用和验证。)