MYCN基因:从正常发育到肿瘤驱动
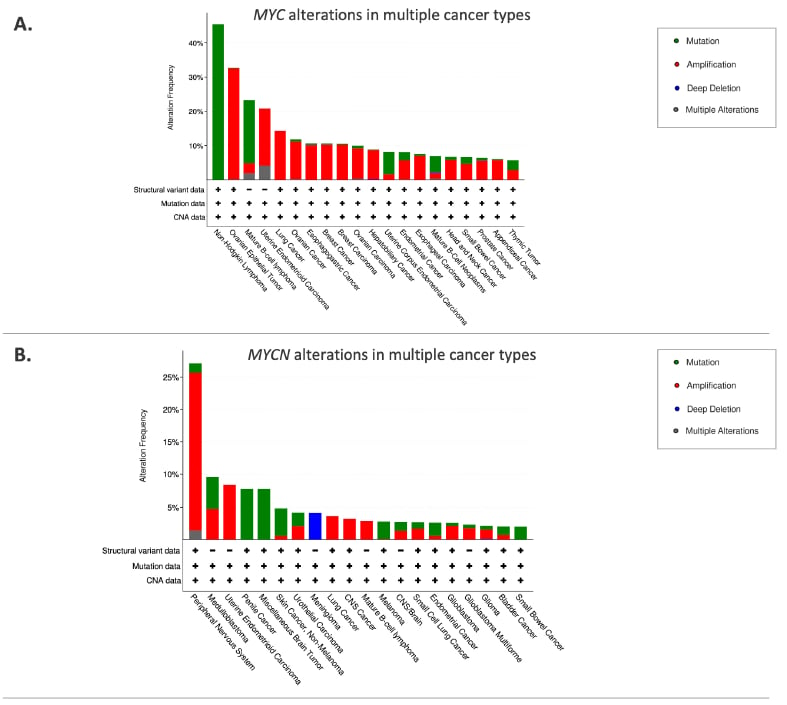
MYCN基因是MYC家族“癌基因”的一员。在儿童的正常发育过程中,MYCN在神经系统的健康成长中扮演着至关重要的角色,它指导神经细胞何时增殖、何时分化成熟。然而,在某些癌症中,会发生一种称为“基因扩增”的遗传错误,导致细胞内出现大量MYCN基因的额外拷贝。这些过量的基因会产生海量的MYCN蛋白,向细胞发送持续的“生长”信号,阻止其正常分化并促使其失控分裂,最终形成肿瘤。
MYCN的异常表达与多种儿童脑肿瘤的发生发展密切相关,并且其扩增状态是评估患者风险和预后的关键因素。通常,MYCN水平越高的肿瘤,其侵袭性也越强。
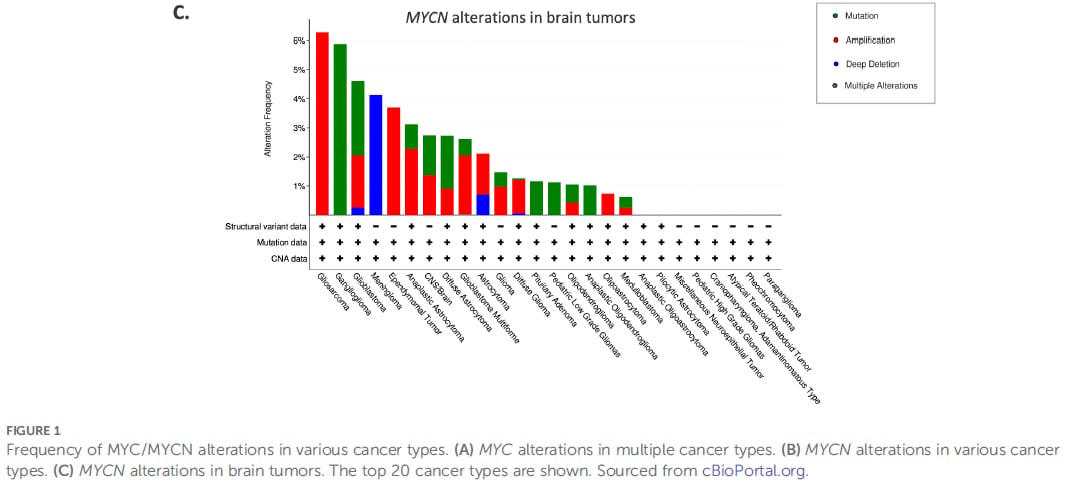
MYCN扩增在哪些儿童脑肿瘤中是关键因素?
MYCN扩增并非在所有儿童脑肿瘤中都存在,但一旦出现,它就是肿瘤侵袭性的重要标志。以下是几种与MYCN变异密切相关的儿童脑肿瘤:
- 神经母细胞瘤: 这是儿童最常见的颅外实体瘤。约22%的神经母细胞瘤病例中存在
MYCN基因扩增,这是预测不良预后的最重要因素之一。 - 髓母细胞瘤: 作为儿童最常见的恶性脑肿瘤,MYCN扩增尤其见于其SHH亚型,与较差的预后相关,特别是当与其他基因突变(如TP53)同时存在时。
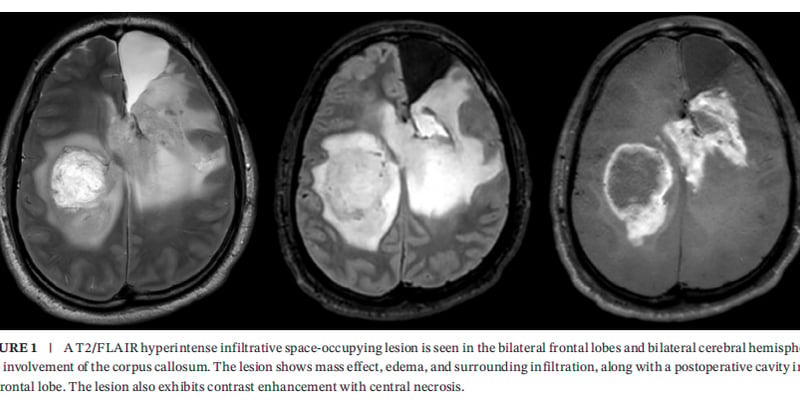
- 高级别胶质瘤: 在这类侵袭性脑肿瘤中,MYCN扩增定义了一个特定的高风险分子亚型,常见于年龄较小的患儿。
- 不典型畸胎样/横纹肌样肿瘤 (ATRT): 在这种罕见且极具侵袭性的肿瘤的ATRT-SHH亚型中,MYCN的表达显著上调,成为驱动肿瘤生长的关键力量。
- 其他肿瘤: 在松果体母细胞瘤、部分脊髓室管膜瘤等其他罕见儿童脑肿瘤中,也发现了MYCN异常表达或扩增的关键作用。
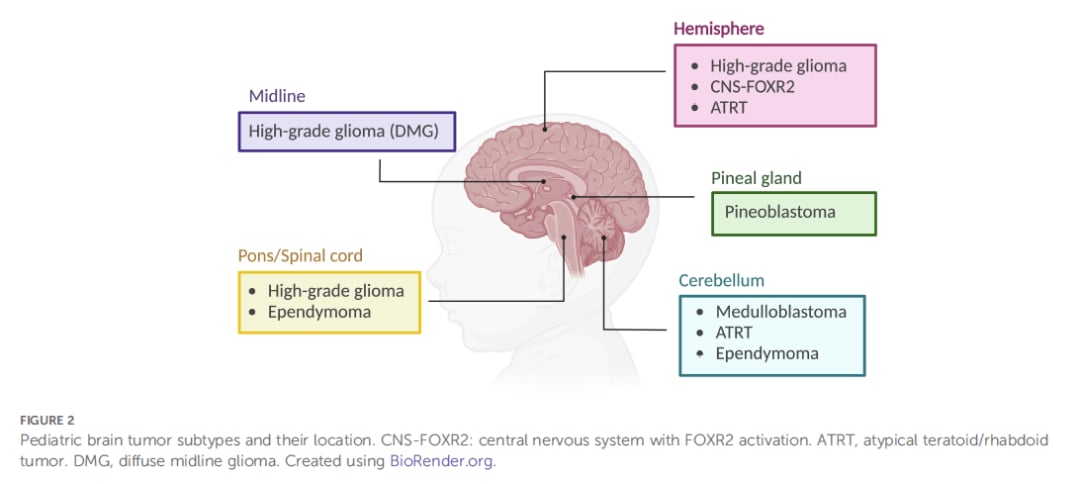
靶向MYCN:挑战与希望并存的治疗策略
几十年来,MYCN一直被视为“不可成药”的靶点。其蛋白结构缺乏一个清晰的“口袋”让药物分子结合,这使得直接抑制其功能变得异常困难。然而,科学家们正通过巧妙的间接策略,旨在瓦解MYCN的功能,并已取得初步进展。
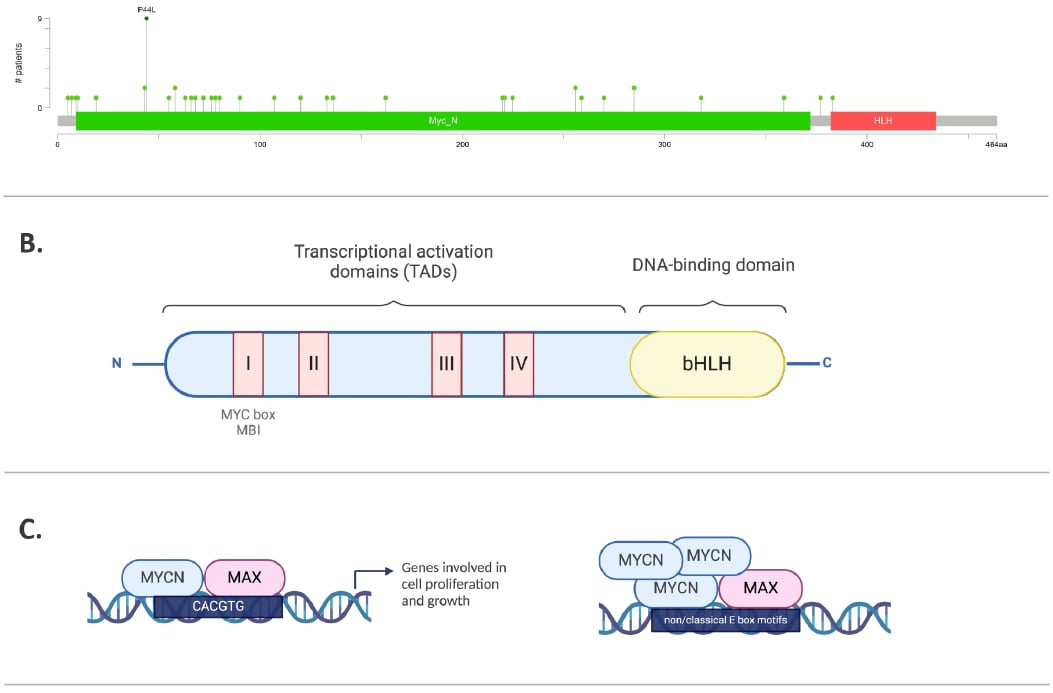
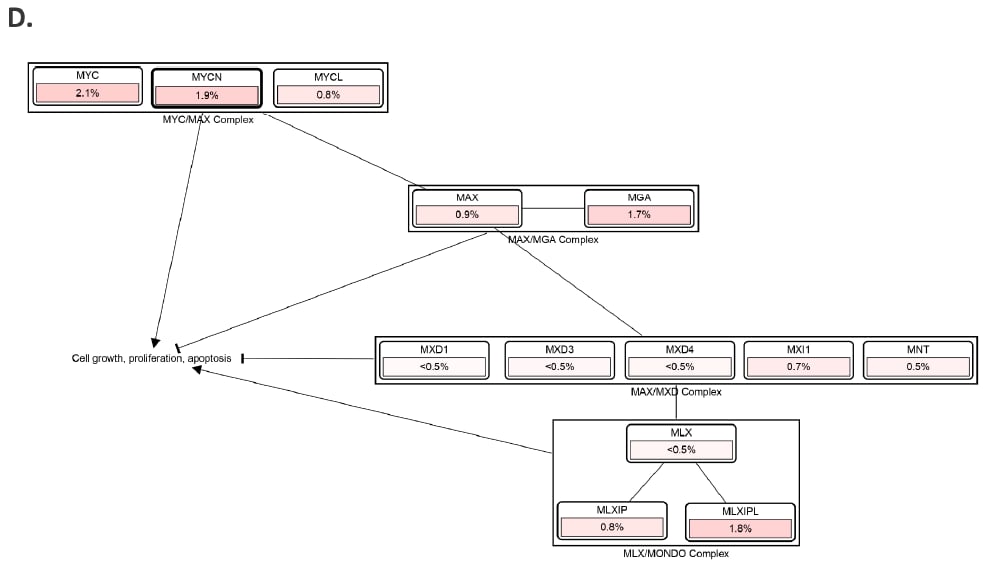

1. BET抑制剂
这类药物(如JQ1)并不直接攻击MYCN蛋白,而是靶向一种名为BET的“阅读器”蛋白(如BRD4)。BET蛋白对于开启MYCN基因至关重要。通过阻断这些阅读器,可以有效降低癌细胞中MYCN的水平。
2. 极光激酶A (Aurora-A) 抑制剂
极光激酶A等蛋白如同MYCN的“保镖”,保护它不被细胞内的机制降解。像阿立塞替 (Alisertib) 这样的药物能够抑制极光激酶A,使MYCN蛋白失去保护,从而被降解清除。
3. CDK抑制剂
另一种策略是靶向将MYCN基因转录为蛋白的细胞机器。例如,CDK7抑制剂在临床前模型中显示出潜力,它能选择性地关闭癌细胞中过度活跃的转录过程。
虽然直接靶向MYCN的药物仍在研发中,但了解这些前沿策略对于制定综合治疗方案至关重要。如果您希望获得关于您孩子病情的个性化分析或想了解更多前沿疗法,可以尝试使用MedFind的AI问诊服务,获取专业的第二诊疗意见。
结语
尽管MYCN扩增给多种儿童脑肿瘤的治疗带来了巨大挑战,但科研和医疗领域正在不断进步。针对MYCN的创新间接靶向策略为治疗开辟了新的道路。对于正在艰难抗癌的家庭而言,持续关注这些前沿进展至关重要。深入了解孩子肿瘤的分子驱动因素,将有助于您与医疗团队更充分地沟通,共同探讨所有可能的治疗选择。