
肾透明细胞癌(ccRCC)是肾癌中最常见的亚型,约占所有病例的80%。这种癌症侵袭性强,且超过三成患者在确诊时或后续病程中会发生转移,这是导致预后不佳的主要原因。尽管现有多种抗癌药物用于治疗ccRCC,但整体疗效仍有提升空间。因此,深入揭示ccRCC的发病机制,精准识别关键风险基因,对于开发新的靶向治疗策略和实现早期诊断至关重要。
传统方法的局限性与强化学习的突破
癌症的发生发展与驱动基因突变的累积息息相关。然而,传统的癌症风险基因识别方法往往依赖于基因的突变频率。这种方法面临挑战,例如某些关键驱动基因(如PIK3CA)在ccRCC患者中的突变频率可能很低(低于5%),难以被有效识别。此外,癌症的遗传背景具有高度异质性,不同患者的突变模式差异显著,这限制了基于突变频率或无监督学习方法的准确性和泛化能力。监督学习方法虽然效果较好,但需要大量已知的高置信度风险基因作为训练样本,而目前明确的ccRCC风险基因数量有限,制约了其应用。
为应对这些挑战,来自西北工业大学、天津大学及四川大学的研究团队联合开发了一种基于深度强化学习的癌症风险基因识别新方法——RL-GenRisk,并成功应用于肾透明细胞癌的风险基因挖掘。这项重要研究成果发表于国际知名期刊《Nature Communications》。
RL-GenRisk:基于强化学习的新范式
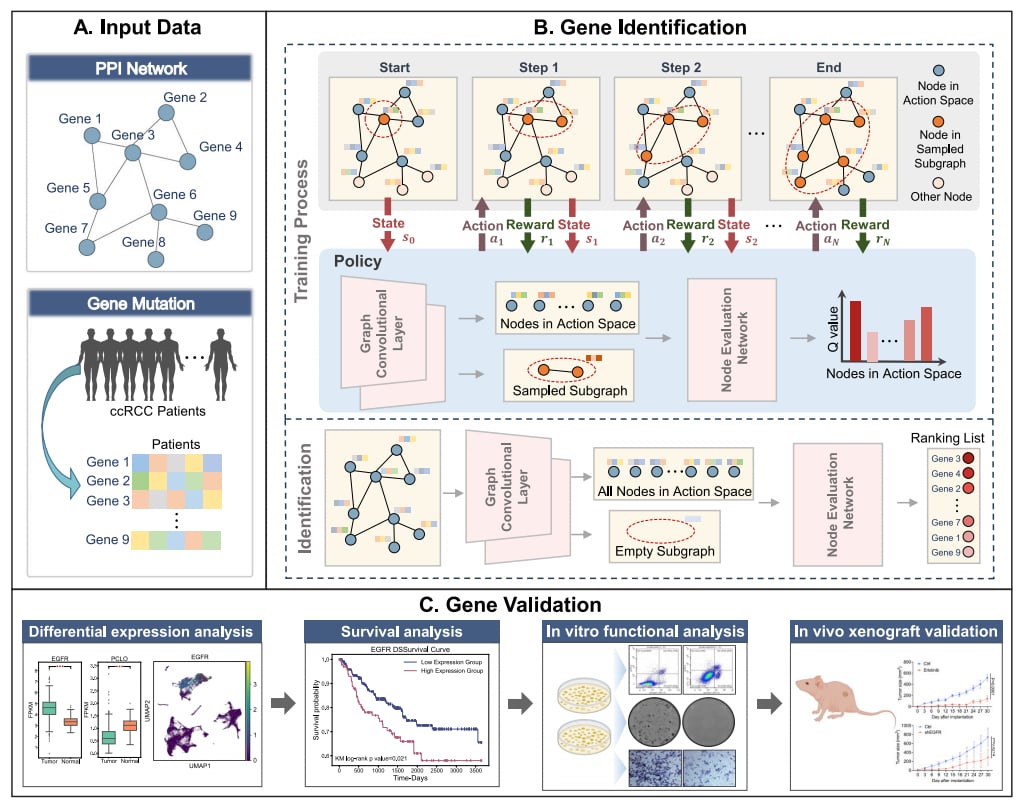
图1. RL-GenRisk 总体框架图
RL-GenRisk创新性地引入了强化学习框架,将ccRCC风险基因的识别过程建模为一个序列决策问题(马尔可夫决策过程, MDP)。该模型以蛋白质-蛋白质相互作用(PPI)网络和基因突变数据作为输入(图1.A)。它将包含突变信息的PPI网络视为“环境”,通过一个策略网络(包含图卷积网络GCN和节点评估网络,图1.B)与环境交互,学习如何在网络中选择节点(基因)。其目标是找到一个基因子集,这个子集能够“覆盖”尽可能多的癌症患者(即这些患者携带子集中至少一个基因的突变),同时通过引入基因长度信息来校正,避免长基因因偶然携带乘客突变而被错误识别。这种方法不严重依赖大量已知的风险基因,能够有效应对数据稀疏的挑战。
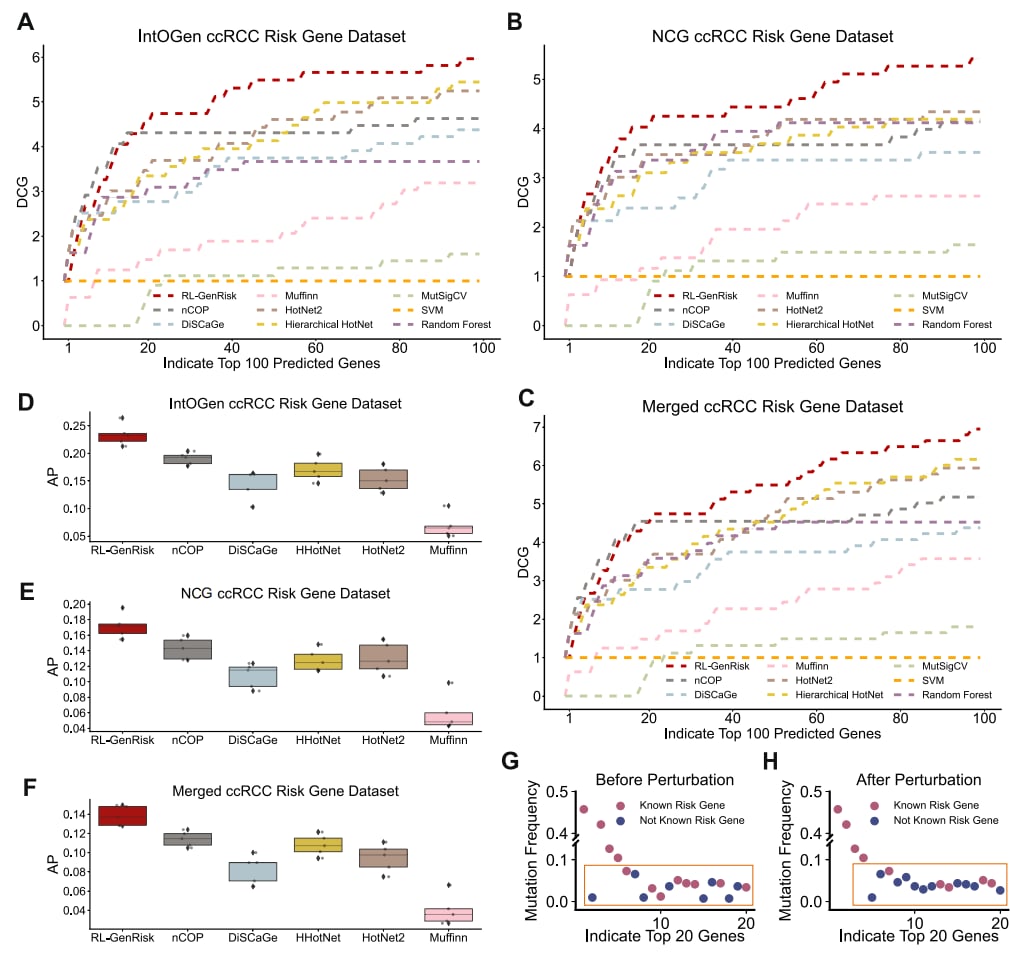
图2. RL-GenRisk和现有方法的对比实验结果
对比实验结果显示,RL-GenRisk在识别ccRCC风险基因方面的表现显著优于现有的多种方法(图2 A-F),证明了其有效性和优越性。
RL-GenRisk识别ccRCC关键风险基因:聚焦EGFR与PCLO
研究团队进一步分析了RL-GenRisk识别出的Top 20 ccRCC相关风险基因。富集分析表明,这些基因显著富集在“肾透明细胞癌通路”上(图3.A)。其中,EGFR基因尤为引人注目。差异表达分析显示,无论是在组织样本(bulk)还是单细胞(single-cell)层面,EGFR在癌组织和癌细胞中均呈现显著的高表达(图3. B,E,F,G)。更重要的是,生存分析发现,EGFR蛋白的高表达与ccRCC患者较差的生存预后显著相关(图3. C,D),提示EGFR可能是一个关键的治疗靶点。
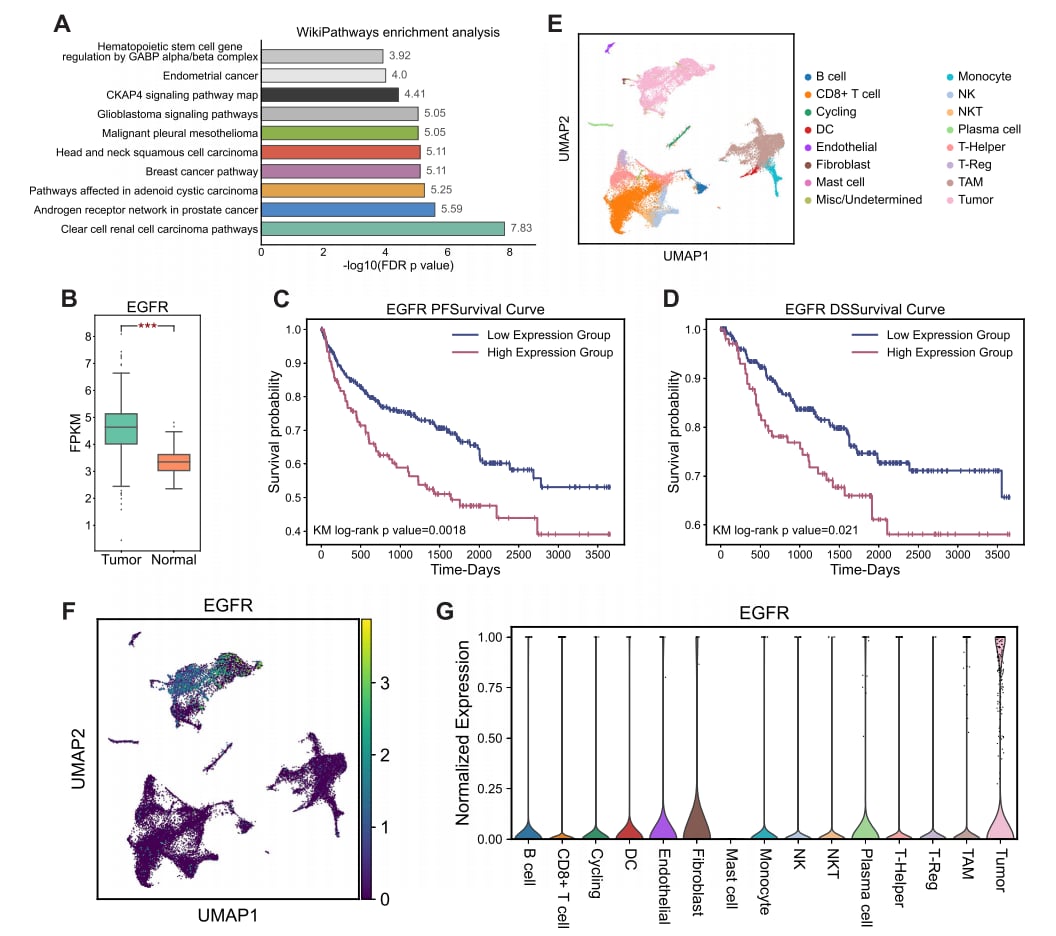
图3. 独立数据集分析
实验验证:EGFR与PCLO的功能研究与治疗潜力
为了验证RL-GenRisk识别出的风险基因的功能,并探索其作为ccRCC潜在治疗靶点的可行性,研究团队进行了深入的生物学实验,重点关注了EGFR和PCLO这两个基因。
EGFR在ccRCC进展中的作用:
- 体外实验:研究发现,下调EGFR的表达能够显著抑制ccRCC细胞的活性、迁移能力和克隆形成能力,并促进细胞凋亡(图4)。
- 体内实验:在小鼠模型中,使用EGFR抑制剂厄洛替尼(Erlotinib)进行治疗,能有效抑制ccRCC肿瘤细胞的生长和迁移,并诱导其凋亡(图5)。这一发现直接证明了靶向EGFR对于ccRCC治疗的潜力。对于需要厄洛替尼这类靶向药的患者,了解可靠的海外购药渠道非常重要,例如可以通过MedFind的代购服务获取相关药物信息和价格参考。
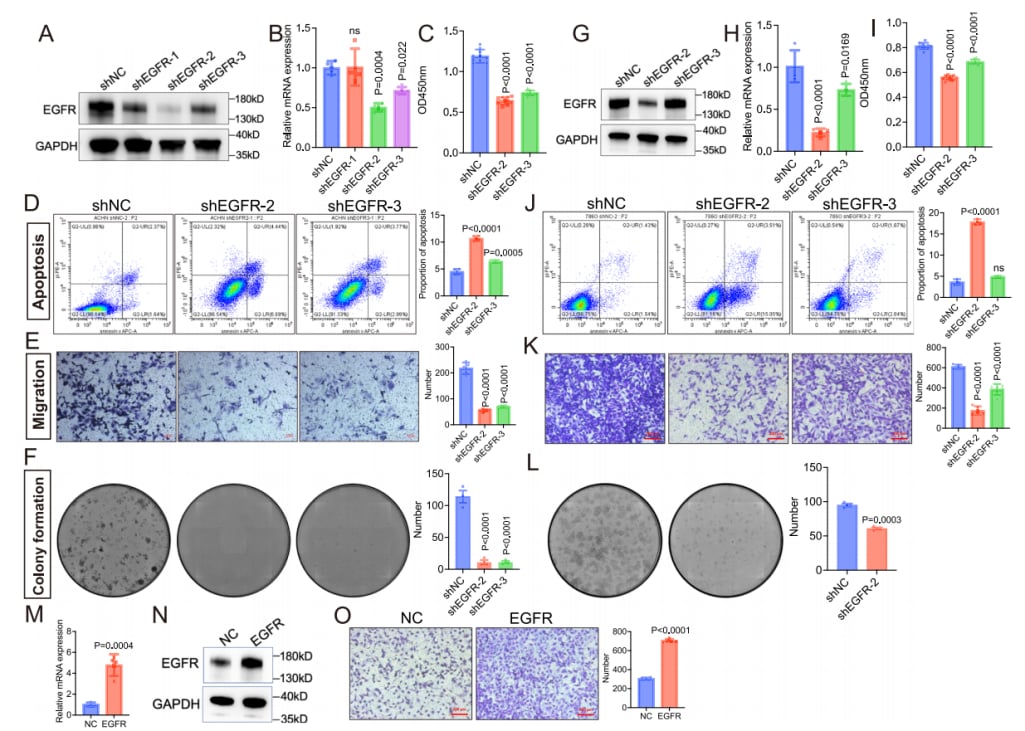
图4. EGFR失调在体外实验中显著影响ccRCC的进展
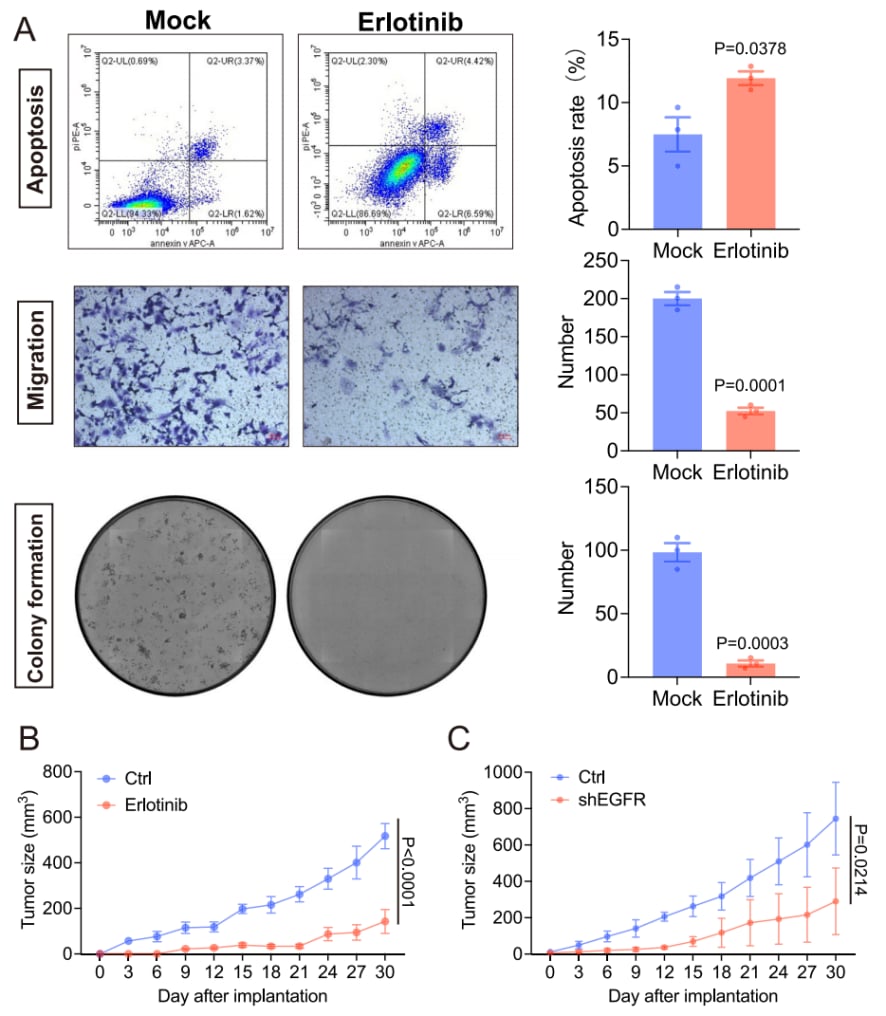
图5. 抑制EGFR表达在体外和体内实验中抑制ccRCC的进展
PCLO在ccRCC进展中的作用:
- 体外实验:研究同样发现,下调PCLO的表达也显著抑制了ccRCC细胞的活力、克隆形成能力、迁移和侵袭能力,并促进了细胞凋亡。此外,PCLO的敲低还影响了细胞的形态和运动能力(图6)。
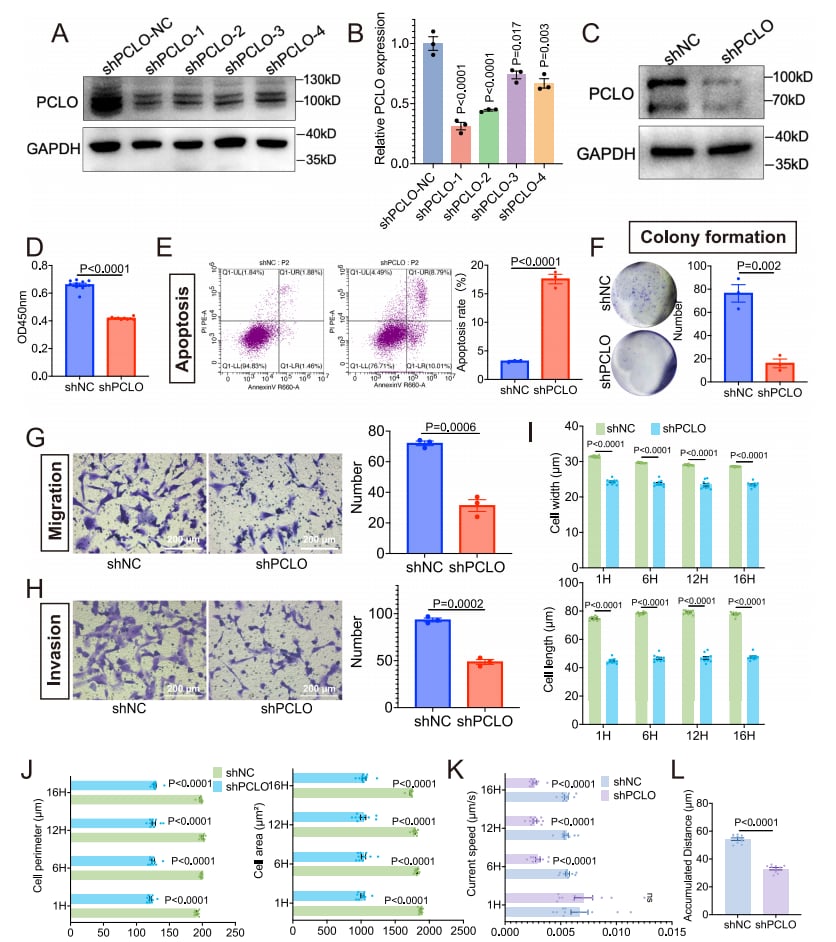
图6. PCLO失调显著影响ccRCC的进展
这些实验结果有力地证明,RL-GenRisk识别出的风险基因,特别是EGFR和PCLO,不仅与ccRCC的发生发展密切相关,而且具有成为潜在治疗靶点的巨大潜力。
研究总结与展望
总而言之,这项临床研究成功设计并验证了一种基于强化学习的癌症风险基因识别新方法RL-GenRisk。该方法通过将风险基因识别建模为节点选择过程,并结合生物学先验知识设计奖励函数,有效提升了识别肾透明细胞癌(ccRCC)风险基因的准确性。通过生物实验验证,研究证实了EGFR和PCLO等基因在ccRCC进展中的关键作用,尤其是EGFR作为靶向治疗的潜力,为开发新的抗癌药物和优化治疗方案提供了重要的科学依据。对于复杂的癌症信息和个性化治疗选择,患者可以考虑使用MedFind AI问诊等工具获取辅助信息。未来,RL-GenRisk有望应用于更多癌种的风险基因识别,推动癌症精准医疗的发展。
(研究由西北工业大学彭佳杰课题组、天津大学郝建业课题组、四川大学艾建忠课题组合作完成,共同第一作者为鹿大智、郑岩、易贤颜翎,共同通讯作者为郝建业、艾建忠、彭佳杰。)





