很多初诊就发现已经发生转移的肾细胞癌患者和家属,都会卡在一个非常现实的选择题上:到底要不要“先把肾切掉”(细胞减灭性肾切除),还是应该先做全身治疗?过去很长一段时间,很多人默认“能切就先切”。但近些年的研究不断提醒我们:对一部分IMDC中危/高危患者来说,贸然上手术未必是最优解。
这篇文章我们会用尽量易懂的方式,带大家看懂一项很新的随机研究——CYTOSHRINK:它探索了一种“更温和但更精准”的减瘤策略:用立体定向放疗(SBRT)先把原发肾肿块用高剂量分次照射“打趴”,同时配合目前常用的一线双免疫方案纳武利尤单抗(Opdivo, Nivolumab)+伊匹木单抗(Yervoy, Ipilimumab)。我们重点回答患者最关心的三个问题:①疗效有没有更好?②副作用会不会更重、会不会伤肾?③这项研究对你当下的治疗决策意味着什么?
一、先把概念说清:什么是“初诊即转移的肾癌(de novo mRCC)”?
“初诊即转移”指的是:第一次确诊肾细胞癌时,就已经在肾以外发现转移灶(比如肺、骨、肝、淋巴结等)。这类患者在门诊并不少见,研究者也提到,它们在临床上占比不低。
这类患者的治疗逻辑通常是“全身治疗为主、局部治疗为辅”,但“局部治疗”到底什么时候做、做什么(手术还是放疗)、做了能不能让全身治疗更有效,一直是肿瘤多学科讨论(MDT)里最常争论的点之一。
二、为什么现在不再默认“先切肾”?SURTIME与CARMENA带来的改变
传统观点认为:把“最大块的肿瘤”(原发肾肿块)先切掉,可以减少肿瘤负荷,给后续药物治疗“减压”。但两项关键研究(SURTIME、CARMENA)让大家开始重新审视:对于IMDC中危和高危的转移性肾癌患者,上来就做细胞减灭性肾切除并不一定带来更好的总体获益,有时甚至可能因为术后恢复、并发症、延误系统治疗而得不偿失。
这并不是说“手术没用”,而是提醒我们:手术的时机与适合的人群非常关键。很多团队开始倾向于:先系统治疗,等病情控制、体力状态改善后,再讨论是否做“反应适应性”的手术或局部治疗。
三、CYTOSHRINK到底在问什么问题?一句话总结
CYTOSHRINK是一项随机Ⅱ期研究,核心问题是:
对初诊即转移的肾细胞癌患者,如果不急着切肾,而是用SBRT对原发肾肿块做“细胞减灭式放疗”,再配合一线双免疫,能否比单纯双免疫带来更好的结局?
1)为什么选择SBRT来“减瘤”?
你可以把SBRT理解为“激光级别的放疗狙击”:它用很陡的剂量梯度把高剂量集中打在肿瘤上,同时尽量保护周围正常组织。研究者的设想是:
- 局部控制:用30–40 Gy/5次(5个分次)这种“消融剂量”压住原发肾肿块;
- 不耽误系统治疗:相比大手术,SBRT通常对整体恢复影响更小;
- 可能的免疫协同:放疗打碎肿瘤细胞后,可能释放更多“肿瘤碎片信息”(抗原),让免疫治疗更容易识别和追杀肿瘤细胞。这种设想常被称为“免疫增敏/免疫协同”。
需要强调:这些免疫协同在不同肿瘤、不同方案里并不一定都能兑现,CYTOSHRINK就是用临床随机试验去验证“到底有没有更好”。
2)为什么搭配双免疫?
研究中使用的是标准治疗之一:纳武利尤单抗+伊匹木单抗,随后以纳武利尤单抗维持。简单打个比方:
- 纳武利尤单抗像是“松开T细胞刹车”的一把钥匙(PD-1通路相关);
- 伊匹木单抗更像是“放开免疫系统总闸门”的一把钥匙(CTLA-4通路相关);
- 两者合用是“双重松刹车”,但也意味着免疫相关副作用需要更严密监测。
四、研究怎么做的?患者最需要记住的设计要点
CYTOSHRINK为随机、2:1分配的Ⅱ期研究,入组人群为初诊即转移的肾细胞癌患者。
- 对照组:纳武利尤单抗+伊匹木单抗,之后纳武利尤单抗维持(标准治疗)。
- 试验组:先用纳武利尤单抗+伊匹木单抗,随后对原发肾肿块进行SBRT(30–40 Gy/5次,实际多数为30–35 Gy/5次),再继续双免疫并进入纳武利尤单抗维持。
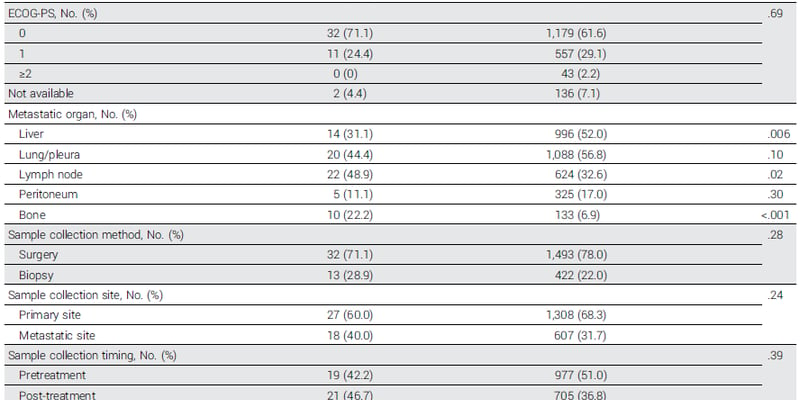
研究者也提到一个现实背景:研究开展在新冠疫情初期,临床上出现较多“更晚期、负荷更重”的患者;并且试验组基线里肝转移、骨转移更多,这一点在解读结果时需要放在心里。
五、最关键的疗效结果:一年PFS没拉开,但“持续缓解”出现信号
1)一年无进展生存期(1-year PFS):两组没有显著差异
研究初步读出显示:1年PFS在SBRT+双免疫组与单纯双免疫组之间没有显著差异。对患者来说,这意味着:就“延缓第一次进展”这个指标而言,现阶段并不能说加了SBRT就一定更好。
2)客观缓解率(ORR):原发肿块在位时,并未显示优势
研究者提到:在“原发肾肿块仍在位”的患者中,缓解率大约为试验组33%,对照组略高(不足42%)。这说明:至少从总体缓解比例看,加SBRT并没有带来更高的“立刻缩小”的人群占比。
3)真正值得关注的信号:随访末次仍在缓解的比例更高(50% vs 10%)
研究里最“让人想继续追下去”的,是随访末次仍处于持续缓解(ongoing response)的比例:对照组约10%,试验组约50%。
把它翻译成更接地气的话:加了SBRT以后,虽然不一定让更多人“马上见效”,但在一部分人身上,可能更容易出现“缓解更持久、更耐用”的免疫效应。
但我们也必须提醒一句:这属于随机Ⅱ期研究的早期信号,样本量、基线不平衡、后续治疗(比如进展后继续治疗、后续是否做了肾切除)都会影响这个结果。它更像“值得继续做大样本验证的线索”,而不是立刻改变所有人的标准方案。
4)总体生存(OS):仍在随访中
研究者明确表示:OS还在继续成熟、继续随访。对患者来说,这很重要,因为最终我们更关心“能不能活得更久、活得更好”,而不仅是某个时间点的影像进展。
六、安全性:最让人松一口气的结论——没有看到更多肾损伤
当把“高剂量放疗”与“双免疫”叠加时,患者最担心的通常是两点:①副作用叠加会不会很可怕?②对肾功能会不会造成不可逆伤害?
CYTOSHRINK的初步结论是积极的:该组合总体耐受良好,在研究设定的剂量和分次下,没有观察到更多的肾损伤或显著不良反应增加。这为后续进一步研究(更大规模、更多分层、更精准筛选人群)提供了安全性基础。
七、这项研究对患者当下的“治疗决策”有什么启发?给你一个可落地的思考框架
1)先明确你属于哪一类风险与负荷:IMDC分层仍然重要
IMDC风险分层会影响治疗策略的倾向。一般来说,中高危患者更强调先系统治疗的价值;而低危、转移负荷较轻、症状主要来自原发灶的人群,局部治疗的角色可能不同。请把你的IMDC分层、转移部位与数量、症状负担,作为与医生讨论的起点。
2)“原发灶在位”不是原罪,但可能影响免疫治疗表现
研究者提出的背景观察是:系统治疗在“已经做过肾切除”的人群里似乎更容易起效。CYTOSHRINK尝试用SBRT去“替代部分减瘤作用”,让原发灶不必立刻手术也能获得“减负荷/免疫协同”的潜在收益。这给了我们一个新的选择:当你不适合马上手术时,局部放疗可能是可讨论的桥梁。
3)不要把SBRT理解成“谁都该加”的标准操作
从现有数据看,一年PFS没有显著差异,因此“所有人都加SBRT”并没有证据基础。更合理的做法是:在MDT里讨论你是否属于可能获得“更持久缓解”的那一小部分人,并结合治疗可及性、放疗中心经验、肿瘤大小与位置、肾功能基础情况综合决策。
4)警惕“后续治疗”对结果的影响:进展后继续治疗、之后再切肾
研究提到:试验组中有人“进展后仍继续治疗”,也有人后续做了肾切除。现实世界里也一样:治疗不是一锤子买卖,而是动态策略。你要问医生的不是“选A还是B”,而是:
- 如果我用双免疫起效,什么时候复评?
- 如果我原发灶症状重(出血、疼痛、梗阻风险),能否用SBRT先解决局部问题?
- 如果我获得深度缓解,是否需要/适合后续手术?
八、把治疗落到生活里:双免疫±SBRT常见副作用与居家应对清单
下面是我们在科普中最希望家属保存下来的一部分:出现问题时,至少知道“可能是什么、该怎么做、什么时候必须立刻就医”。提示:具体处理以主管医生给出的个体化方案为准。
1)双免疫常见免疫相关不良反应(irAEs):早识别比硬扛更重要
- 皮肤:皮疹、瘙痒。居家:温和保湿、避免热水烫洗;若皮疹范围扩大或伴水疱、发热,尽快联系医生。
- 胃肠道:腹泻、腹痛(警惕免疫性结肠炎)。居家:记录每天大便次数与性状、补液;若腹泻明显增加、出现血便/发热/脱水,需紧急就医。
- 肝脏:转氨酶升高常无症状。居家:不要自行服用“保肝药”“草药”;按时抽血复查。
- 肺:咳嗽、气短(警惕免疫性肺炎)。居家:任何新发或加重的气促都不要拖,尤其合并发热或血氧下降时。
- 内分泌:乏力、怕冷、心悸、体重变化(甲状腺、垂体、肾上腺相关)。居家:把“持续乏力”当成需要排查的信号,按医嘱做甲功、皮质醇等检查。
我们反复强调一句:免疫治疗副作用很多不是“忍一忍就过去”,而是“越早干预越容易控”。出现疑似免疫毒性时,请不要自行停药或自行用激素,应第一时间联系治疗团队。
2)SBRT照射肾原发灶:可能出现什么不适?
研究中组合方案总体耐受良好,且未见更多肾损伤信号。现实中,SBRT围绕肾脏照射可能出现:
- 疲劳:放疗期间常见。建议:保证睡眠、适度活动(散步10–20分钟)、白天小憩但避免睡太久影响夜间睡眠。
- 恶心、胃口差(与照射范围、个体差异有关):建议少量多餐、清淡高蛋白(鸡蛋、鱼、豆腐、酸奶),必要时与医生沟通止吐药。
- 肾功能监测:即便研究中未见增加,也建议按时复查肌酐、eGFR、尿常规、尿蛋白,并把既往肾病、单肾状态、糖尿病高血压等风险告诉医生。
3)饮食与运动:目标不是“吃出奇迹”,而是让你更能扛住治疗
- 蛋白质:若肾功能允许,优先优质蛋白(鱼、瘦肉、蛋、奶、豆制品)。若存在明显肾功能受损,蛋白摄入量需听肾内科或营养师建议。
- 补液:腹泻、发热时更要防脱水;但若合并心衰、肾衰,补液策略需谨慎。
- 运动:以“不累到第二天”为标准,抗阻训练(弹力带、深蹲起立)有助于维持肌肉,减少治疗期虚弱。
4)心理与家属协作:把“未知”变成“可管理的清单”
我们见过太多家庭被“下一次复查会怎样”折磨。一个很有效的方法是建立“治疗日志”:每天记录体温、体重、腹泻次数、皮疹情况、血压血糖(如需要)、用药时间与不适评分。你会发现:很多焦虑来自失控感,而记录能让你更早发现异常,也更容易和医生高效沟通。
九、药物与治疗可及性:在中国大陆能否用上?
从药物角度看,纳武利尤单抗与伊匹木单抗均为已获批并在临床使用的免疫检查点抑制剂(不同肿瘤与适应症的覆盖可能随政策更新而变化,具体以就诊医院与最新药监信息为准)。
从技术角度看,SBRT在国内很多肿瘤中心都可以开展,但“对肾原发灶做细胞减灭式SBRT并与双免疫进行严谨衔接”,更依赖放疗科经验、影像引导与剂量学能力,也需要内科与放疗科紧密配合。若你所在地区医疗资源有限,可以考虑向具备泌尿肿瘤MDT的中心咨询第二意见。
十、下一步研究在做什么?为什么“生物标志物”可能决定你是否适合这种策略
CYTOSHRINK后续将重点推进生物标志物项目,包括肠道微生物组与序贯血液采样等。对患者的意义是:未来可能不是靠“感觉”来猜谁适合加SBRT,而是通过更客观的指标,筛出更可能获得“持久缓解”的那部分人。
目前阶段,我们仍处在“看见信号、等待验证”的过程中。对患者最实际的建议是:如果你正在考虑类似策略,优先询问是否有合适的临床试验或前瞻性队列可以加入,因为这类问题最需要高质量证据来回答。
结尾:我希望你带走的结论,与下一步怎么做
把CYTOSHRINK的信息浓缩成三句话:
- 对初诊即转移的肾细胞癌患者,SBRT联合双免疫在一年PFS上未显示明确优势,但出现了“持续缓解比例更高”的早期信号。
- 更重要的是:从这项研究的初步结果看,把高剂量SBRT与纳武利尤单抗+伊匹木单抗联合在安全性上是可行的,未见更多肾损伤信号。
- 它不会立刻取代标准治疗,但给“不能或不宜立刻切肾”的患者提供了一个值得认真讨论的方向:能否用更精准的局部放疗参与减瘤,并争取更持久的免疫获益。
如果你愿意,我们建议你下一次复诊时带着这4个问题去和医生对齐:①我属于IMDC哪一类风险?②我的症状主要来自原发灶还是转移灶?③我是否适合双免疫方案,是否存在免疫治疗高风险因素?④在我身上,SBRT或延后手术的价值在哪里、风险在哪里?
在MedFind,我们最擅长做两件事来帮助你把“复杂选择题”变成“可执行方案”:其一,基于你现有的病理、影像、分期与用药史,提供AI辅助问诊与治疗方案解读,把关键信息整理成医生也看得懂的要点清单,便于你高效完成MDT或第二意见;其二,当你和医生决定使用特定前沿药物方案、但面临可及性与时间差问题时,我们可以提供抗癌药品跨境直邮的信息支持与合规路径参考,尽量减少“等药”带来的治疗窗口损失。
你不需要一次就做出完美决定,但你可以从今天开始,让每一步都更有依据、更可控。
参考信息
Bex A, Mulders P, Jewett M, et al. JAMA Oncol. 2019;5(2):164-170. doi:10.1001/jamaoncol.2018.5543
Méjean A, Ravaud A, Thezenas S, et al. N Engl J Med. 2018;379(5):417-427. doi:10.1056/NEJMoa1803675
Lalani AK, Pond GR, Siva S, et al. J Clin Oncol. 2026;44(suppl 7):416. doi:10.1200/JCO.2026.44.7_suppl.416