亲爱的患者朋友和家属们,当您或家人不幸被诊断出结直肠癌时,内心一定充满了焦虑和疑问。您可能听说过各种癌症类型,但今天我们要深入探讨的是一种特殊且容易被误诊的结直肠癌亚型——结肠腺瘤样腺癌(Adenoma-like Adenocarcinoma, 简称ALAC)。这种癌症形态上极具“迷惑性”,常常被误认为是良性的腺瘤,但其本质却是真正的侵袭性癌症。然而,令人欣慰的是,与其他结直肠癌相比,ALAC的预后通常非常好。准确识别ALAC不仅能避免误诊,更重要的是,能帮助患者获得恰当的治疗,避免不必要的过度干预,这对患者未来的生活质量至关重要。本文将为您全面解析ALAC的奥秘,从背景知识、诊断挑战到预后特征,助您拨开迷雾,更好地理解这一特殊疾病,为接下来的诊疗决策提供坚实基础。
一、结直肠癌的普遍背景与ALAC的特殊定位
结直肠癌(CRC)是全球范围内最常见的恶性肿瘤之一,其发病率和死亡率均居高不下,对人类健康构成巨大威胁。据统计,每年全球有超过190万新发病例,约93万人因此失去生命。随着人口老龄化和筛查项目的推广,结直肠癌的负担在全球范围内持续增加,尤其在老年人群中更为显著。
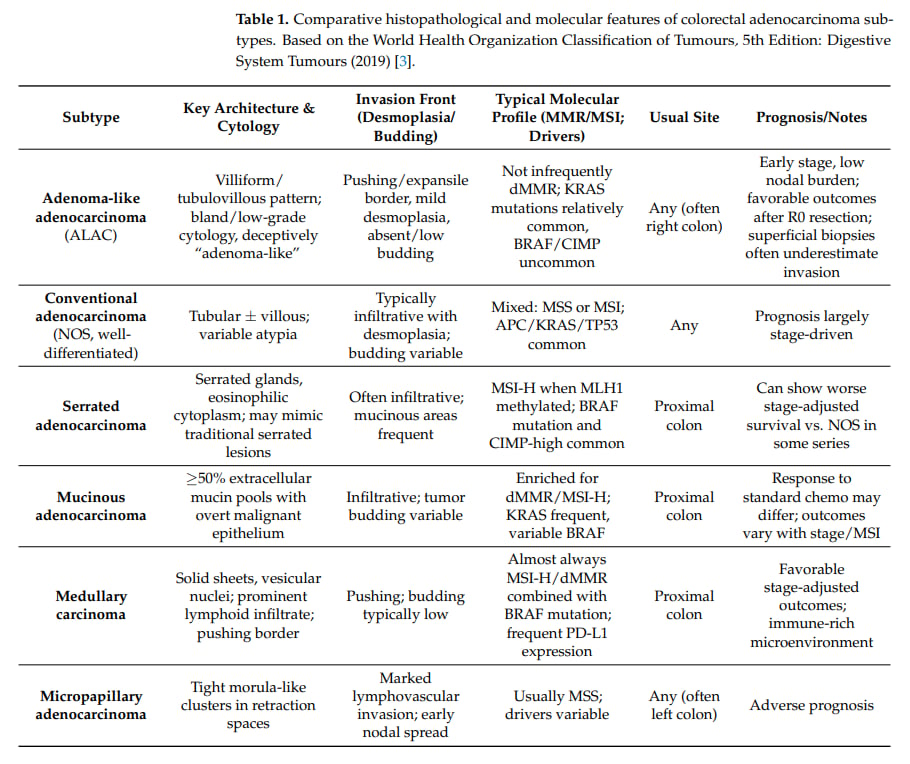
为了更精准地指导临床实践,世界卫生组织(WHO)在2019年发布的第5版《消化系统肿瘤分类》中,将结直肠腺癌细分为多种组织学亚型,包括我们熟知的普通型腺癌、黏液腺癌、锯齿状腺癌等。而结肠腺瘤样腺癌(ALAC)正是在这版分类中新增纳入的一种“新面孔”。之所以称其为“新”,是因为它独特的形态特征使其长期以来难以被清晰界定,很容易与良性病变混淆。其核心特点就是形态上与传统的管状绒毛状腺瘤高度相似,具有极强的“伪装性”。这种迷惑性在病理诊断中常常制造“陷阱”,尤其当活检样本有限时,极易导致诊断不足或错误。
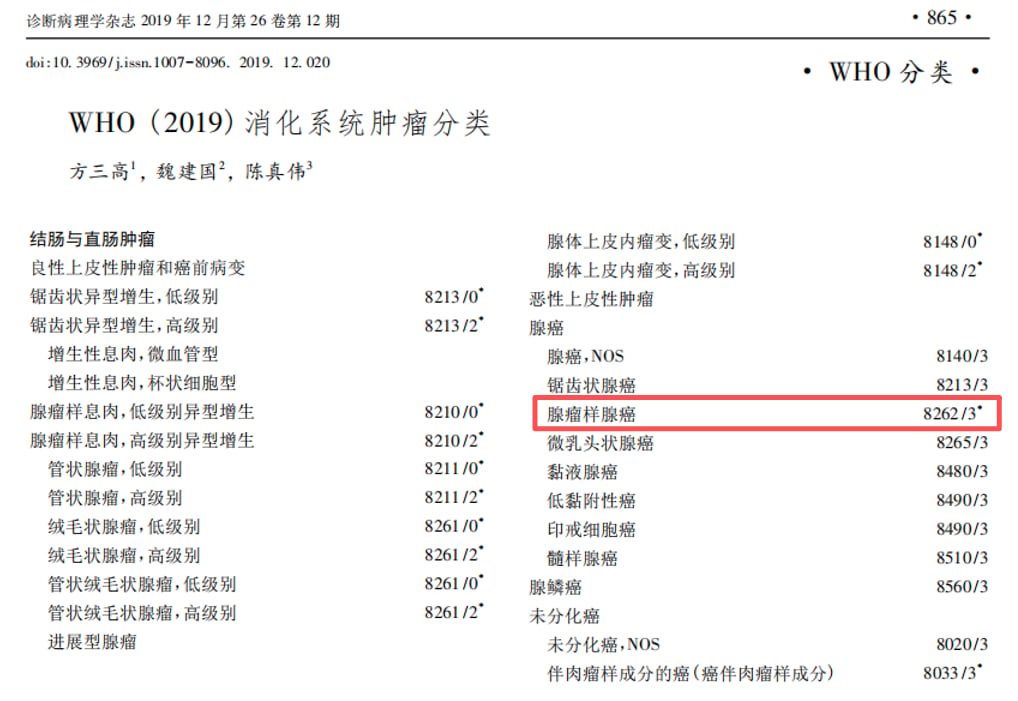
由于诊断上的挑战,ALAC的真实发病率目前仍不明确,很可能被严重低估。据估计,ALAC在所有结直肠腺癌中可能占到3%到9%的比例。因此,提升对这种特殊亚型的认知,对于临床医生和病理医生来说都至关重要,它直接关系到患者能否获得准确的诊断和恰当的治疗。
二、诊断的“陷阱”与“线索”——ALAC为何易被误诊?
ALAC最突出的特点就是其“腺瘤样”的形态,这使得它在病理科医生眼中像一个善于伪装的“骗子”。其组织病理学特征表现为绒毛状或管状绒毛状结构,细胞异型性(即癌细胞与正常细胞形态的差异)程度较低,同时肿瘤通常呈现一种“膨胀性生长”模式,即肿瘤像一个球体一样向外扩张,而不是像其他腺癌那样,细胞散漫地、侵略性地向周围组织浸润。最关键的是,普通腺癌常伴有的浸润性侵袭特征,如促纤维增生(肿瘤周围结缔组织增生变硬)、肿瘤出芽(少量癌细胞脱离主肿瘤灶向外扩散)、筛状结构(癌细胞形成类似筛子的结构),在ALAC中却极少出现或完全缺失。这些特点让浅表活检(内镜下取样)的病理报告很容易将其误判为非侵袭性腺瘤,从而导致诊断不足和临床处置不当。
1. 活检的局限性与临床的警惕信号
就如本文开头提到的病例,患者的病灶最初被判定为非侵袭性病变,但手术切除后才最终确诊为侵袭性腺癌。这充分说明了浅表活检的局限性。很多时候,活检可能只取到了肿瘤表面的腺瘤样成分,而遗漏了深层的侵袭性部分。因此,在临床实践中,内镜医生和病理医生需要保持高度警惕。
当医生在结肠镜检查中发现以下特征的肿物时,应特别注意:
- 体积较大:通常超过2厘米。
- 广基多为无蒂:病灶底部宽阔,没有明显的蒂部。
- 呈绒毛状结构:表面粗糙,像天鹅绒一样。
- 大体观察可见中央凹陷区域:可能提示深部存在侵袭。
- 病灶旁黏膜存在“鸡皮样”外观:一种不规则、颗粒状的外观。
如果出现上述任何一种情况,即使初次活检结果不明显,也应强烈建议进行完整切除或对肿瘤进行充分多点取样,以避免漏诊。
2. 组织病理学上的“火眼金睛”
对于病理医生而言,ALAC的诊断挑战在于如何在显微镜下区分真正的侵袭性癌与结构复杂的良性腺瘤。由于ALAC的生长模式是膨胀性的,而不是典型的浸润性,其分期也需要更加细致的评估。在缺乏典型促纤维增生、肿瘤出芽或显著细胞学异型性的情况下,病理医生需要依赖经验积累的细微征象来判断:
- 腺体扭曲和轮廓不规则:癌变腺体往往失去正常的规则形态。
- 隐窝异位且周围无固有层包绕:腺体结构不正常地出现在黏膜深层,且缺乏正常黏膜固有层的支持。
- 推挤式边界:肿瘤的基底部呈指状向下推挤,突破了黏膜肌层。这种模式虽然在其他部位的低级别浸润性癌中常见,但在结直肠病理中尚未被广泛报道。
这些特征可能与黏膜脱垂或假性侵袭高度相似,尤其在乙状结肠或直肠部位的病变中更容易混淆。因此,结合肿瘤复杂的结构特征和腺体排列间距的消失,即使细胞学级别较低,这些细微之处仍可为ALAC的组织学诊断提供有力支持。
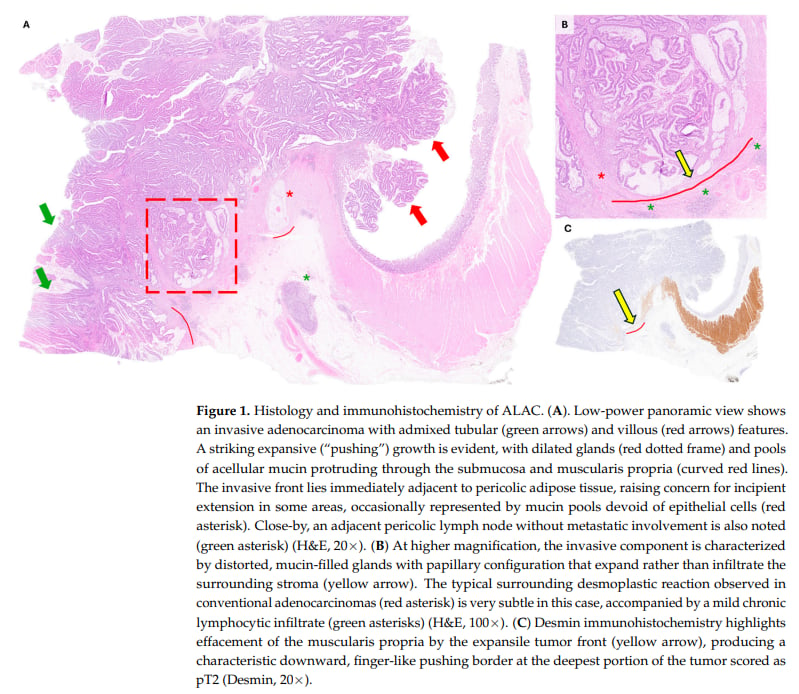
3. 免疫组化:精准诊断的关键辅助手段
对于那些“模棱两可”的病例,免疫组化(Immunohistochemistry, 简称IHC)就成为不可或缺的辅助工具。它通过特定抗体染色,帮助我们识别肿瘤细胞的特定蛋白质表达,从而明确诊断。
PMS2表达缺失与错配修复缺陷(dMMR)
本文中的病例报告显示,患者的免疫组化分析呈现PMS2单独表达缺失。这是什么意思呢?
我们的细胞在复制DNA时,偶尔会发生“错配”,就像打字时敲错了字母。为了纠正这些错误,细胞有一套“纠错系统”,叫做错配修复(Mismatch Repair, 简称MMR)系统。这个系统由多种蛋白质(如MLH1、MSH2、MSH6和PMS2)共同协作完成。当这些蛋白质中的某一个或几个出现问题,导致修复功能丧失时,我们就称之为错配修复缺陷(deficient Mismatch Repair, 简称dMMR)。
dMMR会导致DNA复制错误的累积,特别是在被称为“微卫星”的特定DNA重复序列区域。当这些区域的重复次数发生变化时,就称之为微卫星不稳定性(Microsatellite Instability, 简称MSI)。MSI根据不稳定程度分为高不稳定(MSI-H)和低不稳定(MSI-L),而dMMR通常与MSI-H高度相关。
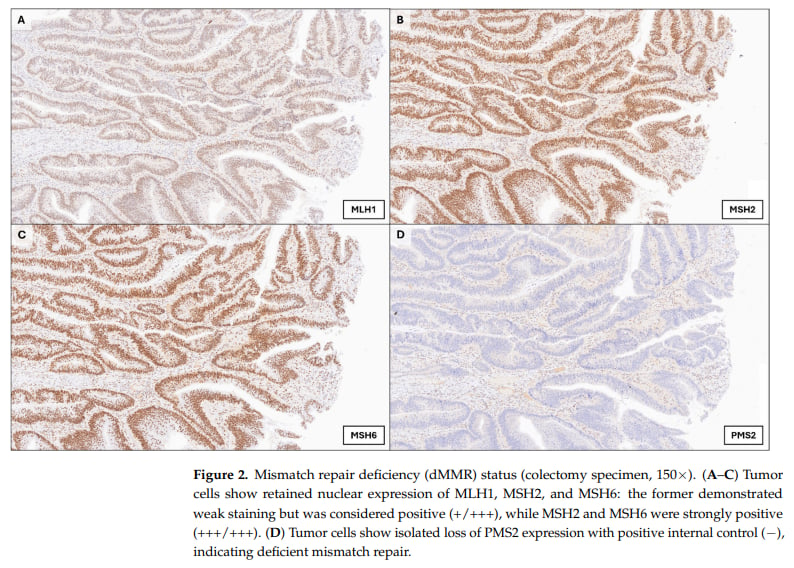
在结直肠癌中,dMMR/MSI-H是一种重要的生物标志物,它不仅对预后有提示作用,更重要的是,它是预测患者对免疫检查点抑制剂(如PD-1/PD-L1抑制剂)治疗敏感性的关键指标。对于ALAC患者而言,PMS2单独表达缺失提示存在dMMR,这意味着他们的肿瘤可能具备某些独特的生物学行为和预后特征,甚至可能预示着对特定治疗方案的反应。
上皮内肿瘤浸润淋巴细胞(iTILs)
除了dMMR,上皮内肿瘤浸润淋巴细胞(intratumoral Tumor Infiltrating Lymphocytes, 简称iTILs)也是识别ALAC的有用线索。iTILs是指浸润到肿瘤细胞团内部的淋巴细胞,它们是人体免疫系统对抗肿瘤的表现。在ALAC患者中,iTILs的出现频率通常高于普通型腺癌,这可能意味着ALAC的肿瘤微环境侵袭性更低,免疫系统对其有一定的抑制作用,进而解释了其相对良好的预后。有研究表明,iTILs水平高(例如每高倍镜视野下≥5个)与更好的无复发生存期独立相关。
三、预后“优等生”的秘密——ALAC的分子特征与良好结局
ALAC之所以被称为结直肠癌中的“预后优等生”,是因为它在生物学行为上展现出与众不同的一面。尽管超过三分之二的ALAC病例在病理分期时已达到pT2期甚至更高,但其淋巴结受累率却显著低于普通型结直肠腺癌(仅约20%),远处转移的发生率也更低(约15%)。经过年龄和分期因素校正后,ALAC患者的总生存期显著优于普通型高分化结直肠腺癌,疾病特异性死亡率仅为12%,处于较低水平。
这意味着,如果ALAC患者能够实现完整的R0切除(即手术切除时,病灶边缘没有癌细胞残留),即使不接受辅助治疗,患者也能获得非常好的预后,复发风险极低,正如本文中的81岁高龄患者,术后三年无肿瘤复发,最终因其他共病而非癌症进展离世。
1. 分子机制探究:为何高KRAS突变率却预后好?
ALAC的良好预后也与其独特的分子特征息息相关。与锯齿状腺癌不同,ALAC极少出现BRAF突变、CpG岛甲基化表型(CIMP高表达状态)或MLH1启动子高甲基化。相反,ALAC通常携带APC、KRAS和TP53等在普通型结直肠癌中常见的关键驱动突变,并且伴随典型的染色体不稳定性(CIN)驱动肿瘤发生过程。
令人感到“意外”的是,ALAC的KRAS突变发生率与普通型腺癌相当甚至更高,在一些最大样本量研究中可达58%。通常情况下,KRAS突变被认为是结直肠癌预后不良的标志,并可能影响某些靶向药物(如EGFR抑制剂)的疗效。然而,在ALAC中,高频率的KRAS突变似乎并未带来同样负面的影响,反而与良好的病理特征和预后相关。这背后的原因可能在于:
- 经典的腺瘤-腺癌序列:ALAC可能通过经典的腺瘤-腺癌序列(即从良性腺瘤逐步发展为癌)发生,而不是通过锯齿状通路,这可能赋予其不同的生物学行为。
- 肿瘤微环境的差异:越来越多的观点认为,癌症进展是一个复杂的生态学过程,肿瘤细胞与周围的基质、免疫细胞和血管组分相互作用。ALAC的肿瘤边界呈膨胀性推挤式,肿瘤出芽极少或缺失,促纤维增生程度极轻,同时存在上皮内淋巴细胞。这些特征共同提示ALAC的肿瘤生态系统侵袭性更低,可能限制了肿瘤的转移扩散,从而支撑了其相对惰性的临床病程。换句话说,即使存在KRAS突变,ALAC的微环境也可能抑制了其致癌作用。
- 未知遗传或表观遗传学改变:可能存在其他尚未被发现的遗传学或表观遗传学改变,这些改变在ALAC中抵消了KRAS突变的致癌作用。
这些发现都强调了ALAC的独特性,也说明了仅仅凭借单一分子标志物来判断肿瘤预后和治疗方案的局限性。
2. dMMR/MSI-H在ALAC中的预后意义
高微卫星不稳定性(MSI-H)在部分ALAC患者中也尤其高发。在普通型结直肠癌中,MSI-H肿瘤通常与早期患者预后更佳相关,并且对免疫治疗敏感。然而,对于ALAC患者,dMMR/MSI-H的预后意义可能有所不同。
由于ALAC本身细胞更新率较低,且其侵袭模式较为细微,这可能会削弱MSI-H肿瘤典型的免疫刺激效应,从而改变dMMR缺陷对预后影响的传统认知。此外,ALAC是否具备典型MSI-H癌症的免疫微环境特征(例如PD-1/PD-L1表达升高),目前也尚未得到充分证实。因此,在解读ALAC患者的dMMR状态时,需要结合其独特的病理和临床特征进行综合评估。
四、MedFind关怀:ALAC患者的诊疗与未来展望
对于ALAC患者而言,准确诊断是避免过度治疗和确保最佳预后的核心前提。由于其形态的隐匿性,患者和家属在收到病理报告时,如果诊断为“腺瘤”但临床表现与肿物体积不符,或病理报告有疑虑时,应积极与医生沟通,寻求多学科会诊或二次病理诊断的意见。
1. 遗传咨询与检测:PMS2缺失的深层含义
本文病例中,患者出现了PMS2单独表达缺失,这提示可能存在遗传性的错配修复缺陷,即林奇综合征(Lynch Syndrome)。林奇综合征是一种遗传性疾病,会显著增加结直肠癌、子宫内膜癌等多种癌症的风险。尽管这位81岁的患者没有提示林奇综合征的个人史或家族史,但在临床实践中,目前NCCN和欧洲指南均建议,无论患者年龄或家族史如何,所有错配修复缺陷(dMMR)的结直肠癌患者都应接受通用胚系检测(即检测基因是否为遗传性突变)。
然而,在老年患者中,PMS2单独表达缺失往往是散发性的(非遗传性),并非都预示着林奇综合征。但在临床实际中,尤其是当患者无自主决策能力、缺乏家庭支持或预期寿命有限时,推行全面的遗传检测可能面临挑战。不过,随着医学的进步,新兴工具如MLH1甲基化检测或靶向测序等,有望在未来无需仅依赖年龄或家族史,即可区分dMMR的散发性和遗传性病因,为患者提供更精准的遗传咨询。
2. 避免过度治疗的重要性
ALAC的独特之处在于其预后良好,这意味着部分患者可能无需接受像其他侵袭性腺癌那样强烈的辅助化疗。过度治疗不仅会增加患者的身体负担和副作用,还会影响生活质量,尤其对于高龄或伴有多种基础疾病的患者。因此,准确诊断ALAC,并根据其具体特征(如dMMR状态、肿瘤分期、患者一般情况)制定个体化的治疗方案,是临床医生和患者共同追求的目标。
3. 未来研究方向与诊疗展望
尽管我们对ALAC的认识逐渐加深,但仍有许多问题亟待解决:
- ALAC的免疫微环境特征:它是否具备典型MSI-H癌症的免疫特性,如PD-1/PD-L1表达升高?这对于免疫治疗的决策至关重要。
- 大样本研究:目前大多数是单病例报告或小样本研究,需要更多前瞻性注册研究来评估其进展风险和更全面的分子谱。
- 数字病理与人工智能:随着技术发展,数字图像分析和人工智能工具的引入,有望帮助病理医生更准确、可重复地识别ALAC的细微特征,明确诊断阈值,从而更精准地筛选出能够从个体化随访或辅助治疗策略中获益的患者。
MedFind致力于为癌症患者提供全面的最新抗癌资讯、药物信息,并协助构建跨境购药渠道。对于ALAC这种需要高度精准诊断的特殊疾病,我们相信,通过持续学习和分享最新研究进展,能帮助患者和家属更好地理解疾病,与医生共同制定最合适的治疗方案。未来,MedFind将继续关注这类少见但临床意义重大的肿瘤亚型,助力患者获得最优管理。
结 论
结肠腺瘤样腺癌(ALAC)是一种形态特征隐匿但具有重要临床意义的结直肠癌亚型。它在生物学层面处于结直肠良恶性病变的交界范畴,因其结构与普通腺瘤相似,且缺乏明确的侵袭性特征,极易导致误诊,尤其在活检样本量有限的情况下问题尤为突出。然而,一旦实现准确诊断和完整手术切除,ALAC整体预后良好,即使不开展辅助治疗,转移率也处于较低水平。
因此,充分认知ALAC的潜在临床与组织病理学诊断陷阱,联合免疫组化标记物(如PMS2等MMR蛋白)等辅助技术,是保障诊断分类准确、患者获得最优诊疗的核心要点。未来,医学界需要开展更大样本量的系列研究,明确ALAC的分子谱与免疫微环境特征,从而更精准地界定其在结直肠肿瘤谱系中的定位,并通过数字病理与人工智能工具来验证可重复的诊断标准,最终为这类特殊患者确定最优化、最恰当的管理方案。
参考文献:
Agüera-Sánchez, A.; Peña-Ros, E.; Martínez-Martínez, I.; García-Molina, F. Adenoma-like Adenocarcinoma of the Colon: Case Report and Diagnostic Pitfalls of an Underrecognized Entity with Favorable Prognosis. Onco 2025, 5, 39. https://doi.org/10.3390/onco5030039