癌症,这个令人闻风丧胆的疾病,每年都在夺走无数生命,让无数家庭蒙上阴影。在各类癌症中,实体瘤占据了绝大多数,例如肺癌、乳腺癌、肝癌、胃癌、结肠癌、卵巢癌等,它们形成一个实体的肿块,存在于身体的各个器官中。与白血病、淋巴瘤等血液系统肿瘤不同,实体瘤不仅生长在特定的组织中,还发展出一套复杂的防御机制,例如致密的肿瘤微环境、血管生成异常以及免疫抑制细胞的聚集,使得免疫细胞难以有效识别和清除。因此,实体瘤治疗一直是癌症研究领域的一大“硬骨头”,挑战重重。尽管近年来,以CAR-T和CAR-NK为代表的免疫细胞疗法在治疗血液肿瘤方面取得了突破性进展,甚至为许多患者带来了治愈的希望,但面对实体瘤,它们的疗效却常常不尽如人意,这让无数患者和家属感到无助和绝望。
然而,近日《自然》(Nature)杂志上发表的一项重磅研究,却为实体瘤的治疗带来了前所未有的曙光。由耶鲁大学的遗传学家Sidi Chen教授领导的科学家团队,历经五年多的不懈努力,发现了一个名为OR7A10的神秘基因。通过将这个基因引入自然杀伤(NK)细胞中,能够显著增强嵌合抗原受体自然杀伤(CAR-NK)细胞对抗实体瘤的能力。这项突破性研究在多个实体瘤小鼠模型中展现出令人震惊的效果,尤其是在乳腺癌模型中,甚至实现了肿瘤的完全消除,为长期困扰癌症治疗的实体瘤患者点燃了革命性的新希望。这一发现不仅有望彻底改变实体瘤的治疗格局,更可能为数百万面临实体瘤困境的患者带来真正意义上的生存转机。本文将深入解析这项前沿研究,带您了解OR7A10基因如何赋能CAR-NK细胞,以及它为实体瘤患者带来的深远意义。
癌症治疗的“圣杯”:实体瘤的挑战与细胞疗法
在人类与癌症的漫长斗争中,征服实体瘤一直被视为癌症治疗的“圣杯”,也是全球科学家共同努力的方向。实体瘤是癌症中最常见的类型,它们形成一个实体的肿块,可能出现在身体的任何部位,如肺部、肝脏、乳腺、结肠、卵巢等。根据世界卫生组织的数据,实体瘤占所有癌症病例的90%以上,其高发病率和死亡率给全球公共卫生带来了巨大负担。
与白血病、淋巴瘤等血液系统肿瘤不同,实体瘤的治疗难度更高,主要原因在于其独特的生物学特性和复杂的微环境:
- 难以渗透的物理屏障:实体瘤往往包裹着一层由纤维和胶原蛋白组成的致密基质,形成一道物理屏障,这就像一个坚固的“堡垒”,阻碍了化疗药物和免疫细胞有效浸润到肿瘤内部。免疫细胞即使被激活,也常常被阻挡在肿瘤外围,无法抵达核心区域发挥杀伤作用。
- 免疫抑制的肿瘤微环境:实体瘤周围的微环境是一个高度免疫抑制的场所。它充满了各种免疫抑制细胞(如调节性T细胞、髓系来源抑制性细胞)和免疫抑制因子(如TGF-β、IL-10),这些“帮凶”会直接“关闭”或“迷惑”前来攻击的免疫细胞,导致它们功能失活,甚至反过来促进肿瘤生长。免疫细胞在这个环境中如同陷入泥沼,逐渐失去战斗力,医学上称之为“免疫耗竭”。
- 肿瘤细胞的异质性与免疫逃逸:实体瘤内部的癌细胞并非铁板一块,它们具有高度的异质性,有些细胞对治疗敏感,有些则不然。更狡猾的是,癌细胞还会进化出各种机制来逃避免疫系统的识别和攻击,例如下调癌细胞表面的特异性抗原表达,或者上调PD-L1等免疫检查点分子,从而“欺骗”免疫系统,使其误认为癌细胞是“自己人”。
- 血管生成异常:实体瘤为了快速生长,会诱导异常的血管生成,但这些血管往往结构不完整,血流不畅,导致肿瘤内部出现缺氧和营养匮乏的区域,这不仅影响药物输送,也给免疫细胞的生存和功能带来了挑战。
面对这些严峻的挑战,传统的放化疗虽然能起到一定的作用,但往往伴随着严重的副作用,且难以彻底根治晚期实体瘤。因此,医学界迫切需要开发出更精准、更有效的治疗策略。在这样的背景下,细胞免疫疗法,特别是CAR-T(嵌合抗原受体T细胞)和CAR-NK(嵌合抗原受体自然杀伤细胞)疗法,作为革命性的抗癌武器应运而生。

这两种疗法的基本原理都是通过基因工程,在体外对患者自身的免疫细胞(T细胞或NK细胞)进行改造,使其表达一种特殊的“导航系统”——嵌合抗原受体(CAR)。这个CAR受体就像一个超级传感器,能够特异性地识别癌细胞表面的特定蛋白质(抗原),然后引导改造后的免疫细胞精准地锁定并攻击癌细胞。CAR-T细胞疗法在治疗血液肿瘤(如急性淋巴细胞白血病、弥漫性大B细胞淋巴瘤等)方面取得了惊人的成功,很多患者因此获得了长期缓解甚至临床治愈。然而,面对实体瘤,CAR-T和CAR-NK疗法却遭遇了瓶颈,主要原因就是它们难以有效克服上述实体瘤的复杂防御机制,包括浸润困难、免疫耗竭和肿瘤微环境的强烈抑制。这使得如何在实体瘤领域复制血液肿瘤的成功,成为摆在科学家面前的一道难题。
Nature重磅突破:OR7A10基因赋能CAR-NK细胞
正是为了攻克实体瘤这一世界性难题,耶鲁大学的科学家们付出了长达五年多的不懈努力,致力于设计出一种能够有效对抗实体瘤的免疫细胞。他们的目标是找到一种方法,能真正“增强”免疫细胞,使其不仅能精准识别癌细胞,还能有效地深入肿瘤内部,并持续作战而不“疲惫”。
OR7A10的发现:从数万基因中脱颖而出
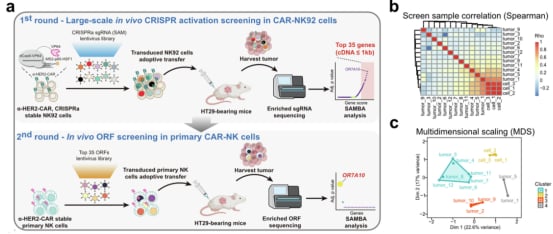
这项发表在国际顶尖学术期刊《自然》杂志上的突破性研究,首先进行了一项系统性的基因筛选工作。研究团队利用先进的基因编辑技术,对数万个基因进行了扫描,旨在识别出哪些基因的引入能够显著改善自然杀伤(NK)细胞在小鼠模型中的肿瘤控制能力。经过严谨而漫长的筛选和验证过程,一个此前并不为人熟知、名为OR7A10的基因最终脱颖而出,成为了最有力的候选者。这个基因属于一个叫做“嗅觉受体”的基因家族,但在这里,它的作用却远超嗅觉,而是展现出令人意想不到的抗肿瘤潜力。
惊人的临床前数据:乳腺癌模型中100%肿瘤消除
在发现OR7A10基因后,研究人员立即通过将这个基因添加到人类NK细胞中,并针对几种类型的癌细胞进行测试,以验证其增强效果。随后,他们在多个实体瘤小鼠模型中进一步验证了其效果,这些模型涵盖了多种高发且难治的实体瘤类型,包括乳腺癌、结肠癌和卵巢癌。结果令人振奋,远远超出了科学家的预期:
- 经过OR7A10基因改造的CAR-NK细胞,相比于未经改造的标准CAR-NK细胞,表现出强大得多的肿瘤控制能力。这意味着,它们能更有效地抑制肿瘤生长,甚至使其缩小。
- 在一个尤为关键的乳腺癌模型中,所有接受治疗的小鼠(100%)都经历了完全的肿瘤消除。这意味着,在这些实验小鼠体内,肿瘤完全消失了,并且在后续观察中没有复发迹象。这在实体瘤治疗中是极其罕见的成就,通常只有在血液肿瘤治疗中才能见到如此高的完全缓解率。
耶鲁医学院遗传学和神经外科副教授Sidi Chen对此充满信心,他表示:“突然之间,这些NK细胞开始对实体瘤起作用了。我们真的相信这种疗法在患者身上具有巨大潜力。”这项突破性研究目前已扩展到靶向脑癌和甲状腺癌等其他实体瘤类型,并且Chen教授表示,他希望在未来几年内启动人体临床试验,将这一有望彻底改变实体瘤治疗格局的突破性疗法从实验室推向患者,为无数深受实体瘤折磨的生命带来新的希望。
OR7A10如何“激活”CAR-NK细胞?探秘其作用机制
这项耶鲁大学的突破性研究最引人注目之处,便是发现了OR7A10这个关键基因。那么,这个神秘的OR7A10基因究竟是如何让CAR-NK细胞变得如此强大,能够有效对抗实体瘤的呢?尽管其完整的作用机制仍在深入研究中,但现有数据和科学推测已为我们揭示了一些关键的分子和细胞层面的增强策略:
- 提升对肿瘤的“靶向识别”与“杀伤效率”:OR7A10可能通过某种机制,优化了CAR-NK细胞与肿瘤细胞之间的结合效率,或者增强了NK细胞启动细胞毒性反应的“扳机”信号。这意味着,当CAR-NK细胞遇到癌细胞时,它们能够更迅速、更精准地锁定目标,并更有效地释放穿孔素和颗粒酶等细胞毒性分子,这些分子就像“微型炸弹”,能够直接在癌细胞膜上打孔,诱导其死亡。研究中,科学家测量了肿瘤杀伤能力、细胞因子产生、耗竭标志物、代谢活性以及对免疫抑制条件的抵抗等多个指标,结果显示OR7A10在多个层面都显著增强了NK细胞的功能。
- 增强“火力输出”——促进细胞因子产生:CAR-NK细胞在攻击肿瘤时,不仅直接杀伤,还会释放一系列细胞因子,如干扰素-γ(IFN-γ)和肿瘤坏死因子-α(TNF-α),这些分子能够募集其他免疫细胞,放大免疫反应,并直接抑制肿瘤生长。研究表明,OR7A10的引入,显著增强了CAR-NK细胞分泌这些关键抗肿瘤细胞因子的能力,从而形成更强大、更持久的抗癌火力,将局部免疫抑制环境转化为抗肿瘤的战场。
- 抵御“免疫耗竭”——维持持久战斗力:实体瘤微环境是免疫抑制的“温床”,长时间暴露于肿瘤抗原和抑制性信号中,免疫细胞会逐渐失去活性,进入“耗竭”状态,如同战场上的士兵精疲力尽。研究发现,OR7A10有助于CAR-NK细胞抵抗这种耗竭,可能通过调控细胞内部的信号通路,使其能够长时间保持活力和杀伤力,延长其在肿瘤微环境中的生存和功能时间,持续对肿瘤进行打击。
- 优化“能量供给”——提升代谢活性与适应性:癌细胞通常具有异常的代谢特征,它们会积极争夺葡萄糖等营养物质,导致肿瘤微环境中的营养匮乏和缺氧。OR7A10可能通过某种方式优化了CAR-NK细胞的代谢活动,使其能够更有效地利用有限的资源,在肿瘤微环境这种恶劣条件下,仍能高效工作并维持其正常的生理功能,如同为细胞配备了更高效的“能量转化器”。
- 克服“免疫抑制”——增强对不利条件的抵抗:实体瘤会产生多种免疫抑制分子,如PD-L1等,这些分子能与免疫细胞表面的受体结合,发出“停止攻击”的信号。OR7A10的引入,可能帮助CAR-NK细胞更好地应对这些抑制信号,甚至直接或间接减弱肿瘤微环境的免疫抑制作用,从而在不利条件下也能坚定不移地发挥抗肿瘤作用。
简而言之,OR7A10基因的作用就像是为CAR-NK细胞提供了一个全面的“升级包”。它不仅增强了细胞的识别和杀伤肿瘤的能力(精准打击),还提升了其“火力输出”和“战场适应性”(持久作战),并赋予了它们更强的“抵抗力”(抵御耗竭和免疫抑制)。这种多维度、协同的功能增强,正是其在实体瘤治疗中取得惊人效果的关键所在。科学家们将继续深入研究OR7A10的具体分子机制,以期未来能更精准地利用这一基因,开发出更安全、更有效的实体瘤治疗方案。
“即用型”疗法前景广阔:惠及更多实体瘤患者
这项突破性研究不仅在疗效上取得了显著进展,更重要的是,OR7A10强化的CAR-NK细胞疗法在实际应用中展现出巨大的优势,尤其体现在“即用型”(Off-the-shelf)治疗的前景上,有望惠及更广泛的实体瘤患者群体。Sidi Chen教授指出,这种潜在的新疗法具有以下主要好处:
- 更高的安全性,减少严重副作用风险:相比于CAR-T细胞疗法,CAR-NK细胞疗法通常被认为具有更好的安全性。CAR-T细胞在攻击肿瘤的同时,可能导致严重的炎症反应,即细胞因子释放综合征(CRS)和神经毒性(ICANS),这要求患者在治疗后必须在重症监护室进行严密监测。而CAR-NK细胞通常不会引起如此剧烈的炎症反应,或者说其副作用更轻微、更易管理。这使得患者更容易耐受治疗,也降低了治疗的整体风险。此外,CAR-NK细胞在体内不会像CAR-T细胞那样持续增殖,通常会随着时间被清除,这进一步降低了长期副作用的风险。
- “即用型”制备,实现标准化与快速响应:这是CAR-NK疗法,尤其是经过优化的CAR-NK疗法,相较于CAR-T疗法的一大显著优势。CAR-T疗法通常需要从每位患者身上单独采集T细胞,然后在体外进行复杂的基因改造和扩增,这一过程耗时数周,且成本高昂。而CAR-NK细胞可以从健康的供体(如脐带血、诱导多能干细胞等)中获取,进行基因改造和扩增后,制备成标准化的产品批次,储存在细胞库中。当患者需要时,可以直接从细胞库中取出并使用,无需等待,真正实现“即用型”。这种模式大大简化了制备流程,显著降低了生产成本,并能极大缩短患者等待治疗的时间,对于那些病情进展迅速的实体瘤患者而言,意义重大。
- 更广的可及性与普及性:由于制备流程更简单、标准化程度更高、成本更低,OR7A10强化的CAR-NK疗法有望实现“治疗民主化”,让更多有需要的实体瘤患者能够负担并获得这一先进的细胞疗法。目前,CAR-T疗法因其高昂的费用(通常在数十万美元甚至更高)而让许多患者望而却步,而“即用型”CAR-NK的出现,有望打破这一壁垒,让更多普通家庭的患者也能享受到前沿科技带来的益处。
- 克服同种异体排斥反应风险:NK细胞的一大特点是其对同种异体细胞的排斥反应远低于T细胞。这意味着,即使使用的NK细胞来源于非患者本人,也能最大限度地避免或减轻移植物抗宿主病(GVHD)的风险,进一步提升了其作为“即用型”异体细胞疗法的安全性。
这项研究为广大实体瘤患者带来了前所未有的希望。目前,研究正积极向人体临床试验迈进。如果人体试验能重复小鼠模型中的积极结果,那么这无疑将是癌症治疗史上的一座里程碑,有望为数百万饱受乳腺癌、结肠癌、卵巢癌乃至脑癌、甲状腺癌等实体瘤困扰的患者带来根治或长期缓解的可能。我们期待未来这项技术能够尽快从实验室走向临床,点亮更多患者的生命之光。
MedFind与实体瘤患者:信息、希望与行动
对于正与实体瘤抗争的患者及其家属而言,每一次医学上的突破都意味着新的希望。然而,前沿疗法从实验室走向临床,需要漫长的过程,患者如何获取最准确、最及时的信息,并为未来的治疗做好准备,就显得尤为重要。MedFind作为专注于抗癌资讯和患者服务的平台,始终致力于为患者提供最新、最权威的抗癌信息,包括新药研发进展、临床试验招募、国际诊疗指南等。我们深知患者在寻求治疗过程中的焦虑与迷茫,因此,我们将持续关注OR7A10增强CAR-NK细胞疗法的后续研究进展,并及时分享给您。
如果您或您的家人正面临实体瘤的挑战,对包括细胞疗法在内的前沿治疗方案有疑问,或者希望了解更多关于跨境购药、海外就医的信息,MedFind平台可以为您提供专业的AI辅助问诊服务,帮助您梳理病情,匹配可能的治疗方案,并协助您构建安全、合法的跨境购药渠道,确保您能及时获得所需的抗癌药物。请记住,医学的进步永不止步,希望之光从未熄灭。保持积极的心态,与专业的团队携手,共同面对挑战。
参考文献
Luojia Yang et al. OR7A10 GPCR engineering boosts CAR-NK therapy against solid tumours, Nature (2026). DOI: 10.1038/s41586-026-10149-8.