艾滋病(获得性免疫缺陷综合征)是全球面临的重大公共卫生挑战,尽管抗逆转录病毒疗法(ART)的出现极大地改善了感染者的生活质量,使其病毒载量降低到检测不到的水平,但“治愈”艾滋病依然是一个世界性难题。其核心障碍在于体内根深蒂固的“潜伏病毒库”——那些隐藏在免疫细胞深处的HIV病毒,ART药物难以触及。这些潜伏病毒就像埋藏在地下的“定时炸弹”,一旦停止服药,病毒就会卷土重来。然而,近期一项发表在国际顶尖医学期刊《Nature Medicine》上的突破性研究,为我们描绘了一幅激动人心的未来图景:原本用于治疗癌症的免疫“神药”——PD-1抑制剂,竟然能够跨界重编程抗病毒免疫反应,显著减少HIV病毒库。这一发现不仅为艾滋病治疗带来了全新的希望,也深刻揭示了个体内在免疫状态在决定治疗反应中的关键作用。作为专注于前沿抗癌与抗病毒资讯的MedFind平台,我们深知患者及家属对新疗法的渴望与期待,特此为您深度解析这项划时代的研究成果。
艾滋病治疗的困境:为何HIV病毒难以彻底清除?
HIV病毒主要攻击人体的免疫系统,特别是CD4+ T细胞,这些细胞是免疫系统的“指挥官”,负责协调全身的免疫防御。当HIV病毒感染CD4+ T细胞后,它们不仅在体内大量复制,还会有一部分病毒悄悄地整合到宿主细胞的基因组中,进入一种“休眠”状态,形成所谓的“潜伏病毒库”。抗逆转录病毒疗法(ART)虽然能高效抑制活跃复制的HIV病毒,使其在血液中的载量降至极低,但对这些处于休眠状态的潜伏病毒却束手无策。这些潜伏病毒主要存在于表达PD-1蛋白的CD4+ T细胞中,它们就像披着隐身衣的敌人,ART药物无法识别和清除。因此,艾滋病患者需要终身服药,一旦停药,潜伏病毒就会被重新激活,导致病毒反弹,疾病进展。
抗癌“神药”跨界:PD-1抑制剂与HIV病毒库的新发现
PD-1抑制剂属于免疫检查点抑制剂,这类药物在近十年间彻底改变了癌症治疗的格局。它们通过解除免疫系统中的“刹车机制”——PD-1通路,重新激活T细胞的抗肿瘤活性。有趣的是,临床上早就观察到,那些同时患有癌症和艾滋病的患者在接受PD-1抑制剂治疗后,除了肿瘤缩小,部分患者的HIV病毒库也出现了意想不到的减少。这一现象引发了科学界的广泛关注:PD-1抑制剂是否也具备清除HIV病毒库的潜力?以及,为什么并非所有患者都能获益?
正是在这样的背景下,埃默里大学的研究人员于2026年2月12日在《Nature Medicine》上发表了题为“Innate antiviral and immune functions associated with the HIV reservoir decay after anti-PD-1 therapy”的研究论文。这项研究深入探讨了PD-1抑制剂(如帕博利珠单抗)如何影响HIV病毒库,并试图找出决定疗效的关键因素。
PD-1抑制剂如何“唤醒”抗病毒免疫系统?
要理解PD-1抑制剂如何对HIV“下手”,首先要了解PD-1蛋白的作用。PD-1(程序性死亡受体-1)是T细胞表面的一种重要免疫检查点蛋白,它就像免疫系统的一个“刹车”,在正常情况下,PD-1与癌细胞或病毒感染细胞表面的PD-L1(PD-1配体)结合,可以避免免疫系统过度激活,损伤正常组织。然而,癌细胞和HIV病毒却很“聪明”,它们会高表达PD-L1,踩下T细胞的“刹车”,让免疫细胞“熄火”,从而逃避免疫系统的攻击。而PD-1抑制剂的作用,正是要松开这个“刹车”,让T细胞重新“启动”,恢复其杀伤功能。
研究团队想知道,当这个免疫“刹车”被松开时,除了攻击癌细胞,我们的身体是否也能更有效地清除那些潜伏的HIV病毒库?通过一项名为CITN-12的临床试验,研究人员对30名同时患有癌症和HIV感染的患者进行了探索性纵向多组学分析,旨在全面了解PD-1抑制剂(特别是帕博利珠单抗)治疗后患者体内免疫状态的变化。

免疫“总动员”:从I型干扰素到CD8+ T细胞的联动效应
研究结果令人振奋!答案是肯定的,但在机制上远比想象的复杂和精妙。当PD-1抑制剂发挥作用后,研究人员观察到了一场快速而持久的内部“抗病毒总动员”:
- I型干扰素的“警报”拉响:在接受PD-1抑制剂治疗后短短24小时内,患者体内的I型干扰素水平就迅速升高。I型干扰素是一种强大的“警报信号”,是身体对抗病毒感染的第一道防线,它能迅速唤醒免疫系统进入“战备状态”。
- “抗病毒武器库”被激活:这个“警报”的拉响,随即激活了一整套名为“干扰素刺激基因”(ISG)的“抗病毒武器库”。特别是在一种名为“经典单核细胞”的免疫哨兵中,这些基因被大量激活。单核细胞是先天免疫系统的重要组成部分,它们能识别并吞噬病原体,同时还能将抗原信息呈递给T细胞,启动适应性免疫反应。
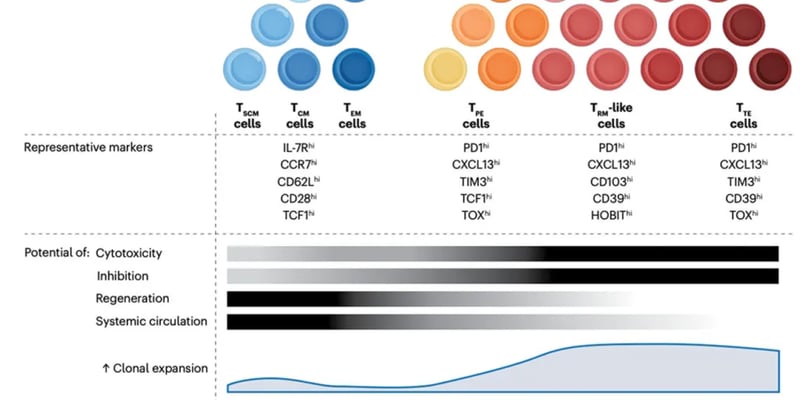
- “杀手部队”集结:紧接着,另一批更具针对性的“杀手”被动员起来。HIV特异性CD8+ T细胞(免疫系统的主力杀伤部队)开始显著增殖,变得更加活跃,这些细胞能够识别并清除被HIV感染的细胞。PD-1抑制剂的“松刹车”效应,使得这些被长期抑制的T细胞得以重获自由,像训练有素的士兵一样,准备定点清除那些被重新唤醒、暴露了踪迹的HIV感染细胞。
这场迅捷而强劲的免疫风暴,在治疗结束时结出了实实在在的果实:在被跟踪到治疗结束的14名患者中,有9人的HIV病毒库出现了显著下降。这有力地证明,通过PD-1抑制剂解除免疫抑制,确实能有效缩小HIV病毒潜伏的“堡垒”。
解码“幸运儿”:预先免疫状态是关键预测因子
然而,为什么只有一部分人能够获益,成为“幸运儿”呢?这个问题的答案,或许比疗法本身更具颠覆性,因为它指向了“个体化精准治疗”的核心。
通过详尽的基因图谱分析,研究人员将所有参与者分成了两组:
- 高应答组:HIV病毒库在治疗后显著减少的患者。
- 低应答组:HIV病毒库变化不大的患者。
惊人的是,这两组人的关键差异,在治疗开始前就已经存在!
研究发现,在高应答组的患者中,其免疫系统在治疗开始前就呈现出一种独特的“战备状态”:他们的先天免疫细胞(特别是单核细胞)中,干扰素相关抗病毒基因模块和Toll样受体信号通路的“活性基线”就更高。可以理解为,这些患者的免疫系统里,抗病毒的“预警雷达”本就处于更高等级的待机状态,对病毒的感知能力更强,反应更迅速。当PD-1抑制剂这根“引线”被点燃时,本就处于高级别“战备状态”的高应答组,其抗病毒程序被迅速、猛烈且持久地激活,从而实现了对HIV病毒库的有效打击。反之,低应答组的免疫图谱则显示,一些与细胞增殖和免疫抑制相关的“耗竭通路”(例如TGFβ信号转导和WNT信号通路)活性更强,这些通路可能抑制了有效的抗病毒反应,导致免疫系统未能被充分激活。
研究团队还将这一基因标签,与超过1000个公共数据库中的健康人、其他癌症和传染病患者的数据进行比对,发现这种高预警的免疫特征广泛存在于不同疾病状态的人群中。这说明,它并非HIV或癌症所独有,而是一种可能决定个体对免疫疗法反应程度的、普遍存在的基础免疫状态,可以作为预测患者治疗反应的“分子密码”。
这项突破性研究对艾滋病治疗意味着什么?
这项研究为我们描绘了一幅激动人心的未来图景,对艾滋病“治愈”研究和免疫治疗领域都具有里程碑式的意义:
- 1. 个性化精准治愈策略的曙光:通过简单的血液检测,在治疗前分析患者的免疫基因图谱,我们或许就能精准预测谁最有可能从PD-1抑制剂(或其组合疗法)中获益。这避免了对无效人群进行可能带来副作用的治疗,减少了不必要的资源浪费,并能更高效地筛选出最适合该疗法的患者,实现真正的“精准打击”。
- 2. “唤醒+清除”联合疗法的新思路:该研究验证了通过解除免疫抑制来“唤醒”潜伏病毒,同时激活强大的先天和后天免疫应答来“清除”被感染细胞的可行路径。这为未来设计更有效的组合疗法提供了坚实的科学依据,例如,将PD-1抑制剂与I型干扰素或其他能够进一步增强免疫激活的药物联用,或许能更彻底地清除病毒库。
- 3. 从偶然到必然的治愈之路:这些研究为HIV治愈研究提供了一个清晰的分子标签。未来的努力方向,可能是寻找更安全有效的方法,将低应答者的免疫状态“重编程”为高应答状态,或直接为高应答者“量身定制”治愈方案。通过深入理解决定治疗反应的内在免疫机制,我们有望从根本上解决艾滋病“治愈”的难题。
- 4. 拓宽免疫治疗的应用前景:虽然这项研究的人群是同时患有癌症的HIV感染者,但其核心发现——“个体内在的免疫状态是决定治疗反应的关键”——无疑为艾滋病治疗乃至整个免疫治疗领域,开辟了一条极具前景的新战线,可能影响其他慢性感染性疾病甚至自身免疫病的治疗策略。
尽管这项研究仍处于早期阶段,且是在癌症合并HIV感染的患者中进行的,其样本量相对较小,但其揭示的免疫机制和预测因子,无疑是艾滋病治愈研究领域的一大突破。它提醒我们,人体自身的免疫系统蕴藏着巨大的抗病潜力,而科学家的任务就是找到开启这些潜力的“钥匙”。
MedFind助您获取前沿抗癌与抗病毒药物资讯
面对艾滋病和癌症的严峻挑战,每一次科学的突破都为患者和家属带来了新的希望。在MedFind,我们深知信息的重要性,致力于为您提供最新、最全面、最权威的抗癌与抗病毒药物资讯、诊疗指南和临床研究进展。我们不仅分享前沿医学知识,更希望能搭建起患者获取创新疗法的桥梁。如果您对这项研究或其他抗癌/抗病毒药物有任何疑问,或者正在寻找更个性化的治疗方案,欢迎通过MedFind的AI辅助问诊功能,获取专业指导和支持。我们愿与您并肩,共同探索生命的无限可能。
参考文献
- Nature Medicine: Innate antiviral and immune functions associated with the HIV reservoir decay after anti-PD-1 therapy. Published: 2026-02-12. DOI: https://www.nature.com/articles/s41591-025-04139-y