肝癌治疗的“双效”新靶点——SOAT1
肝癌因其高异质性和快速进展的特性,一直是医学界面临的重大挑战。传统的治疗方案效果有限,而寻找能够同时打击肿瘤代谢和免疫逃逸的新靶点,成为突破治疗瓶颈的关键。近日,国际权威期刊《Hepatology》上的一项研究为肝癌治疗带来了新希望。
香港大学的研究团队发现,胆固醇酰基转移酶1(SOAT1)在肝癌组织中显著高表达,并且其高表达水平与患者的不良预后,如静脉侵犯、晚期肿瘤和更短的生存期密切相关。这表明,SOAT1不仅是肝癌的一个代谢弱点,更是一个极具潜力的治疗靶点。

图1. 研究证实SOAT1在肝细胞癌中高表达
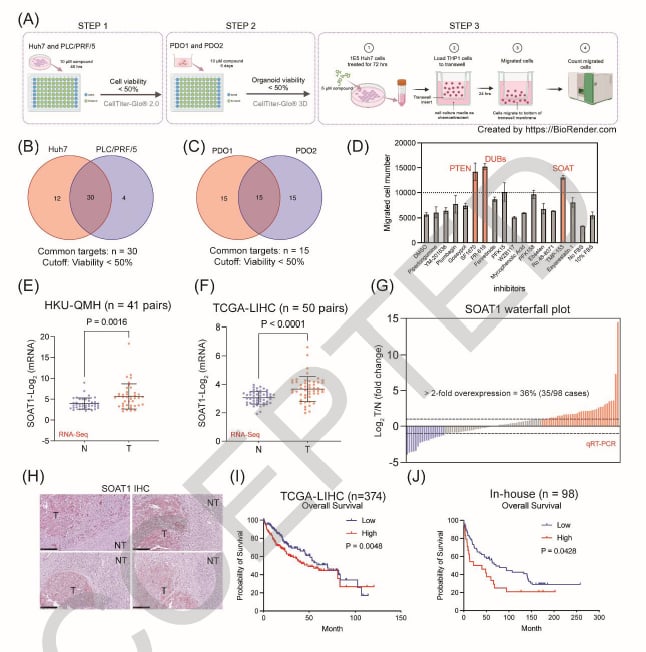
图2. SOAT1对肝细胞癌的发生和恶性程度至关重要
抑制SOAT1:重塑代谢与激活免疫的双重打击
研究人员通过基因编辑或使用SOAT1抑制剂阿伐西米布(Avasimibe)进行干预,发现能够显著减缓肝癌细胞的增殖速度,并抑制患者来源类器官的生长。那么,抑制SOAT1是如何实现抗癌效果的呢?
- 代谢重塑:抑制SOAT1会打破癌细胞内的代谢平衡,导致长链脂肪酸等物质堆积,引发“脂质毒性”,并使细胞产生大量活性氧,最终诱导癌细胞凋亡。
- 免疫激活:更关键的是,这种代谢紊乱会激活一系列信号通路,促使肿瘤释放出多种“招募信号”(如促炎细胞因子),吸引能够杀伤癌细胞的免疫细胞(如CD8+T细胞)浸润到肿瘤内部,将原本免疫细胞难以进入的“冷肿瘤”转变为易于攻击的“热肿瘤”。
对于肝癌患者而言,这意味着一种全新的治疗思路。如果您想了解更多关于肝癌前沿疗法或需要海外靶向药代购服务,MedFind可以为您提供专业的支持。
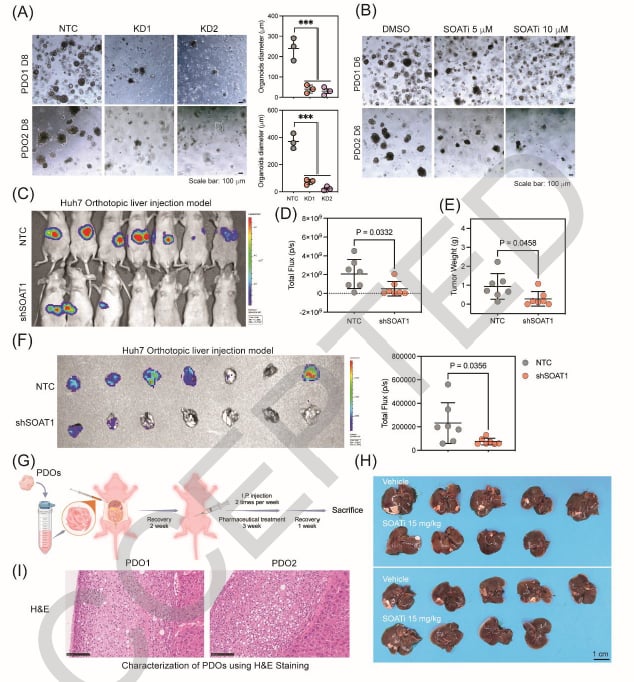
图3. 靶向SOAT1可重编程脂质代谢
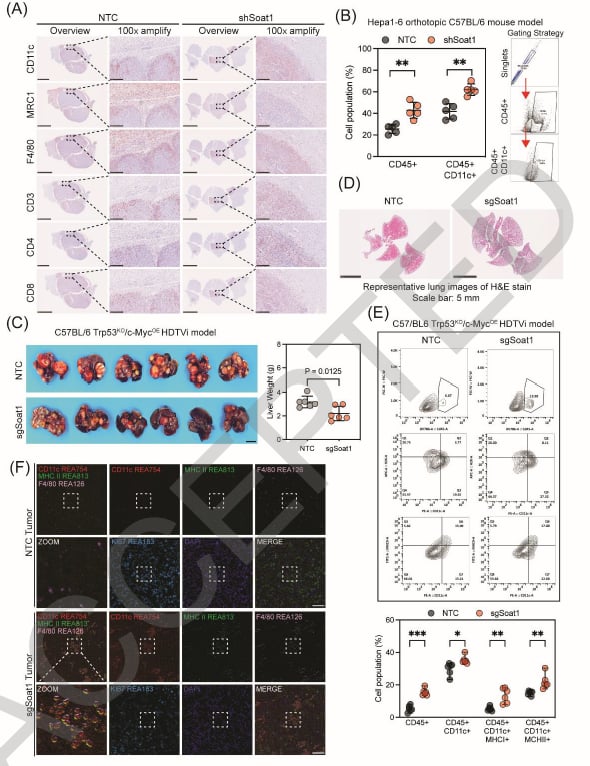
图4. SOAT1调控肿瘤与免疫系统的相互作用
强强联合:SOAT1抑制剂与PD-1疗法协同增效
研究最令人振奋的发现,在于联合治疗的巨大潜力。当研究人员在肝癌小鼠模型中,将阿伐西米布与抗PD-1抗体(一种主流的免疫检查点抑制剂)联合使用时,观察到了远超单一疗法的抑瘤效果。
这种协同效应的原理在于:SOAT1抑制剂首先改善了肿瘤的免疫微环境,为免疫细胞的进攻扫清了障碍;随后,PD-1抑制剂解除了免疫细胞自身的“刹车”,使其能够全力攻击并清除癌细胞。这种“1+1>2”的效果,显著缩小了肿瘤体积,降低了肿瘤负荷。
这种“代谢+免疫”的双重打击策略,为肝癌治疗开辟了新的道路。若您对自己的病情或治疗方案有疑问,可以尝试MedFind的AI问诊服务,获取个性化的参考信息。
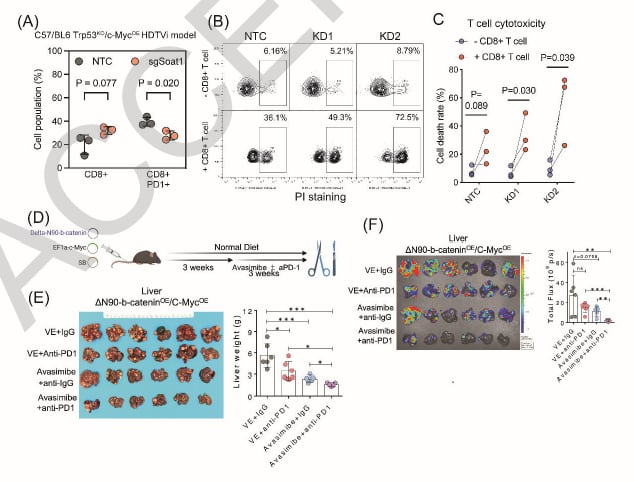
图5. 抑制SOAT1可增强CD8+T细胞毒性并与抗PD-1免疫治疗协同作用
老药新用,为肝癌患者带来新希望
值得一提的是,阿伐西米布是一款最初用于治疗动脉粥样硬化的药物。本次研究发现其在肝癌治疗中的新用途,属于“老药新用”,这有望大大缩短其进入临床应用的时间和成本。对广大肝癌患者来说,“SOAT1抑制剂 + PD-1抑制剂”的组合疗法,有望同时解决肿瘤代谢依赖和免疫逃逸两大难题,为克服耐药、改善预后提供了切实可行的新希望。更多关于肝癌的最新药物信息和诊疗指南,欢迎访问MedFind资讯中心。





