癌症治疗领域正不断探索创新策略,其中铁死亡作为一种独特的非凋亡性程序性细胞死亡方式,展现出巨大的潜力。与传统细胞死亡机制不同,铁死亡不受常见肿瘤突变的影响,并且能够诱导肿瘤细胞发生免疫原性死亡,从而有效激活机体的抗肿瘤免疫治疗反应。然而,现有铁基纳米材料在肿瘤部位的特异性聚集能力和生物相容性方面仍面临挑战,可能对正常组织产生“脱靶”毒性。因此,开发能在肿瘤微环境中精准响应的铁基纳米制剂,对于提升癌症治疗效果至关重要。
在此背景下,树枝状介孔有机硅(DMOS)纳米粒子因其独特的结构优势而备受关注。它们拥有较大的孔体积和孔径,以及出色的生物降解性和生物相容性,使其成为药物递送的理想载体。更值得一提的是,DMOS纳米粒子可通过引入二硫键等功能基团,在谷胱甘肽(GSH)作用下快速降解,并有效消耗肿瘤细胞内过量表达的GSH,这对于诱导铁死亡至关重要。尽管DMOS在癌症治疗中多作为载体使用,但将其本身开发为治疗试剂的研究尚属少数。
近期,哈尔滨工程大学杨飘萍教授团队在国际权威期刊《Advanced Materials》上发表了一项突破性研究。他们成功合成了Fe3+掺杂枝状介孔有机硅(Fe-DMOS)纳米粒子,并将其作为一种新型铁死亡诱导剂。这项研究深入阐明了Fe-DMOS在透明质酸修饰的过氧化钙(CaO2-HA)纳米粒子以及免疫检查点抑制剂(如anti-PD-1)的协同作用下,如何有效诱导肿瘤细胞铁死亡,激活强大的抗肿瘤免疫响应,并最终抑制癌症的生长、转移及复发。这一发现为癌症免疫治疗带来了新的希望。

Fe-DMOS@CaO2-HA纳米复合物:精准靶向与协同增效
研究团队巧妙利用Fe3+与模板剂的配位作用,成功构建了具有独特枝状介孔结构的Fe-DMOS纳米粒子。这些纳米粒子粒径适中,孔径可观,能够高效负载小颗粒CaO2-HA纳米粒子,形成均匀的Fe-DMOS@CaO2-HA纳米复合物(图1)。该复合物的精妙之处在于其对肿瘤微环境的智能响应:Fe3+与二硫键的协同作用使其在酸性和高GSH环境下迅速降解,释放大量Fe3+并显著降低细胞内GSH水平。同时,负载的CaO2-HA在酸性条件下释放Ca2+和过氧化氢(H2O2)。关键在于,释放的Fe3+能通过芬顿反应催化H2O2生成大量剧毒的·OH自由基(图2),这是诱导铁死亡的核心机制。
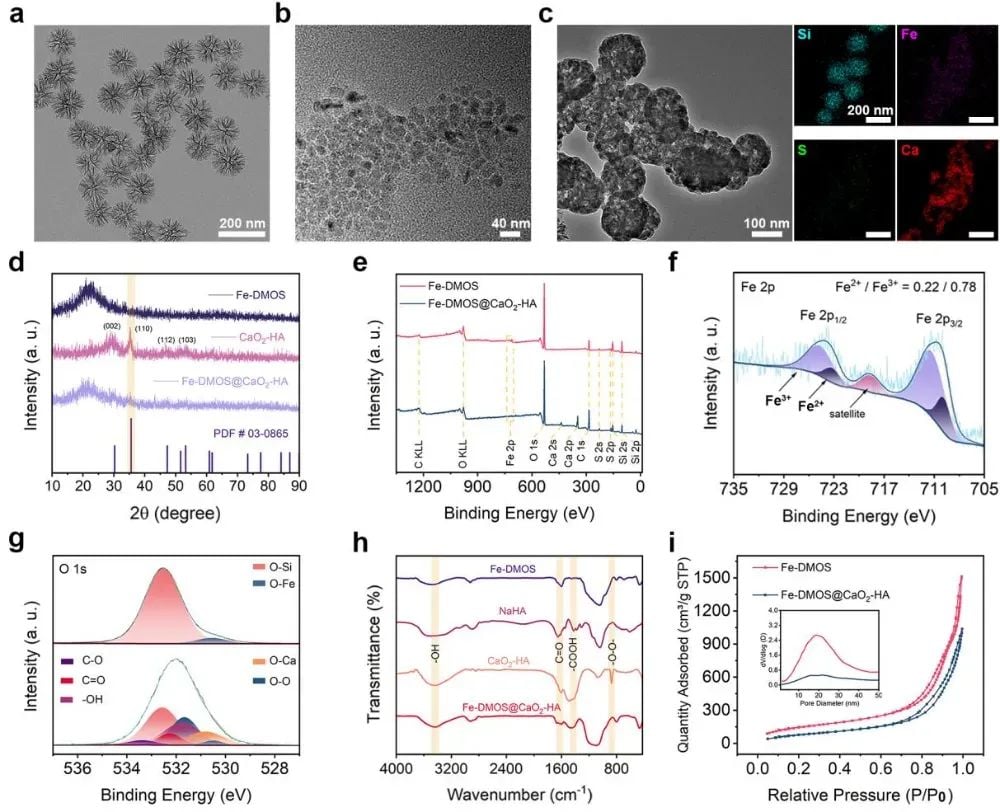
图1 Fe-DMOS@CaO2-HA纳米复合物的合成与表征
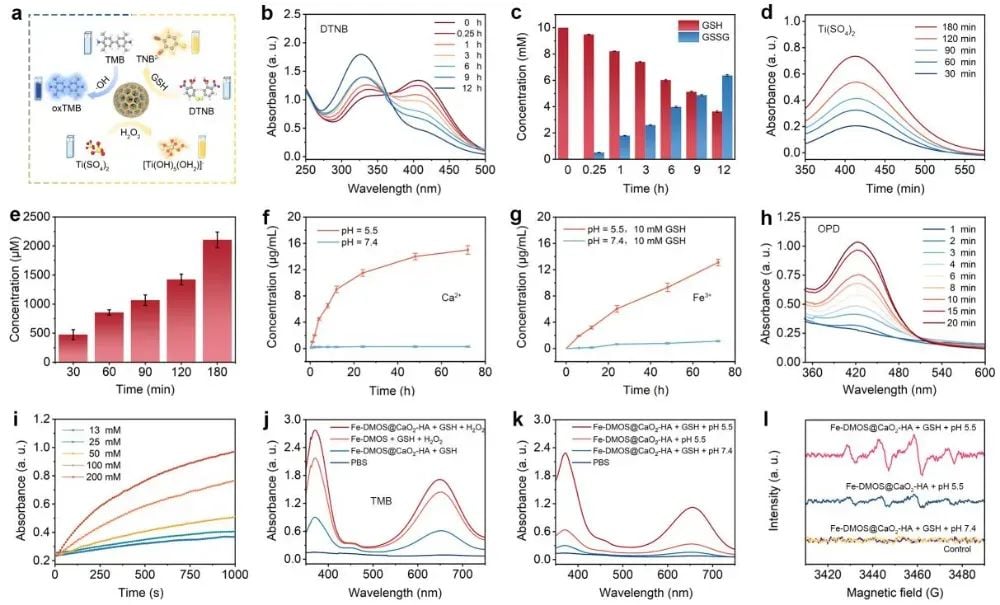
图2 Fe-DMOS@CaO2-HA纳米复合物酸及GSH双响应降解、GSH消耗、H2O2自补偿及·OH生成等性能测试
体外实验验证:高效杀伤肿瘤细胞并激活免疫
为评估Fe-DMOS@CaO2-HA纳米复合物的治疗潜力,研究团队进行了全面的体外细胞实验。结果显示,由于透明质酸的修饰,该纳米复合物能有效靶向并被肿瘤细胞吞噬,同时对正常细胞毒性不明显。深入机制研究表明,被吞噬后,复合物在肿瘤细胞内释放Fe3+、Ca2+并生成H2O2,通过芬顿反应产生大量·OH自由基。Ca2+过载和·OH的协同作用导致线粒体损伤,ATP生成受阻,最终显著杀伤肿瘤细胞(图3)。
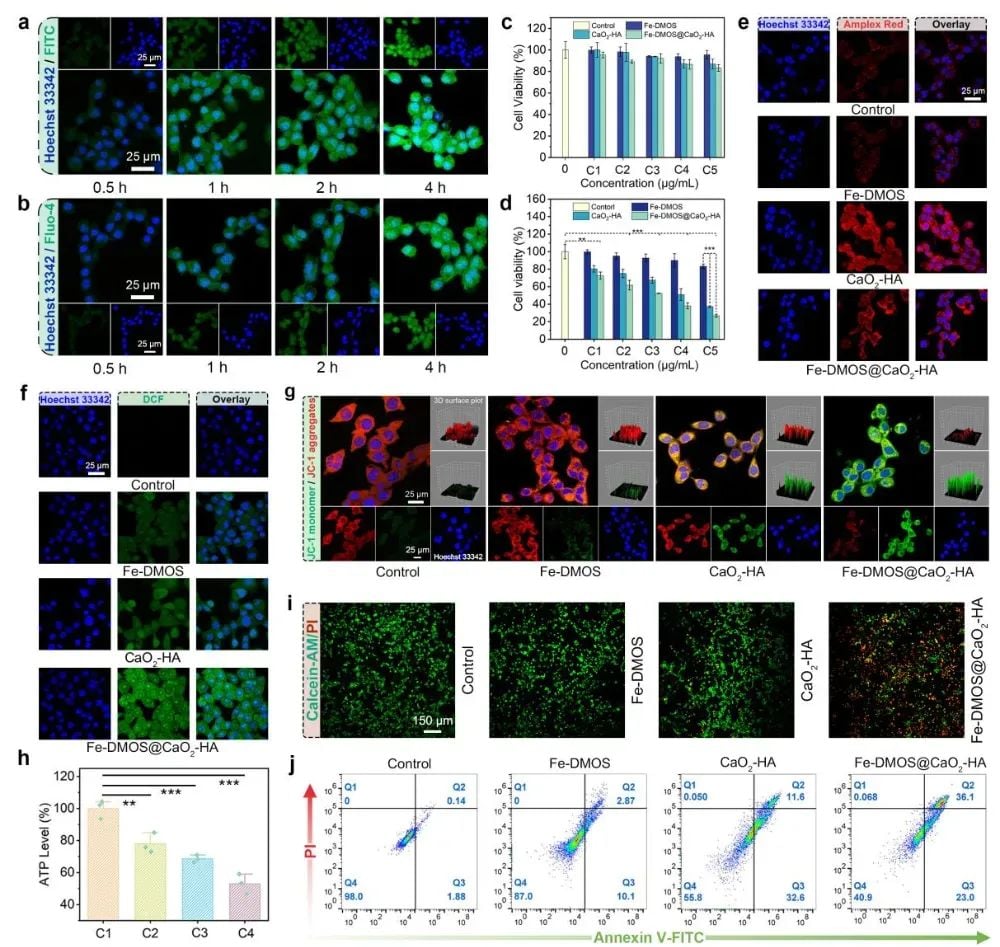
图3 Fe-DMOS@CaO2-HA纳米复合物可杀伤肿瘤细胞
更重要的是,Fe3+和二硫键的存在有效降低了肿瘤细胞内高表达的GSH,并下调了谷胱甘肽过氧化物酶4(GPX4)的表达,从而显著促进脂质过氧化物的积累,最终诱导肿瘤细胞发生铁死亡。这项研究还揭示,Fe-DMOS介导的铁死亡并非“静默死亡”,而是能引发肿瘤细胞的免疫原性死亡(ICD)。死亡的肿瘤细胞会暴露钙网蛋白(CRT),并释放HMGB1和ATP等“危险信号分子”(图4),这些信号能被树突状细胞(DCs)识别并促进其成熟,进而分泌大量促炎细胞因子(如TNF-α和IL-6),有效激活抗肿瘤免疫响应。
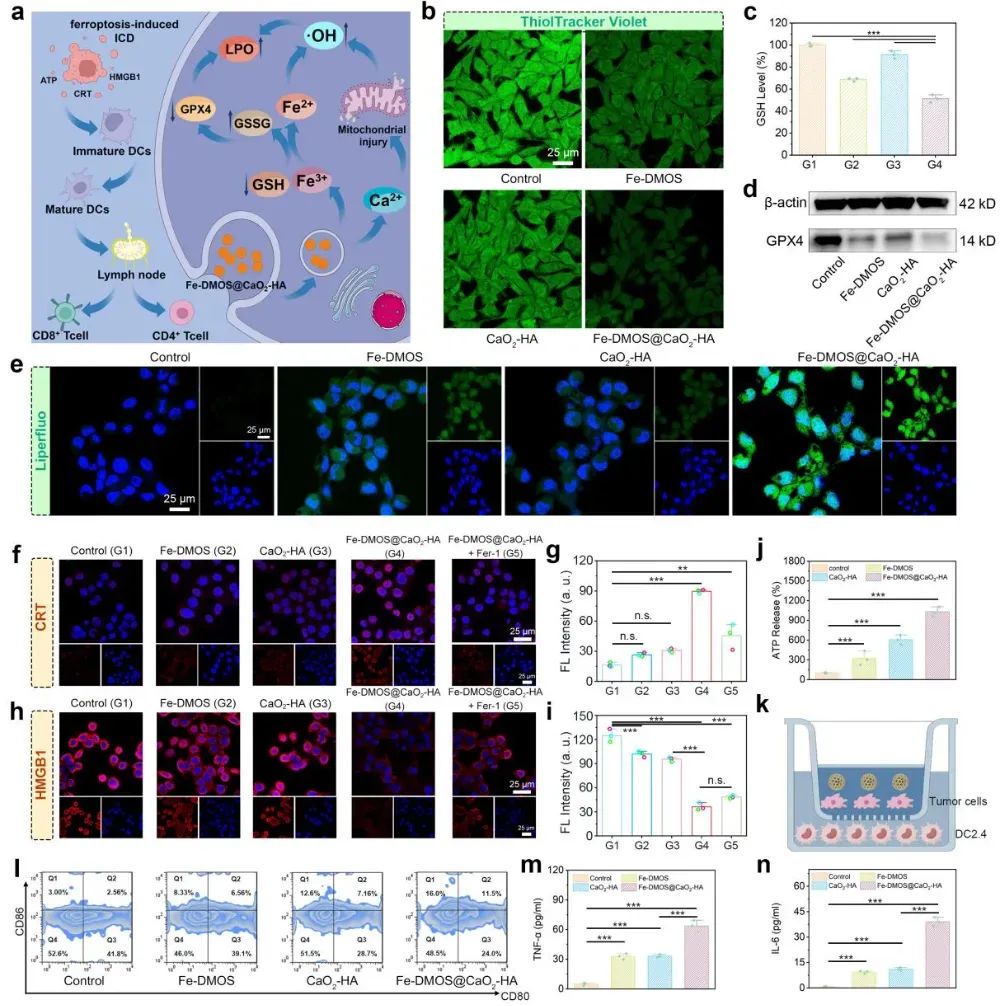
图4 Fe-DMOS@CaO2-HA纳米复合物诱导肿瘤细胞铁死亡并引发免疫原性死亡
体内研究:协同anti-PD-1,全面抑制肿瘤生长与转移
为了在活体层面验证其疗效,研究团队构建了双侧小鼠荷瘤模型。结果令人鼓舞:静脉注射Fe-DMOS@CaO2-HA纳米复合物后,其能在肿瘤部位高效积累,并展现出良好的生物相容性。治疗后,荷瘤小鼠的原发瘤和远端瘤生长均受到显著抑制。更重要的是,当纳米复合物与免疫检查点抑制剂(如anti-PD-1)联合使用时,肿瘤抑制效果达到最佳,显著延长了荷瘤小鼠的生存期。
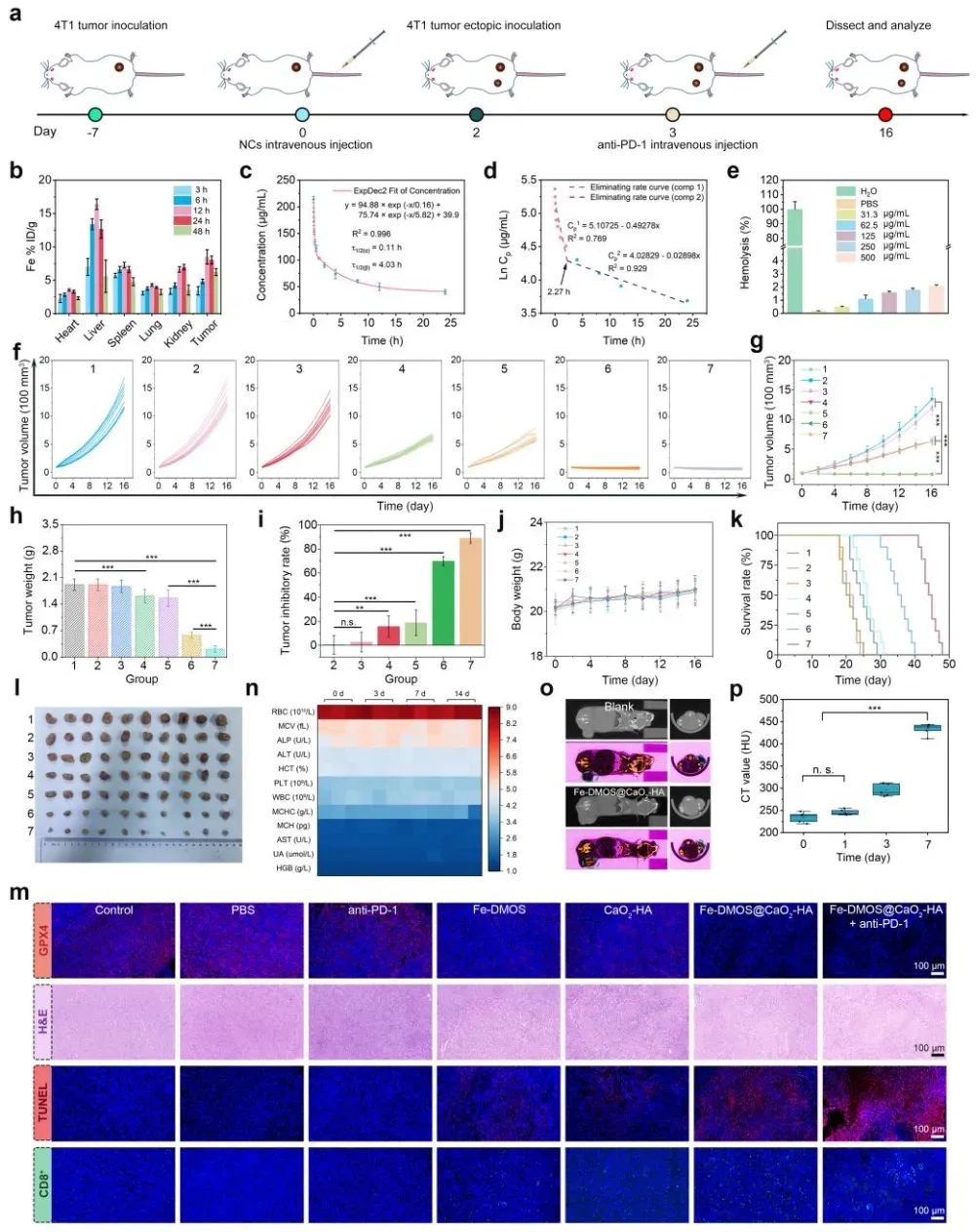
图5 Fe-DMOS@CaO2-HA纳米复合物联合anti-PD-1抑制肿瘤生长
CT图像显示,由于Ca2+过载导致的肿瘤细胞钙化,肿瘤部位呈现出清晰的成像效果。组织切片染色进一步证实,Fe-DMOS@CaO2-HA纳米复合物联合anti-PD-1能有效诱导肿瘤细胞铁死亡,同时提高CD8+ T细胞在肿瘤部位的浸润(图5)。此外,联合治疗显著提升了脾脏和淋巴结中DCs的成熟度,这些成熟的DCs能将肿瘤抗原呈递给CD8+和CD4+ T细胞,从而激活特异性抗肿瘤免疫响应。
值得注意的是,免疫检查点抑制剂(anti-PD-1)在此联合治疗中发挥关键作用,它能有效阻断肿瘤细胞通过PD-L1与T细胞PD-1结合而产生的免疫逃逸机制,使得被激活的T细胞能够持续攻击肿瘤细胞。实验数据显示,联合治疗后,肿瘤部位CD8+ T细胞和CD4+ T细胞积累量大幅增加,记忆T细胞比例也显著提高,这有效预防了肿瘤的转移与复发,在肺转移模型中未观察到明显的转移灶(图6)。

图6 Fe-DMOS@CaO2-HA纳米复合物联合anti-PD-1抑制肿瘤转移
对于正在寻求创新癌症治疗方案的患者,了解这类前沿研究至关重要。如果您需要获取最新的药物信息或诊疗指南,可以访问MedFind抗癌资讯。
结论与展望:纳米材料在肿瘤免疫治疗的新篇章
总而言之,这项研究成功合成了一种新型Fe-DMOS纳米铁死亡诱导剂,并与CaO2-HA纳米粒子结合,形成了高效的纳米复合物。实验结果明确指出,该纳米复合物不仅能有效诱导肿瘤细胞铁死亡并引发免疫原性死亡,更在与anti-PD-1联合治疗时,展现出显著抑制肿瘤生长、转移及复发的能力。这一突破性进展不仅拓宽了硅基纳米材料在癌症治疗中的应用范畴,使其不再局限于单一的药物载体,更为肿瘤的长期免疫治疗提供了极具价值的新策略。
面对复杂的癌症挑战,患者往往需要寻找全球范围内的靶向药和先进疗法。如果您有海外购药需求,MedFind海外靶向药代购服务可以为您提供帮助。同时,您也可以通过MedFind AI问诊服务,获取个性化的治疗建议和信息支持。





