“手术切干净了,还要不要做PD-1/PD-L1免疫治疗?是术前做新辅助更好,还是术后做辅助更稳?”这几乎是可切除非小细胞肺癌、黑色素瘤、肾细胞癌等患者最纠结的核心问题。本文会用患者能听懂的话,把辅助/新辅助/围手术期免疫治疗的原理讲清楚,梳理关键临床试验告诉了我们什么、哪些人更可能获益、为什么有时看不到总生存获益,并重点说明pCR、MPR、ctDNA清除这些“早期信号”如何帮助做决策,以及免疫治疗常见不良反应的居家识别与应对。
一、先把概念说清:辅助、新辅助、围手术期分别在做什么
很多家属把“免疫治疗”当作一个笼统的大类,但在可切除肿瘤里,治疗时机不同,目的完全不同。
1)辅助治疗(术后)
辅助免疫治疗是在肿瘤已经切除后,用药“扫尾”。你可以把它理解为:手术像是把“看得见的杂草”拔掉,而辅助治疗要处理可能残留的“看不见的草籽”(微小转移灶或微小残留病灶),目标是降低复发和远处转移风险。
2)新辅助治疗(术前)
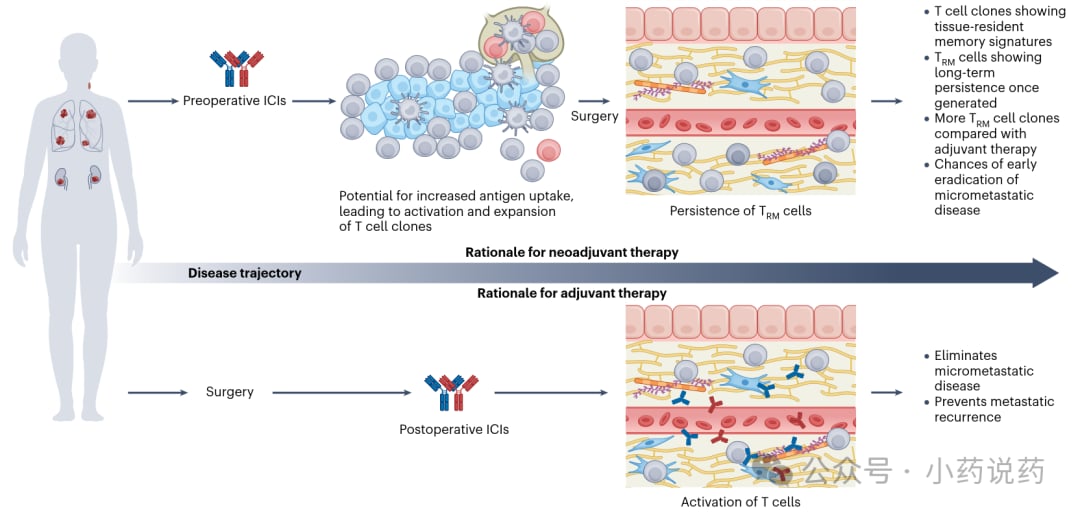
新辅助免疫治疗是在手术前先用药,目标通常是:缩小肿瘤、降低分期、提高R0切除概率,并且更关键的是让免疫系统在“原发肿瘤还在”的状态下被充分“训练”。通俗比喻:让免疫系统在“敌人还在现场”时学习识别敌人特征,形成更强、更持久的“记忆军团”。
3)围手术期治疗(术前+术后组合)
围手术期免疫治疗通常是术前“化疗+免疫”几个周期,术后再把免疫维持到接近一年。它想同时吃到两种策略的红利:术前把免疫效应做强,术后继续降低复发概率。但它也带来一个现实问题:如果患者术前已经反应很好,术后“还要不要继续用满一年”,可能存在过度治疗的风险。
二、免疫治疗为什么在“早期可切除”阶段越来越重要
PD-1/PD-L1抑制剂的核心逻辑是解除免疫刹车,让T细胞重新识别并杀伤肿瘤细胞。在转移期,肿瘤负荷大、免疫抑制微环境强,治疗常常是“对抗消耗战”。在可切除阶段,肿瘤负荷相对小,很多研究观察到:当原发灶仍存在(新辅助或转移期),免疫系统更容易被充分激活,产生更强的全身抗肿瘤免疫反应,从而带来更好的事件控制结局。
但也必须诚实地说:在辅助治疗里,很多试验最先看到的获益是无复发生存(RFS)/无病生存(DFS),而总生存(OS)的改善在不少肿瘤类型中并不“立刻显现”。原因通常包括:随访时间还不够长,以及一旦复发后,转移期仍可再用免疫治疗或其他有效药,导致OS差异被“稀释”。对患者来说,这意味着:辅助免疫治疗的价值常常是“把复发风险往后推、把远处转移概率压下去”,但是否一定能延长寿命,需要更长时间和更精细的人群分层来回答。
三、不同肿瘤的关键证据:哪些结论更“落地”
早期可切除肿瘤中,辅助与围手术期免疫治疗的核心矛盾:复发风险降低更清晰,而OS获益常需更长随访与更精准分层
1)黑色素瘤:免疫治疗的“试验田”,但OS并非总能立刻看到
黑色素瘤之所以常被视为免疫治疗的“理想模型”,与其较高的肿瘤突变负荷(TMB)相关:突变越多,越容易产生更多“异常蛋白”被免疫系统识别为外来物。
在切除后的中高风险人群中,纳武利尤单抗(欧狄沃, Nivolumab)在关键III期研究中可显著改善RFS,并且3-4级不良事件发生率低于伊匹木单抗(逸沃, Ipilimumab)。同时,帕博利珠单抗(可瑞达, Pembrolizumab)也在切除的IIIA-C期患者中证明RFS优于对照(安慰剂或其他方案)。后续研究进一步把人群扩展到IIB/C期(深浸润和或溃疡但无淋巴结转移)患者,显示RFS和远处无转移生存(DMFS)改善。
患者常问:“既然RFS更好,为什么有时看不到OS明显更好?”一个重要现实是:一旦复发进入转移期,PD-1药物仍然常用且有效,后续治疗把两组生存差距拉近了。这并不等于辅助治疗“没用”,而是提示我们:辅助治疗真正的价值往往是降低复发和远处转移发生的概率与时间,而OS需要更长随访或更精准挑选人群才能体现。
2)非小细胞肺癌:从术后辅助到术前新辅助,策略正在快速迭代
非小细胞肺癌(NSCLC)在可切除阶段仍有不低的复发率,文献中常见范围约30%–55%。因此,“术后要不要加治疗”在肺癌里尤其关键。
术后辅助证据方面:IMpower010研究显示,在完全切除、II–IIIA期且PD-L1阳性的NSCLC患者中,辅助阿替利珠单抗(泰圣奇, Atezolizumab)可带来DFS改善。KEYNOTE091(PEARLS)把适用人群扩展到IB–IIIA期、且不限制PD-L1状态,显示辅助帕博利珠单抗改善DFS。但需要患者特别注意的一点是:亚组分析提示,未接受化疗的患者中,疾病进展风险反而增加约25%,这强化了“免疫治疗往往更适合与细胞毒化疗配合”的临床直觉与实践。
术前新辅助证据方面:CheckMate 816研究比较了新辅助化疗联合或不联合纳武利尤单抗用于可切除IB–IIIA期NSCLC。结果显示联合方案显著改善EFS和OS,并把病理完全缓解(pCR)从2.2%提高到24%。对患者来说,pCR意味着手术标本里几乎找不到活的肿瘤细胞,是一个非常强的“早期好信号”。
围手术期探索方面:AEGEAN、KEYNOTE671、Neotorch、CheckMate 77T等III期研究把策略做成“术前化疗+免疫3-4周期 + 术后免疫维持约1年”,整体上可提高pCR和主要病理缓解(MPR)率,并改善EFS。但也有合理批评:对照组通常是术前安慰剂+化疗、术后安慰剂,使得我们很难严格区分获益到底来自术前、术后,还是两者叠加。这也直接引出患者最现实的问题:如果术前已经达到pCR或接近MPR,术后是否必须“继续打满一年”,仍需要更精细的证据支持。
3)肾细胞癌:并非所有免疫药都在术后同样有效
透明细胞肾细胞癌术后辅助免疫治疗中,KEYNOTE564研究显示辅助帕博利珠单抗可改善DFS和OS。在中位随访57.2个月时,帕博利珠单抗组48个月DFS为64.9%,安慰剂组为56.6%。
但对比也同样重要:IMmotion010评估辅助阿替利珠单抗未显示DFS显著改善;CheckMate 914评估纳武利尤单抗联合或不联合伊匹木单抗也未证明DFS改善。原文提示一个关键解释是:不同试验纳入的风险分层不一致,若纳入较低风险患者,整体获益可能被稀释。对患者来说,这提示两点:第一,同一类“免疫治疗”并不意味着术后都等效;第二,是否适合辅助免疫,必须结合复发风险分层,而不是只看“是不是肾癌”。
四、决定“做不做、何时做”的三把钥匙:风险、时机、替代指标
1)为什么有人适合“立刻做辅助”,有人反而可以“推迟”
支持尽早辅助的逻辑:对于复发风险极高的人群,在更可控的“预防性环境”使用免疫治疗,可能更容易把风险压下去,减少远处转移发生。
支持推迟治疗的逻辑也同样合理:在一些相对低风险的可切除分期里,很多患者可能终生不复发,如果所有人都接受一年免疫治疗,会带来不必要的毒性、经济负担与生活质量下降。并且一旦复发,转移期仍可能有免疫治疗、新辅助或围手术期策略可用。
真正的难点是:我们能否提前识别“谁才是真正需要辅助的人”。这就引出了两个越来越被重视的“早期替代标志物”:pCR/MPR与ctDNA清除。
2)pCR/MPR:手术标本里的“即时战报”
pCR(病理完全缓解)可以理解为“标本里找不到活肿瘤细胞”;MPR(主要病理缓解)通常指残余活肿瘤细胞比例非常低。它们的意义在于:比起等待几年观察复发或死亡结局,这些指标更早出现,能帮助我们判断术前方案是否“真有效”。在CheckMate 816中,达到pCR的患者复发率极低,因此很多专家开始思考:对这类反应非常好的人,术后继续免疫是否会出现“收益递减”。
3)ctDNA:血液里寻找“残留信号”的雷达
ctDNA(循环肿瘤DNA)可以类比为肿瘤在血液里掉落的“碎片指纹”。术后如果ctDNA阳性,往往提示存在微小残留病灶风险更高;如果治疗后ctDNA清除,可能意味着复发风险更低。
在IMvigor 011 III期研究中,切除的肌层浸润性膀胱癌患者仅在术后ctDNA阳性时才随机接受阿替利珠单抗或安慰剂,结果显示阿替利珠单抗组DFS和OS均改善。这种“用ctDNA挑人”的设计,对未来的辅助免疫非常重要:它让治疗更接近“该用的人用、可能不需要的人不硬上”。
五、治疗“降阶梯”:疗程一定要12个月吗?
目前多数辅助免疫试验把疗程设为12个月,但这在很大程度上是历史与设计选择,并非已经被随机对照试验证实“12个月一定最佳”。原文也明确指出:尚无随机数据支持缩短疗程,但出现了一些支持“在反应好的患者中缩短可能可行”的线索,例如对新辅助抗PD-1达到MPR的患者似乎长期结局很好;以及在一项前瞻性研究中,使用肿瘤知情ctDNA评估不可切除III期NSCLC巩固免疫缩短疗程,关键时间点ctDNA清除者PFS显著改善。
对患者的现实建议是:如果医生提出“是否需要做满一年”或“是否可以停”,请务必把问题具体化到三个层面再讨论:(1)你的复发风险分层(分期、淋巴结、病理高危因素);(2)你的反应证据(pCR/MPR、ctDNA动态、影像学);(3)你的承受能力(免疫相关不良反应史、基础自身免疫病、生活质量与经济负担)。
六、个性化治疗:生物标志物能帮到什么程度
1)常见标志物:PD-L1、TMB、dMMR/MSI
在转移期,PD-L1表达、TMB、错配修复缺陷(dMMR)或MSI等可作为免疫治疗决策的重要参考。但在辅助环境中,预测获益更难。原文举例:在切除的IB–IIIA期NSCLC中,PD-L1高表达与低表达患者未观察到辅助帕博利珠单抗的差异获益。这提醒我们:早期阶段的免疫生物学可能与转移期不同,不能简单“照搬”。
2)GEP与ctDNA:更接近“复发风险”的工具
基因表达谱(GEP)可能帮助识别高危可切除黑色素瘤患者;ctDNA在识别高危复发患者方面更直观,且可动态监测。对患者来说,ctDNA最大的价值是“随时间变化”:一次阴性不等于永远安全,但持续清除往往是好信号;一次阳性也不等于一定复发,但值得与医生讨论是否需要更积极的辅助或更密集随访。
七、联合策略与“该避开的坑”:并非所有人都适合免疫
1)联合免疫并不总成功
在辅助治疗环境中,联合免疫(如加入伊匹木单抗)并未在所有研究中带来明确的DFS获益。原文提出了一个深层问题:在没有筛选的患者里,去“靶向”微转移病灶的生物学基础可能不同于转移期大肿瘤负荷状态,简单叠加药物不一定更好,反而可能增加毒性。
2)个体化癌症疫苗:前沿方向,但仍需等待更多证据
个体化癌症疫苗(mRNA或多肽新抗原平台)被视为增强抗PD-1活性的方向之一。原文提到mRNA4157(V940)与帕博利珠单抗联合作为切除的IIIB–IV期黑色素瘤辅助治疗,在随机II期试验中较帕博利珠单抗单药改善RFS,提示其潜力。但对患者而言,这仍属于前沿进展,需要关注后续更大规模与更长期的验证。
3)EGFR突变NSCLC:关键提醒
原文明确提出:对于EGFR突变的NSCLC,应引导接受分子靶向药物,例如奥希替尼(泰瑞沙, Osimertinib),而非优先使用免疫治疗。这一点非常重要,因为不同分子亚型对免疫治疗的敏感性差异很大,错误的治疗顺序可能带来更少获益甚至更高风险。后续再出现时:奥希替尼。
八、免疫治疗常见副作用:家属最该会的“早识别、早处理”
免疫检查点抑制剂的不良反应不同于化疗,它更像是“免疫系统被放开后误伤正常组织”,称为免疫相关不良事件(irAEs)。多数可控,但关键在于不要硬扛。
1)需要立刻联系医生或急诊的警报
- 呼吸困难、胸闷、持续干咳加重:警惕免疫相关肺炎。
- 严重腹泻、便血、腹痛:警惕免疫相关结肠炎。
- 黄疸、尿色深、乏力明显:警惕免疫相关肝炎。
- 持续高热、意识改变、严重头痛:需排查中枢神经系统不良反应或感染。
- 心悸胸痛、活动耐量骤降:警惕免疫相关心肌炎(虽少见但危险)。
2)居家管理的实操建议
- 皮疹/瘙痒:温和保湿、避免热水烫洗与搔抓;出现大片红斑、水疱、黏膜受累要尽快就医。
- 腹泻:记录每天次数与性状;先补液与电解质,避免辛辣油腻与乳制品;若≥4次/天或伴发热便血,尽快联系医生。
- 乏力与食欲下降:少量多餐,高蛋白饮食(鱼、蛋、豆制品、瘦肉);若伴体重快速下降或头晕心慌,需排查甲状腺功能与肾上腺功能等内分泌问题。
- 内分泌异常(甲状腺炎、垂体炎等)常起病隐匿:建议按医嘱定期监测TSH、FT4、皮质醇等;出现畏寒怕热、心率异常、体重突变、低血压等及时报告。
重要原则:免疫相关副作用越早处理,越可能用更小剂量、更短疗程的激素控制,并保住后续治疗机会。
九、一个可执行的决策框架:拿着这份清单去和医生沟通
原文提出可切除肿瘤使用免疫治疗已形成初步流程。我们把它改写成患者可执行的“问诊清单”。你可以把以下问题带到门诊:
1)我属于哪一类风险?复发风险高在哪里?
- 分期、淋巴结状态、脉管/神经侵犯、溃疡/深浸润等高危因素有哪些?
- 如果不做辅助治疗,大致复发风险处于什么区间(医生通常会给一个经验分层)?
2)我做了哪些必要检测,结果如何影响方案?
- 免疫相关:PD-L1、TMB、dMMR/MSI等(不同肿瘤差异很大)。
- 分子检测:EGFR、ALK、KRAS、STK11、KEAP1等(尤其肺癌)。
- 动态指标:是否适合做ctDNA监测?何时做、做几次、结果如何用来决定是否继续治疗?
3)时机怎么选:术前、新辅助,还是术后辅助?
- 肿瘤是否容易实现R0切除?肿瘤负荷是否大到需要先降期?
- 我是否有自身免疫病、间质性肺病等免疫治疗高风险背景?
- 若术前达到pCR/MPR,术后免疫是否需要、持续多久?
十、药物可及性与就医路径:把“先进方案”变成“可落地方案”
对于多数家庭,真正的困难不是“知道有新药”,而是“能不能用上、如何规范用、费用是否可承受”。免疫治疗与靶向治疗在不同国家和地区的获批、医保覆盖、供药稳定性都可能不同;同一药在不同适应症(如辅助或围手术期)也可能存在可及性差异。
MedFind建议的务实做法是:先在正规肿瘤专科完成分期、病理与分子检测,明确“你到底属于哪条治疗路径”;若医生确认适合某一前沿方案,但遇到药物可及性、购药渠道或用药衔接问题,可以把处方与检查结果整理齐全,进一步评估合规可行的获取方式与随访监测计划。
结尾:把不确定变成可管理的选择
辅助与围手术期免疫治疗的核心矛盾,是“人群复发风险并不相同”,而我们过去常用“一刀切的一年疗程”。越来越多证据提示:对某些肿瘤(如NSCLC、黑色素瘤、肾细胞癌),免疫治疗在早期阶段确实能降低复发风险;同时,pCR/MPR与ctDNA等工具正在帮助我们更接近个体化:该积极的人更积极,该降阶梯的人不被过度治疗。
如果你正在面对“术前要不要加免疫”“术后要不要做满一年”“复发风险到底有多高”的选择,MedFind可以提供两类实用支持:第一,基于你的分期、病理与检测结果,帮助你把方案差异、关键证据与风险点解释清楚(AI辅助问诊与方案解读);第二,当医生明确需要某些关键药物时,提供合规的抗癌药品跨境直邮支持,尽量减少因为可及性导致的治疗延误。下一步建议:把你的病理报告、分期、治疗经过和分子检测结果整理成一份清单,我们一起把方案“落到你身上”。
【参考文献】
Reconsidering adjuvant and perioperative immunecheckpoint inhibition: deescalation, expansion and personalization. Nat Rev Clin Oncol. 2026 Feb 18.

![转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析 2 转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析](https://medfind.link/wp-content/uploads/2026/05/b5eabf912ca30af172ff43ee330147e8.jpg)