病理报告要等一两天,手术切多切少却要马上决定怎么办?对乳腺癌患者和家属来说,“H&E染色多久出片”“术中能不能更快给结果”“活检组织会不会因为染色用掉而没法做基因检测”都是最真实的焦虑。本文把一种正在改变病理流程的技术讲清楚:基于多光谱自发荧光成像与深度学习的AI虚拟H&E染色,它如何把传统24-48小时的流程压缩到“几分钟级”,它的可靠性证据在哪里,以及它未来最可能先落地在哪些临床环节。
一、先弄明白:H&E染色为什么又慢又“耗样本”
乳腺癌的很多关键决策都离不开病理:是否恶性、肿瘤类型、分级、浸润范围、切缘情况等。传统病理最常用的是H&E染色(苏木精-伊红染色):用化学染料把细胞核染成偏蓝紫、细胞质和间质染成偏粉红,让病理医生在显微镜下识别结构。
慢主要来自流程本身:取材后需要固定、脱水、包埋、切片、染色、封片、扫描/阅片等多个步骤。即便在高效率病理科,从取材到形成高质量可诊断切片,常常需要24-48小时。
“耗样本”指的是:化学处理会对组织造成一定影响,且切片数量有限。对一些样本量很小的穿刺活检而言,患者更关心的是:“染色用了这么多组织,会不会影响后续做基因检测、多组学、空间转录组或单细胞测序?”这也是临床一直想解决的矛盾:既要快速诊断,又要尽量保留样本的完整性。
二、AI虚拟H&E染色是什么:不“上色”,却能“看起来像上色”
这项技术的核心思路是:不再依赖化学染料去“染”,而是先用光学手段采集组织自身的信号,再用AI把这些信号“翻译”为病理医生熟悉的H&E外观。
1)多光谱自发荧光成像:组织自己会“发光”
人体组织里有一些内源性物质会在特定光照下发出荧光(不需要外加染料)。研究采用的是多光谱自发荧光成像:用多个光谱通道采集同一张切片的不同荧光信息。你可以把它理解成“同一个场景,用多种滤镜分别拍照”,每张照片强调的细节不同:有的更突出细胞核相关信息,有的更突出细胞质、间质或代谢相关结构。
2)增强型循环生成对抗网络:把“荧光语言”翻译成“H&E语言”
随后,研究使用增强型循环生成对抗网络(属于生成对抗网络的一类)把无标记图像转换成“诊断级”的虚拟H&E图像。更关键的一点是:它可以在无需配对训练数据的情况下学习这种转换(不要求每一张无标记图像都严格对应同一位置的真实H&E图像)。
用一个更贴近生活的比喻:传统做法像“必须拿到同一段中文与英文对照文本才能翻译”;而这种方法更像“通过大量中文文章和大量英文文章,学习两种语言的风格和规律”,也能把中文翻成很像英文的表达。
三、最重要的问题:虚拟H&E“像不像”“能不能用”
对患者来说,真正关心的不是模型多先进,而是:医生看这张图能不能做出同样可靠的判断?这项研究从两个层面给了证据:形态学量化一致与病理医师双盲评分一致。
1)关键形态学指标:分布几乎完全重合
研究把虚拟H&E图像与同一组织的标准H&E进行了定量对比,提取了细胞与细胞核的多项关键形态参数(文中提到八项,举例包括:细胞面积、核面积、核周长、核质比、核圆度等)。结论是:这些指标在两种图像中的分布几乎完全重合。
以核质比为例(很多肿瘤病理判断会关注“核更大、更深、比例更高”等特征),研究报告:Jaccard重叠系数为0.92±0.02;Kolmogorov-Smirnov检验p=0.81;Cohen’s d效应量0.06。这些统计结果的直观含义是:两种图像在这个关键指标上差异非常小,小到在统计学上“分不出”。核面积、核周长等也呈现同样的一致性。
虚拟H&E与标准H&E在细胞与细胞核关键形态参数上进行定量比较
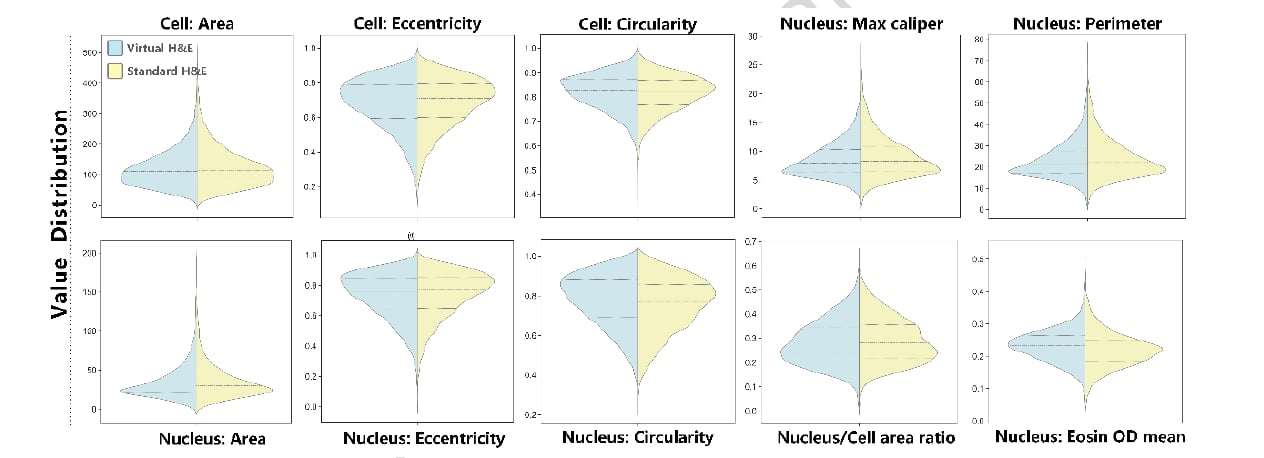
虚拟H&E与标准H&E在多项形态学参数上的分布高度重合
| 证据类型 | 研究怎么做 | 对患者意味着什么 |
|---|---|---|
| 形态学量化一致 | 提取细胞/细胞核面积、周长、核质比、圆度等指标,对比分布与统计检验 | AI生成的图像在“肿瘤看图的关键线索”上与真实H&E非常接近 |
| 医师主观可用性 | 资深病理医师双盲给分,并做统计与ROC分析 | 不仅像,而且“好用”:医生用它做判断时不容易被察觉是虚拟图 |
2)病理医师双盲评分:临床上难以区分
研究邀请5位资深病理医师,对18对虚拟H&E与标准H&E图像进行双盲评分。评分维度包括:细胞核染色细节、细胞质染色细节、细胞间质染色细节、整体染色质量,采用4分制(1分不可接受,4分优秀)。结果显示:两组在上述四个维度评分均无显著差异(Wilcoxon符号秩检验p值均大于0.05)。
更贴近患者直觉的两个数字是:在整体染色表现上,82.2%的虚拟H&E图像得分不低于标准H&E;在细胞核染色细节上,这一比例为83.3%。此外,ROC分析中区分虚拟与标准的AUC接近0.5(报告为0.463和0.584),这意味着:从“能否把两者分开”这个角度看,病理医师几乎做不到稳定区分,也就从侧面支持了其诊断等效性。
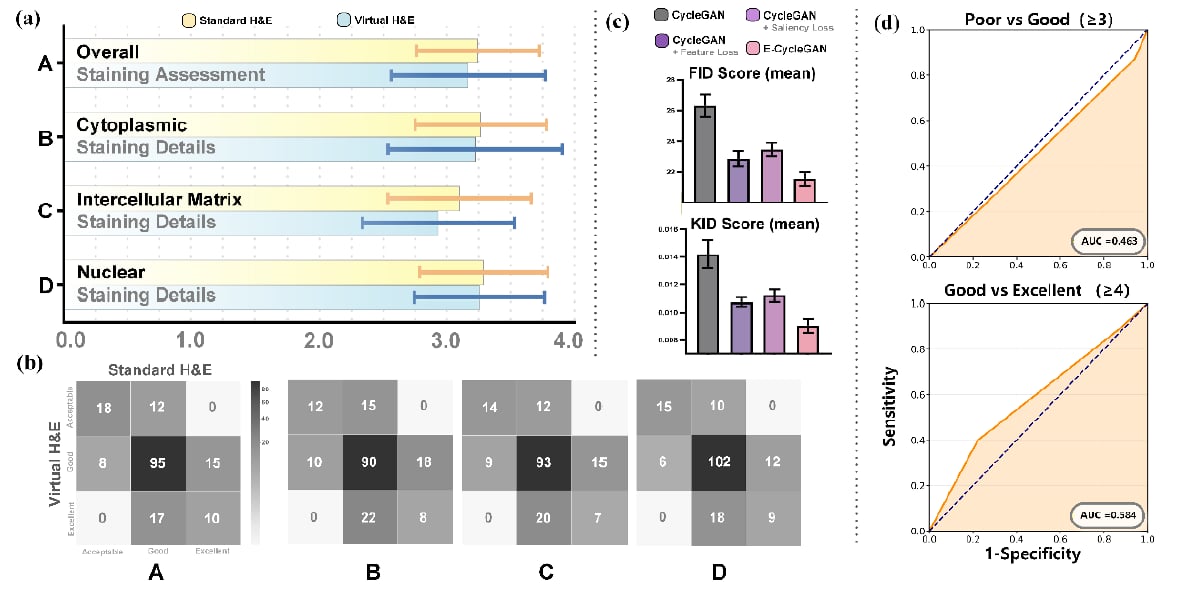
病理医师双盲评分与ROC分析显示虚拟H&E与标准H&E在临床评估上难以区分
四、为什么“多光谱”更关键:单通道容易失真
研究还回答了一个很实际的问题:如果只用单个荧光通道(例如只看某一种信号),能不能也生成虚拟H&E?答案是:可以生成,但质量容易不稳定。
文中对比显示:单通道输入生成的图像更容易出现色彩失真、结构边界模糊、细胞核与细胞质对比不足等问题。多光谱融合则能利用不同内源性荧光物质信息的互补性,使生成图像色彩更准确、结构更清晰,连细胞核染色质分布、细胞质细节也更容易重建。
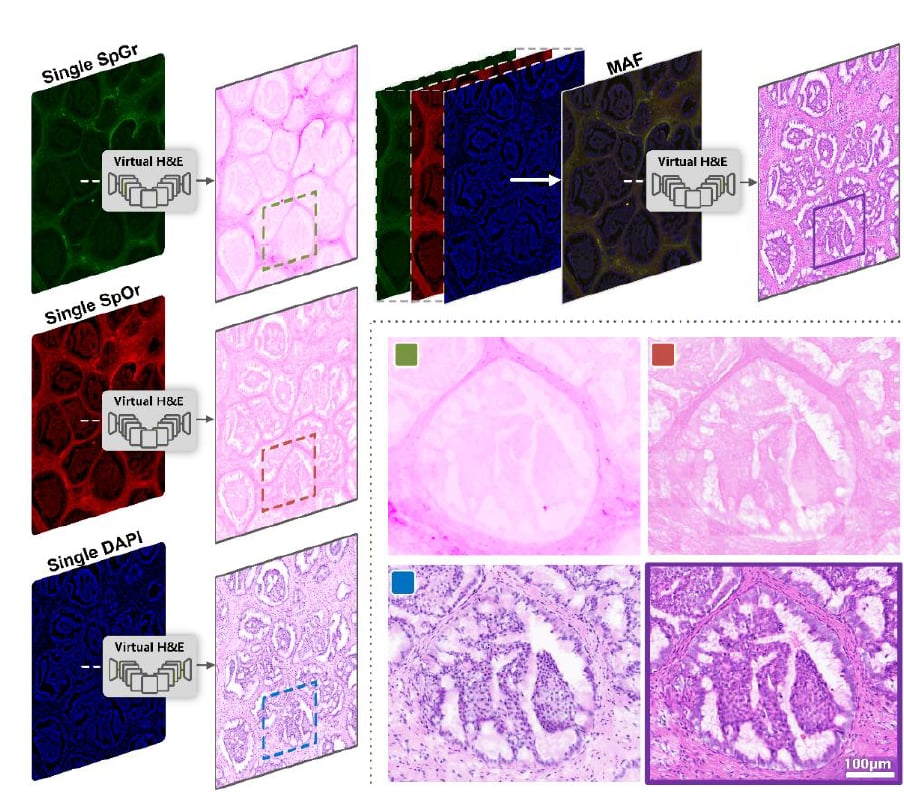
多光谱融合相比单通道可显著改善虚拟H&E的色彩还原与结构细节
五、跨模型验证意味着什么:不只“在一种样本上好看”
很多AI研究卡在一个问题:在某一类数据上表现很好,换个样本来源、换个模型就“掉链子”。这项研究进一步做了跨模型验证:
- 小鼠乳腺癌模型:虚拟H&E能够再现肿瘤异质性、坏死区域、免疫细胞浸润等病理特征。
- 乳腺癌-肺类器官共培养模型:虚拟染色可清晰显示癌细胞团与基质的相互作用;更重要的是,染色后的样本仍可用于后续单细胞测序或空间转录组分析,达到“同一份样本,多重研究维度”。
对患者而言,这类验证并不等于“明天就能在所有医院用上”,但它提示:这不是只在单一场景凑巧成功的技术,而更接近一种可迁移、可扩展的工具链。
六、它会先用在哪里:术中快速决策与“保留样本”两条主线
把“24小时变成几分钟”的意义,最可能体现在两类临床场景:
1)术中(或术前紧急)病理需求:减少等待与二次手术风险
当医生需要快速判断切缘、浸润范围或病变性质时,时间就是代价。若未来将便携式多光谱成像设备与边缘计算结合,理论上有机会在术中更快给到病理层面的参考信息,为手术范围提供更及时的依据。
需要强调:目前常见的术中快速病理(如冰冻切片)与常规石蜡H&E各有优势与局限。AI虚拟H&E更像是在探索一种新的“快而不损”的路径,最终是否能成为标准流程的一部分,仍取决于更多临床验证、质控体系与监管审批。
2)小样本活检:尽量把组织留给分子检测与精准治疗
乳腺癌的治疗越来越依赖分子层面信息(例如分型相关检测、基因层面的风险评估、复发风险预测等)。当组织很少时,如何在“尽快明确诊断”与“留足材料做进一步检测”之间平衡,是很多家庭会遇到的现实难题。无标记成像+虚拟染色如果能减少对组织的化学处理与消耗,就有机会让“一份样本发挥更多价值”。
七、患者最关心的5个问题(直说版)
1)这是不是“AI替代病理医生”?
不是。它更像是把传统的“化学染色步骤”用“光学成像+算法转换”替换掉,让病理医生更快拿到熟悉的阅片图像。诊断责任仍在病理医生与医疗机构。
2)虚拟H&E会不会“生成不存在的结构”?
这是所有生成类模型必须高度警惕的问题,因此研究用形态学量化一致与双盲评分来验证“关键结构没有偏移”。未来要真正临床落地,还需要更大规模、更多中心、更复杂病例(不同亚型、不同处理方式、不同扫描设备)的验证与质控。
3)什么时候能在医院用上?
文章展示的是研究级证据与潜力,不等同于已成为常规临床服务。能否进入临床流程,通常还需要:多中心临床验证、标准化操作规范、设备与软件的合规审批、与现有病理工作流的整合等。
4)它对“是否需要做基因检测”有帮助吗?
它本身不是基因检测,但其价值在于:如果能减少传统化学处理对样本的影响,并降低样本消耗,就更可能让后续的基因检测或多组学检测“有材料可做、质量更稳定”。具体是否适用仍取决于医院流程与检测平台要求。
5)患者现在能做什么准备?
- 做穿刺或手术前,和医生沟通:本次取材是否需要同时考虑后续检测(例如基因检测/多组学),是否需要病理科预留组织。
- 索取并保存好:病理报告、蜡块/切片编号、免疫组化结果、影像与手术记录等,方便后续多学科会诊或复核。
- 如果面对“方案选择困难”(是否需要更深入分子检测、结果如何解读),建议尽早进行规范的辅助问诊或第二意见咨询,避免在时间窗口内反复试错。
八、写在最后:更快的诊断,是为了更稳的治疗选择
对乳腺癌患者而言,技术进步的意义从来不是“酷”,而是:少等一天、少一次手术、少走弯路,以及把有限的样本用在刀刃上。这项研究提示我们,AI虚拟H&E染色有机会把传统病理流程中最耗时、最消耗样本的一环,转化为“更快、更温和”的路径,并在形态学一致性与临床双盲评分上给出了扎实证据。
如果你正在经历诊断等待、担心活检样本不够用,或在治疗决策(手术范围、后续治疗与检测路径)上感到信息不对称,MedFind可以提供两类务实支持:其一,帮助你梳理检测与治疗的关键问题清单,进行辅助问诊与治疗方案解读;其二,当你和医生确认需要特定前沿抗癌药物且面临可及性问题时,我们提供合规路径的信息支持与抗癌药品跨境直邮服务,让“找到药、用对药”的过程更少阻碍。
【参考文献】
Sun J, Ye J, Chen S, Yang Z, Xu G, Xue Y, Ou Z, Chen X, Wang J. Artificial intelligence assisted multi-model pathological diagnosis of breast cancer based on multispectral autofluorescence images. NPJ Breast Cancer. 2026 Mar 12. doi: 10.1038/s41523-026-00915-2.

![转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析 5 转移性去势抵抗性前列腺癌治疗新进展:镥[177Lu]特昔维匹肽联合帕博利珠单抗疗效与副作用全解析](https://medfind.link/wp-content/uploads/2026/05/b5eabf912ca30af172ff43ee330147e8.jpg)