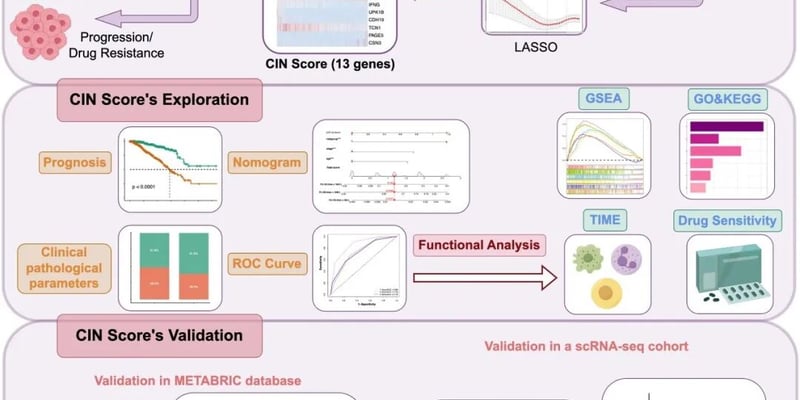
对于HER2阳性早期乳腺癌患者而言,新辅助治疗(手术前进行的治疗)是重要的治疗环节,其目标是缩小肿瘤、提高手术成功率,并评估药物疗效。病理完全缓解(pCR)是衡量新辅助治疗效果的关键指标,达到pCR通常预示着更好的长期预后。
DESTINY-Breast11研究:T-DXd联合方案的突破性结果
一项重要的III期临床研究——DESTINY-Breast11(NCT05113251)公布了令人振奋的顶线结果。该研究旨在评估靶向药fam-trastuzumab deruxtecan-nxki(T-DXd,商品名:Enhertu)序贯曲妥珠单抗(Herceptin)、帕妥珠单抗(Perjeta)和紫杉醇(THP)的新辅助治疗方案,在高风险、局部晚期HER2阳性早期乳腺癌患者中的疗效和安全性。
研究结果显示,与标准治疗方案(ddAC-THP,即剂量密集阿霉素和环磷酰胺序贯THP)相比,T-DXd序贯THP方案显著提高了患者的病理完全缓解(pCR)率。这一提升在统计学上具有显著性,并且在临床上具有重要意义。
尽管事件生存期(EFS)等关键次要终点的数据尚未完全成熟,但早期分析结果显示,基于T-DXd的治疗方案在EFS方面也呈现出优势趋势。
阿斯利康肿瘤研发执行副总裁Susan Galbraith表示,DESTINY-Breast11研究中观察到的具有临床意义的pCR率提升以及良好的安全性数据,凸显了T-DXd挑战当前HER2阳性早期乳腺癌标准治疗的潜力。Enhertu已是转移性乳腺癌治疗的重要选择,这些数据有望使其应用于早期阶段,从而提高治愈的可能性。
第一三共全球研发负责人Ken Takeshita补充道,许多早期乳腺癌患者在新辅助治疗后未能达到pCR,这增加了疾病复发的风险。DESTINY-Breast11的顶线结果表明,T-DXd序贯THP方案有望为HER2阳性乳腺癌患者提供一种有前景的新术前治疗方法,帮助更多患者走向潜在的治愈之路。
研究设计与患者入组标准
DESTINY-Breast11是一项开放标签研究,共入组927名符合条件的患者。入组标准包括经组织学确认的HER2阳性早期乳腺癌(T0-4 N1-3, M0;或 T3, N0, M0),ECOG体力状态评分为0或1,器官功能良好等。既往有浸润性乳腺癌史、IV期疾病、近期其他恶性肿瘤、间质性肺病史或当前患有间质性肺病、或既往接受过乳腺癌全身治疗的患者被排除。
患者被随机分为三组(1:1:1):T-DXd单药组(已根据独立数据监察委员会建议停止入组)、T-DXd序贯THP组,以及标准治疗ddAC-THP组。
主要研究终点是病理完全缓解(pCR)率,定义为手术后乳腺和淋巴结中无浸润性癌残留。次要终点包括事件生存期(EFS)、无浸润性疾病生存期、总生存期、安全性和耐受性。
T-DXd(Enhertu)的现有应用
目前,T-DXd(Enhertu)已在美国FDA获批用于治疗既往接受过抗HER2治疗的不可切除或转移性HER2阳性乳腺癌成人患者。此外,Enhertu也被批准用于治疗激素受体阳性、HER2低表达(IHC 1+或2+/ISH阴性)或HER2超低表达(IHC 0伴膜染色)的不可切除或转移性乳腺癌成人患者,这些患者在转移性疾病阶段接受过至少一种内分泌治疗后疾病进展。
这些新的研究数据进一步拓展了T-DXd在乳腺癌治疗领域的潜力,为更多患者带来了新的希望。对于需要获取这类靶向药或抗癌药的患者,了解海外购药途径或寻求专业的AI问诊服务,可以帮助更好地了解治疗方案和药物获取方式。
DESTINY-Breast11试验的完整数据将在未来的医学会议上公布,并提交给监管机构进行审评。
参考资料
- Enhertu (fam-trastuzumab deruxtecan-nxki) followed by THP before surgery showed statistically significant and clinically meaningful improvement in pathologic complete response in patients with high-risk HER2-positive early-stage breast cancer in DESTINY-Breast11 Phase III trial. Astra Zeneca. News Release. May 7, 2025. Accessed May 7, 2025. https://www.astrazeneca-us.com/media/press-releases/2025/ENHERTU-fam-trastuzumab-deruxtecan-nxki-followed-by-THP-before-surgery-showed-statistically-significant-and-clinically-meaningful-improvement-in-pathologic-complete-response-in-patients-with-high-risk-HER2-positive-early-stage-breast-cancer-in-DESTINY-Breast11-Phase-III-trial.html
- Trastuzumab deruxtecan (T-DXd) alone or in sequence with THP, versus standard treatment (ddAC-THP), in HER2-positive early breast cancer. ClinicalTrials.gov Updated May 6, 2025. Accessed May 7, 2025. https://clinicaltrials.gov/study/NCT05113251
- FDA grants regular approval to fam-trastuzumab deruxtecan-nxki for breast cancer. FDA. May 4, 2022. Accessed May 7, 2025. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-regular-approval-fam-trastuzumab-deruxtecan-nxki-breast-cancer
- Enhertu approved in the US as first HER2-directed therapy for patients with HER2-low or HER2-ultralow metastatic breast cancer following disease progression after one or more endocrine therapies. News Release. AstraZeneca. January 27, 2025. Accessed May 7, 2025. https://www.astrazeneca.com/media-centre/press-releases/2025/enhertu-approved-in-us-for-breast-cancer-post-et.html