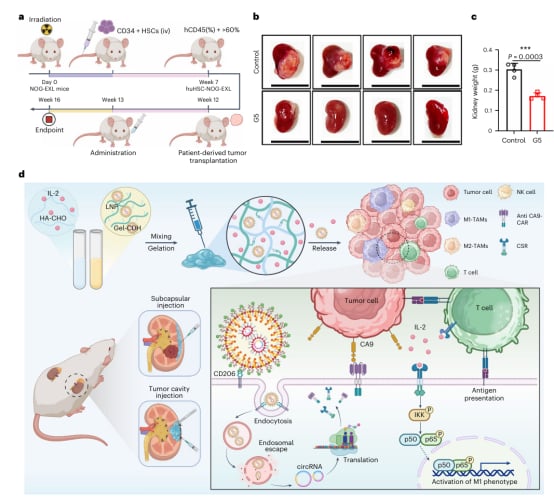
肾细胞癌(Renal Cell Carcinoma, RCC)作为一种常见的泌尿系统恶性肿瘤,尽管具有一定的免疫原性,但其治疗面临诸多挑战。肿瘤微环境(TME)中广泛存在的免疫抑制细胞和因子,使得传统治疗手段效果有限,且术后复发和转移风险较高。近年来,免疫治疗为肾细胞癌患者带来了新的希望,然而,现有免疫疗法在实体瘤中的疗效仍有待提升。
巨噬细胞是肿瘤微环境中的重要组成部分,它们可以根据环境信号在促肿瘤的M2型和抗肿瘤的M1型之间转换。嵌合抗原受体巨噬细胞(CAR-Ms)作为一种新兴的细胞疗法,在理论上具有改造肿瘤微环境、增强抗肿瘤免疫的潜力。但CAR-Ms在实体瘤复杂的免疫抑制环境中容易被“策反”,重新分化为M2型,这极大地限制了其治疗效果。因此,如何工程化改造CAR-Ms,使其在肿瘤微环境中保持抗肿瘤活性并维持M1表型,成为了当前研究的焦点。
近期,山东大学的研究团队在《Nature Cancer》上发表了一项突破性研究,他们开发了一种新型策略,通过构建嵌合IL-2信号受体(CSR)来增强CAR巨噬细胞在肾细胞癌中的抗肿瘤能力。这项创新性工作结合了CSR设计、circRNA技术以及水凝胶局部递送系统,为克服实体瘤免疫治疗的瓶颈提供了全新的思路。这项题为“An in situ engineered chimeric IL-2 receptor potentiates the tumoricidal activity of proinflammatory CAR macrophages in renal cell carcinoma”的研究,通过严谨的动物模型验证,为其未来向临床转化奠定了坚实基础。

突破性设计:构建增强型CAR巨噬细胞
为了解决CAR-Ms在肿瘤微环境中功能受限的问题,研究人员进行了巧妙的设计:
- 嵌合IL-2信号受体(CSR)的设计: 他们将IL-2受体的胞外信号域与TLR4受体的胞内信号域融合,构建了CSR。这一设计使得CAR-Ms在接收到外源IL-2信号时,能够激活TLR4下游的信号通路,从而强力诱导巨噬细胞向抗肿瘤的M1表型极化。
- circRNA介导的基因递送: 利用环状RNA(circRNA)的高稳定性和高效翻译特性,研究团队构建了同时编码CSR和靶向肾细胞癌抗原CA9的CAR的circRNA。
- 脂质纳米颗粒(LNP)递送系统: 开发了优化的LNP系统,用于高效地将circRNA导入巨噬细胞,确保CSR和CAR的有效表达。
- 水凝胶局部给药策略: 构建了一种可注射的水凝胶,用于包裹载有circRNA的LNPs和IL-2。这种水凝胶系统能够实现药物在肿瘤部位的缓释和局部高浓度维持,从而更有效地重塑肿瘤微环境。
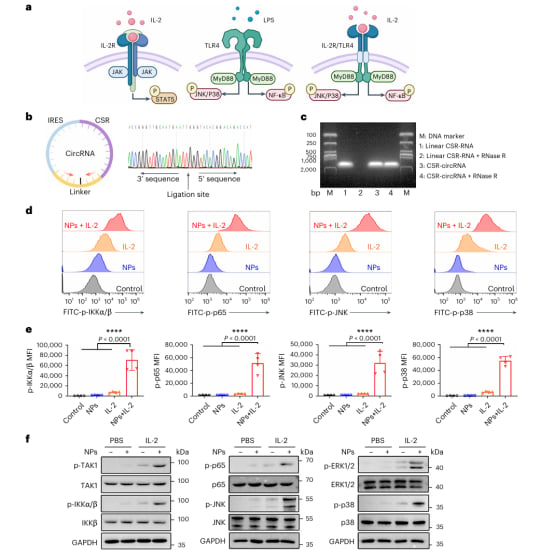
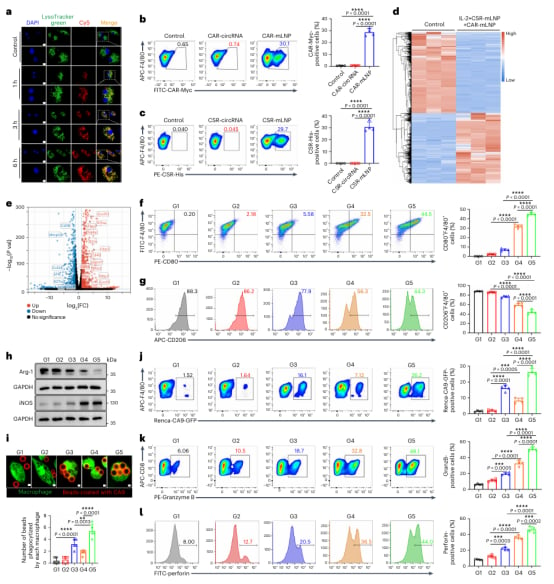
图1 CSR的设计与功能验证
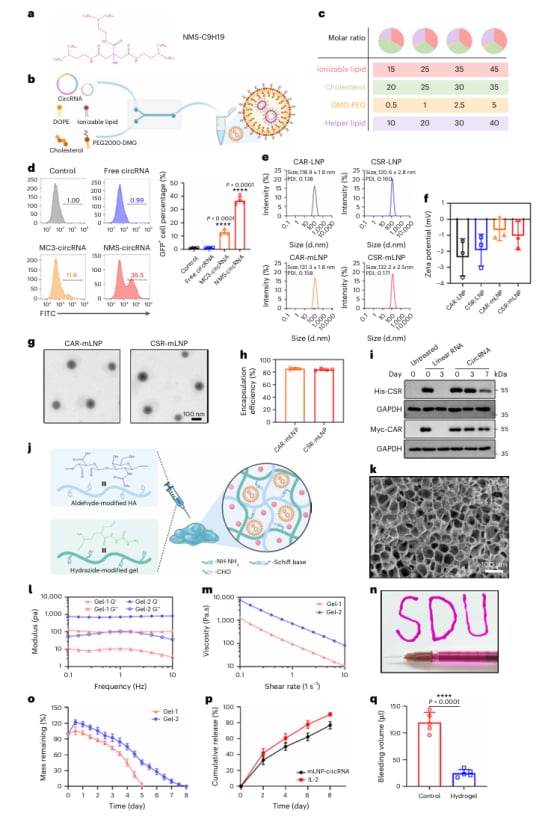
图2 LNP水凝胶递送系统的构建与表征
实验验证:强大的抗肿瘤活性与微环境重塑
研究团队通过一系列体外和体内实验,全面评估了这种新型CAR巨噬细胞疗法的效果:
- 体外功能增强: 实验结果显示,同时表达CSR和抗CA9 CAR的巨噬细胞,在IL-2刺激下,M1型标志物(如CD80)表达显著上调,M2型标志物(如CD206)表达下调,表明成功实现了M1极化。这些工程化巨噬细胞还表现出更强的抗原特异性吞噬能力,能有效识别并吞噬表达CA9的肿瘤细胞。

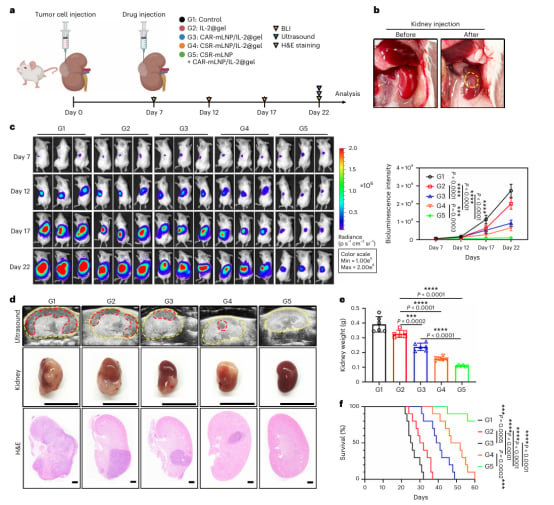
- 体内抑瘤效果显著: 在肾细胞癌小鼠模型中,通过水凝胶局部注射CSR-mLNPs、CAR-mLNPs和IL-2的联合治疗组,肿瘤生长受到显著抑制,肾脏重量减轻,小鼠生存期显著延长。生物发光成像和超声成像也证实了联合治疗组的肿瘤负荷最低。

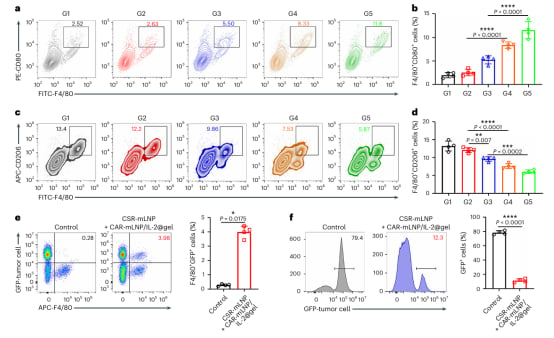
- 肿瘤微环境重塑: 治疗后的肿瘤组织分析显示,联合治疗显著增加了肿瘤内M1型巨噬细胞的比例,降低了M2型巨噬细胞比例,并增强了巨噬细胞对肿瘤细胞的吞噬。这表明该策略成功地将免疫抑制的肿瘤微环境转化为免疫激活状态。

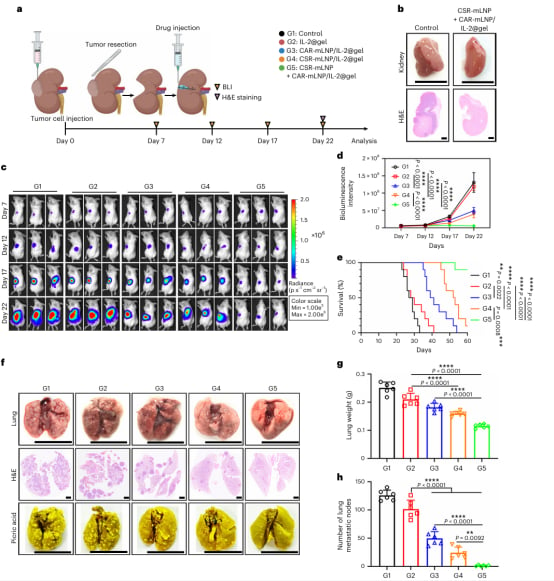
- 术后复发抑制: 在肾癌部分切除术后模型中,局部注射联合治疗的水凝胶能够显著抑制肿瘤复发和肺部转移,延长小鼠生存期。组织学分析显示手术部位肿瘤细胞被纤维组织替代,进一步验证了其在术后局部控制中的潜力。

- 人源化模型验证: 在人源化PDX肾癌模型中,该联合治疗同样显示出显著的抑瘤效果,且CAR巨噬细胞能有效靶向并富集在肿瘤部位,进一步支持了其临床相关性。

图3 CAR和CSR在巨噬细胞中的表达及功能
图4 体内抗肿瘤效果评估
图5 肿瘤微环境中巨噬细胞的极化和吞噬活性
图6 术后局部注射治疗的抗肿瘤效果
图7 人源化PDX模型中的治疗效果
总结与展望:为实体瘤免疫治疗开辟新路径
这项研究成功开发了一种新型的CAR巨噬细胞治疗策略,通过CSR设计、circRNA递送和水凝胶局部应用,有效增强了巨噬细胞的抗肿瘤功能,并克服了肿瘤微环境的免疫抑制。在肾细胞癌动物模型中取得的显著疗效,包括抑制肿瘤生长、减少转移和延长生存期,充分展示了该策略的巨大潜力。
虽然这项研究仍处于临床前阶段,但它为肾细胞癌乃至其他实体瘤的免疫治疗提供了令人振奋的新方向。随着更多前沿研究的不断涌现,癌症治疗手段日益丰富。对于正在积极寻求更优治疗方案的患者而言,及时了解最新的抗癌资讯至关重要。探索海外前沿药物,如特定的靶向药或仿制药,可以通过专业的海外代购平台获取信息。同时,AI问诊服务也能提供初步的参考和指导,帮助患者更好地理解病情和治疗选择。
未来,期待这项新型CAR巨噬细胞疗法能够顺利进入临床试验,最终惠及更多肾细胞癌及其他实体瘤患者。