复发难治大B细胞淋巴瘤怎么选治疗?是继续化疗、自体移植,还是尽快转向CAR-T、双特异性抗体或ADC?很多患者最关心的,其实是四件事:还有没有治愈机会、哪种方案更适合自己、复发后下一步怎么排、治疗能不能真正用得上。在复发难治性大B细胞淋巴瘤中,标准答案已经不再只有化疗和移植,治疗路径正在被CAR-T、双抗和新一代抗体偶联药物快速改写。
复发后为什么更难治?
大B细胞淋巴瘤并不是一种“复发了就原样回来”的疾病。很多患者在复发时,肿瘤已经发生了新的克隆演化、免疫逃逸和抗原变化,因此同样的药、同样的化疗强度,往往不再获得同样的效果。
临床上,约有30%到40%的大B细胞淋巴瘤患者最终会进入复发或难治阶段。尤其是原发难治或12个月内早期复发的人群,通常预后更差,也是当前新疗法重点覆盖的人群。
过去几十年,含铂挽救化疗后序贯自体造血干细胞移植一直是主要治愈路径。但这条路径有几个明显局限:一是要求患者体能和器官功能较好;二是肿瘤需要对挽救化疗敏感;三是对早期复发或原发难治患者,长期控制率有限。
正因如此,CAR-T细胞疗法、CD20×CD3双特异性抗体、抗体药物偶联物迅速成为复发难治性大B细胞淋巴瘤的核心新方向。

复发难治大B细胞淋巴瘤的治疗核心,正从传统化疗移植转向免疫治疗主导。
CAR-T、双抗、ADC到底是什么?
CAR-T为什么被视为“冲治愈”的方案?
CAR-T是把患者自身T细胞取出、改造后再回输,使其能够识别肿瘤表面的特定抗原,最常见的是CD19。它的价值不只是“缩瘤”,而是让一部分患者获得长期缓解平台期,这也是淋巴瘤领域最接近“治愈性免疫治疗”的证据之一。
目前在复发难治性大B细胞淋巴瘤中,二线CAR-T已经改变了治疗标准,尤其适用于早期复发、原发难治、体能状态允许、具备细胞治疗条件的患者。
双特异性抗体为什么越来越受关注?
双特异性抗体可以一端抓住肿瘤细胞,一端抓住T细胞,把患者自身免疫系统重新“拉到”肿瘤面前。对于LBCL,最常见的是CD20×CD3双抗。这类药的优势在于:
- 现货型,不需要等待细胞制备;
- 部分方案可以门诊开展;
- 对不适合移植或无法及时做CAR-T的患者尤其重要;
- 在CAR-T后复发人群中仍有活性。
当前最受关注的药物包括格菲妥单抗、艾可瑞妥单抗和奥尼妥单抗。
ADC为什么成为“连接化疗与免疫”的桥梁?
ADC是“抗体+细胞毒载荷”的组合,利用抗体把药物更精准地送到肿瘤细胞。它不像传统化疗那样完全“地毯式打击”,但也不是完全无毒。其优势在于兼具靶向识别和杀伤能力,可单用,也可与双抗或化疗联合。
在LBCL领域,最典型的是维泊妥珠单抗(优罗华, Polatuzumab vedotin),另外还有loncastuximab tesirine等新药平台。
二线治疗怎么选?关键先看这四点
复发难治性大B细胞淋巴瘤进入二线后,治疗选择不能只看药名,更要先回答下面四个问题:
- 是原发难治,还是复发?原发难治和12个月内早期复发,通常更偏向优先考虑CAR-T。
- 能否耐受移植或细胞治疗?适合移植不等于适合所有方案,不适合移植也不一定不能做CAR-T。
- 病情进展速度快不快?如果病情进展快,能否等待CAR-T制备就很关键,双抗或ADC可能承担桥接作用。
- 是否能真正获得治疗?很多时候决定方案的,不只是医学证据,还包括中心资源、路程、支付能力、照护条件和感染管理能力。
当前证据显示,二线谁更强?
现有证据提示:对于体能状态较好、早期复发或原发难治患者,二线CAR-T已经是重要标准;对于不适合移植或现实中难以及时接受CAR-T的患者,双抗或ADC联合方案正在快速上位。
| 治疗类型 | 更适合的人群 | 核心优势 | 主要限制 |
|---|---|---|---|
| CAR-T | 早期复发、原发难治、体能允许、可进入细胞治疗中心 | 长期缓解和治愈潜力强 | 制备周期、中心可及性、桥接治疗需求、感染与细胞因子释放综合征管理 |
| 双特异性抗体 | 不适合移植、无法及时做CAR-T、CAR-T后复发 | 现货型、部分可门诊、缓解率高 | CRS、感染、最佳序贯尚未定型 |
| ADC联合方案 | 需快速控病、希望保留后续CAR-T机会、部分不适合强化治疗患者 | 起效较快,可与化疗或双抗搭配 | 神经毒性、骨髓抑制、前线暴露后复用价值受限 |
| ASCT | 化疗敏感、晚期复发、筛选后适合移植者 | 在合适人群中仍有治愈价值 | 适用人群窄,现实使用率下降 |
格菲妥单抗联合GemOx值得关注吗?
在不适合移植的复发难治性大B细胞淋巴瘤患者中,格菲妥单抗联合吉西他滨/奥沙利铂是最值得关注的双抗方案之一。
STARGLO研究显示,这一方案相较于利妥昔单抗联合GemOx,带来了更好的总生存、无进展生存和完全缓解率。尤其值得注意的是,这不是单纯“提高了缓解率”,而是把生存终点也一并拉开了。
| 研究 | 方案 | 中位OS | 中位PFS | CR率 |
|---|---|---|---|---|
| STARGLO | 格菲妥单抗+GemOx | 未达到 | 13.8个月 | 58.5% |
| STARGLO | 利妥昔单抗+GemOx | 13.5个月 | 3.6个月 | 25.3% |
这组数据说明,双抗联合化疗骨架已经不是简单替代,而是可能在一部分患者中接近二线CAR-T所呈现的疾病控制形态。
但也必须看到它的现实争议:该研究在不同地区亚组中的结果并不完全一致,监管层面的解读也因此出现分歧。这提醒患者,看到“研究阳性”还不够,更要看适用人群、入组结构和自己所在地区的真实可及性。
维泊妥珠单抗联合GemOx效果如何?
POLARGO研究把维泊妥珠单抗(优罗华, Polatuzumab vedotin)联合R-GemOx与R-GemOx进行了比较,结果显示新方案在总生存、无进展生存和完全缓解率方面均更优。
| 研究 | 方案 | 中位OS | 中位PFS | CR率 |
|---|---|---|---|---|
| POLARGO | 维泊妥珠单抗+R-GemOx | 19.5个月 | 7.4个月 | 40% |
| POLARGO | R-GemOx | 12.5个月 | 2.7个月 | 19% |
这意味着,对于未接受过维泊妥珠单抗、又希望尽量避免苯达莫司汀相关深度免疫抑制的人群,这一方案具有较高临床价值,尤其在需要控制病情、同时保留后续CAR-T机会的场景下更值得考虑。
双抗加ADC会不会成为下一代标准?
从目前趋势看,答案很可能是“有机会”。双抗负责激活T细胞,ADC负责定点输送杀伤载荷,两者理论上能够覆盖不同的耐药机制,减少单一模式的局限。
SUNMO研究比较了莫妥珠单抗联合维泊妥珠单抗与R-GemOx,在不适合移植的R/R LBCL患者中显示出明显优势。
| 研究 | 方案 | ORR | CR率 | 中位PFS | 中位OS |
|---|---|---|---|---|---|
| SUNMO | Mosun-Pola | 70% | 51% | 11.5个月 | 18.7个月 |
| SUNMO | R-GemOx | 40% | 24% | 3.8个月 | 13.6个月 |
这类固定疗程、现货型、相对更适合门诊实施的方案,最大价值在于:把接近深度缓解的可能性,带到更多无法接受细胞治疗的患者面前。如果后续长期随访继续证实缓解持久,双抗+ADC很可能成为未来极其重要的序贯节点。
不过也要注意,这些结果未必能直接外推到一线已经用过维泊妥珠单抗的患者,尤其是短时间内复发的人群。
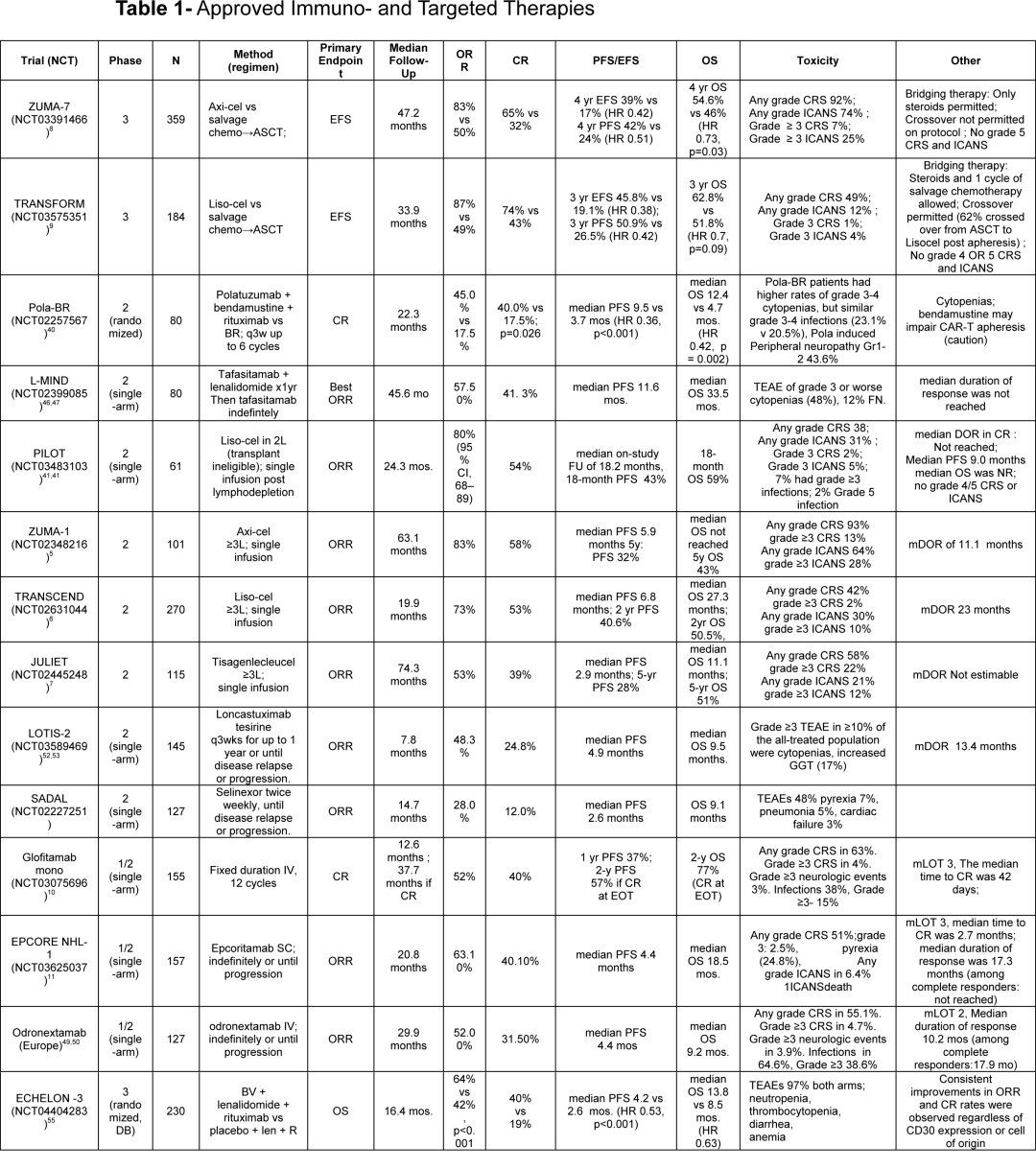
关键研究正在推动复发难治大B细胞淋巴瘤从化疗时代走向免疫治疗时代。
三线及以后还有哪些关键选择?
进入三线及以后,患者最怕的问题通常是:“前面方案都用过了,还有没有路?”目前答案仍然是有,但要更强调分层和序贯。
CAR-T仍是后线疗效标杆
在三线关键研究中,CAR-T仍然是很多新疗法拿来比较的“标杆”。原因很简单:它在相当一部分患者中可以带来持久缓解平台,约40%的患者有机会获得长期控制。
双特异性抗体是后线最实用的补充
格菲妥单抗、艾可瑞妥单抗和奥尼妥单抗等CD20双抗,在三线及以后大致呈现出相近的疗效轮廓:总体缓解率约60%,完全缓解率约40%,且对CAR-T后复发患者仍有活性。
这使双抗成为后线治疗中非常关键的“现货武器”,尤其适合以下情况:
- 等不起CAR-T制备时间;
- 既往做过CAR-T后再次复发;
- 基础疾病多,不适合高强度化疗;
- 需要尽量在门诊完成治疗。
ADC和其他靶向方案正在补位
除维泊妥珠单抗外,loncastuximab tesirine也在后线治疗中显示出价值。对部分患者而言,ADC更像是“可快速接入的控病平台”,而不是一次性解决所有问题的终点方案。
为什么真实世界疗效常比试验差?
这是患者非常容易忽视、却极其关键的问题。临床试验里的患者,往往经过了严格筛选:年龄、感染状态、血细胞水平、器官功能、既往治疗史、体能评分都要满足标准。真实世界则完全不同。
以坦昔妥单抗联合来那度胺为例,试验中的完全缓解率和无进展生存远优于真实世界结果,提示“研究能做出来”和“现实能用得好”之间,差着筛选标准、支持治疗能力和患者基础状态。
因此,患者解读治疗信息时一定要看三层:
- 这项研究的入组患者像不像自己;
- 自己所在医院是否具备相同的管理能力;
- 药物是否真正可及,是否能完成整个疗程。
复发后为什么还要关心分子生物学?
因为复发难治性大B细胞淋巴瘤不是一个单一疾病。不同亚型、不同复发时间、不同前期暴露,会直接影响后续方案反应。
目前已知,复发肿瘤可出现以下不利特征:
- TP53功能障碍;
- MYC/BCL2共扩增;
- CD58、B2M缺失,影响抗原呈递和免疫识别;
- CD19或CD20下调,导致CAR-T或双抗效果下降;
- IFN/JAK-STAT通路异常,削弱T细胞作用。
这也是为什么有些患者前面做了CAR-T,后面再用CD19相关策略时效果就未必理想;或者前面暴露过CD20导向治疗后,后续双抗疗效可能受到影响。未来治疗越来越依赖动态分型,而不是只看最初病理报告。
哪些新方案值得提前了解?
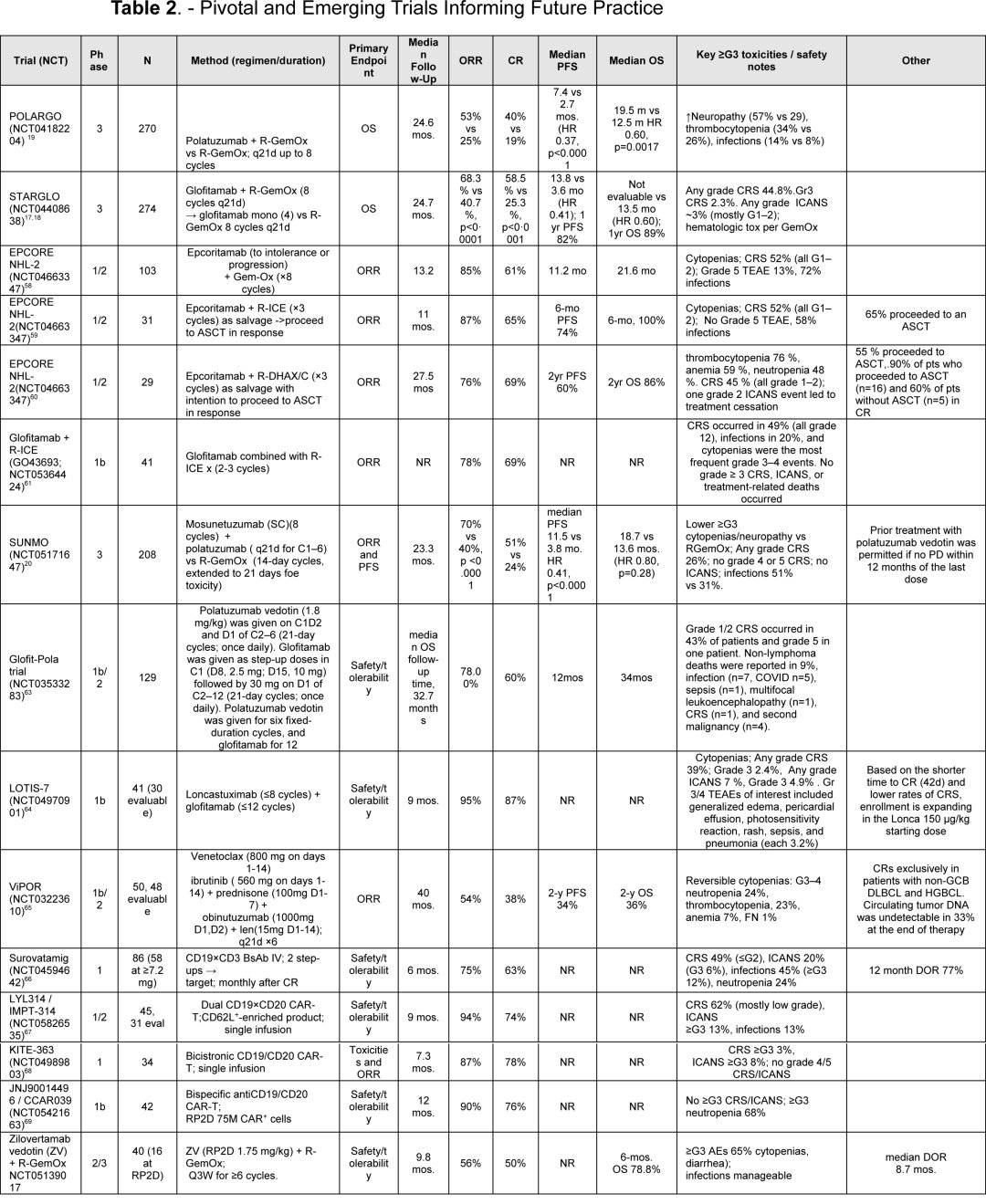
下一代治疗正在瞄准抗原逃逸、CAR-T后复发和无化疗治愈路径。
ViPOR:多通路固定疗程组合
ViPOR方案由维奈克拉(唯可来, Venetoclax)、伊布替尼(亿珂, Ibrutinib)、泼尼松(Prednisone)、奥妥珠单抗(佳罗华, Obinutuzumab)和来那度胺(瑞复美, Lenalidomide)组成。其设计思路不是“加大化疗强度”,而是从BCL2、BTK、免疫调节和抗CD20多个方向同时打击。
在早期研究中,这一固定疗程方案在non-GCB和双打击淋巴瘤中更活跃,而在GCB亚型中活性有限。对患者来说,它提示了一个重要方向:未来并不是所有复发患者都继续走同一路线,而是要按分子亚型定制组合。
下一代CD19×CD3双抗
Surovatamig这类下一代双抗试图在保留疗效的同时,降低细胞因子释放综合征风险。早期数据显示其完全缓解率和缓解持久性值得关注,提示CD19导向双抗未来可能在CAR-T后复发场景中承担更大角色。
双靶点CAR-T
针对CD19和CD20或CD22的双靶点CAR-T,是应对抗原逃逸最直接的思路之一。早期研究显示较高的缓解率和可观的持续时间,如果随机研究进一步证实优势,未来可能直接挑战现有单靶点CAR-T标准。
ROR1靶向ADC
Zilovertamab vedotin瞄准的是ROR1,这是一类在正常成人组织中极少表达、但在部分LBCL中与差预后相关的靶点。它的意义在于:当CD19、CD20路径越来越拥挤,新的非重叠靶点就变得更重要。
BCL6降解剂
BCL6是B细胞淋巴瘤的重要驱动因子之一。BCL6降解剂的早期临床结果显示,即便在既往接受过双抗或CAR-T的患者中也可见反应,且血液学毒性和免疫毒性相对可控。对后线患者而言,这类药物代表的是不同机制的新出口。
副作用怎么管?居家最该盯住哪些风险?
复发难治性大B细胞淋巴瘤的新治疗虽然更精准,但绝不意味着“轻松”。很多危险副作用并不是疼痛,而是感染、炎症风暴、神经症状和持续骨髓抑制。患者和家属居家管理时,最该盯住以下几类问题:
CAR-T和双抗最要防什么?
- 发热:治疗后出现发热,首先要同时警惕CRS和感染,不能自行当作普通感冒处理。
- 意识变化:包括反应迟钝、说话不清、定向力差、手抖、嗜睡,需立即联系医生,警惕神经毒性。
- 持续乏力和气促:可能与贫血、感染、肺炎或炎症反应相关。
- 反复感染:双抗和CAR-T后都可能出现长期免疫抑制,尤其要注意肺部感染、带状疱疹、真菌感染风险。
ADC和化疗联合常见哪些问题?
- 血细胞减少:白细胞、血小板、血红蛋白下降都常见,需按时复查血常规。
- 周围神经病变:手麻、脚麻、穿袜样感觉异常,应尽早反馈,必要时调整剂量。
- 恶心、食欲差、便秘或腹泻:多能通过止吐、补液和饮食调整改善,但持续加重要尽快就诊。
居家管理四个原则
- 每天测体温,一旦发热及时联系医生,不要自行拖延。
- 每周记录症状变化,包括食欲、精神、睡眠、大小便、麻木、头痛和咳嗽。
- 避免人群聚集和生冷饮食,骨髓抑制阶段尤其重要。
- 保留完整用药和检验记录,便于后续跨院会诊、辅助问诊和疗程衔接。
患者最关心的“能不能治愈”,现在该怎么理解?
在复发难治性大B细胞淋巴瘤中,“治愈”不是空话,但也不能一概而论。
现阶段最接近治愈证据的,仍然是:
- 二线CAR-T,尤其是早期复发和原发难治患者;
- 筛选后的ASCT,尤其是对化疗敏感、较晚复发患者;
- 部分双抗或双抗联合方案,如果后续随访继续出现稳定平台期,未来可能进入治愈性讨论。
但对很多患者来说,现实问题并不是“有没有最强方案”,而是“能不能在合适时机用上合适方案”。如果错过CAR-T窗口,或者因为药物、中心、支付、物流等问题延误,预后可能明显变差。
治疗顺序怎么排,才不容易走弯路?
当前较符合证据逻辑的思路是:
- 首次复发且适合CAR-T:优先评估CAR-T可行性,尤其是12个月内复发或原发难治患者。
- 不适合移植或难以及时做CAR-T:优先考虑双抗或ADC为基础方案。
- CAR-T后复发:重点评估CD20双抗、ADC联合、新机制药物或临床试验。
- 一线已暴露某些靶向药:二线三线要重新评估靶点是否仍然可用,避免机械重复。
真正难的地方在于,很多患者并不是标准教科书病例,而是同时存在感染风险、血细胞低、器官功能波动、病情进展快、就医半径大等现实困难。此时最需要的不是“多知道几个药名”,而是有能力把病理、分期、既往方案、复发时点、可及药物、中心资源整合成清晰的下一步路线。
药物可及性为什么正在决定疗效上限?
复发难治性大B细胞淋巴瘤已经进入“证据更新很快、可及性差异很大”的阶段。很多前沿药物和组合方案,在不同国家和地区的获批、支付、供应和用药路径并不一致。患者经常会遇到三种痛点:
- 知道有药,但本地医院暂时没有路径;
- 知道有方案,但不同地区获批节奏不同;
- 知道该换方案,却难以判断自己是否真适合。
这也是为什么复发后尽早进行系统梳理非常重要。越到后线,时间越宝贵,试错成本越高。
走到复发难治阶段,下一步最需要什么?
最需要的不是盲目追新,而是把信息差变成决策优势。对于复发难治性大B细胞淋巴瘤患者,真正关键的是三件事:尽快确认自己是否适合CAR-T、明确双抗和ADC的可用顺序、提前了解国内外前沿药物和可及路径。
如果已经面临复发、疗效不理想、需要比较不同国家和地区的药物选择,或者想进一步弄清楚某个双抗、ADC、CAR-T方案是否适合自己,MedFind可提供更有针对性的支持:包括前沿药物信息检索、治疗方案辅助解读,以及部分抗癌药物的跨境直邮路径参考,帮助患者尽量少走弯路,更快连接到真正可执行的下一步。
对复发难治性大B细胞淋巴瘤来说,希望从来不只来自新药本身,更来自在正确时间,用上正确方案。
【参考文献】
Blood. 2026 Mar 23:blood.2025030859. doi: 10.1182/blood.2025030859