食管鳞状细胞癌为什么一发现就常常偏晚、还容易侵袭转移?这类患者最关心的不只是“病理报告怎么看”,更是“为什么肿瘤这么凶”“后续还能怎么治”。围绕食管鳞状细胞癌的分子机制,越来越多研究正在寻找决定复发、转移和预后的关键开关,其中KHSRP与JAK1/STAT3信号轴的关系,提供了一个值得重视的新方向。
什么是KHSRP,为什么值得关注?
KHSRP是一类RNA结合蛋白,主要参与RNA剪接、稳定性调控、降解以及部分miRNA生成。对患者来说,可以把它理解为细胞内“信息加工环节”的调控者:它不直接等同于驱动基因突变,但能影响一批与肿瘤增殖、迁移、侵袭有关的分子表达。
这类分子之所以重要,是因为肿瘤恶化并不只靠单一突变完成。很多肿瘤细胞之所以更会长、更会跑、更容易转移,是由于多个信号网络同时被打开。KHSRP如果处于高表达状态,理论上就可能通过改变下游RNA与蛋白的表达,帮助肿瘤细胞获得更强的生存与扩散能力。
JAK1/STAT3通路为何和转移密切相关?
JAK/STAT通路是肿瘤研究中的经典信号网络之一。细胞因子、生长因子或炎症信号与细胞膜受体结合后,可激活JAK家族蛋白,继而促进STAT蛋白磷酸化并进入细胞核,驱动一系列促增殖、抗凋亡、促血管生成、促转移相关基因表达。
其中,JAK1和STAT3在多种实体瘤中都与肿瘤进展、免疫逃逸、治疗抵抗相关。对食管鳞状细胞癌而言,如果这一通路持续活跃,往往意味着肿瘤细胞更容易突破局部组织屏障、形成淋巴结或远处转移。
KHSRP在食管鳞状细胞癌中高表达吗?
研究纳入72例食管鳞状细胞癌患者组织样本,并结合多种食管鳞状细胞癌细胞系进行验证。结果显示,KHSRP在肿瘤组织和肿瘤细胞中均呈上调状态,提示它并非偶然变化,而可能与疾病生物学行为有关。
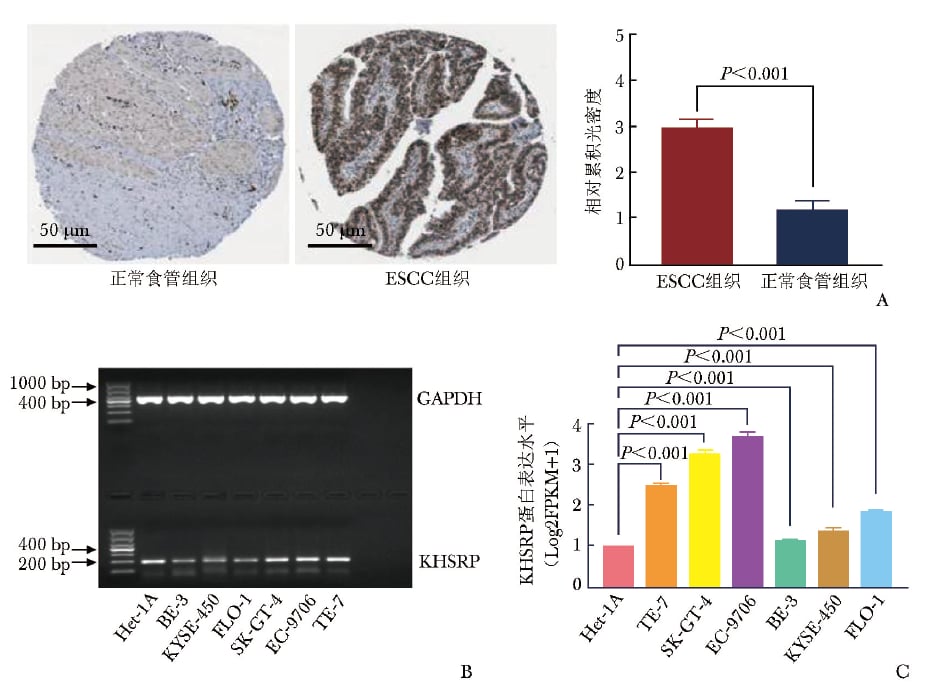
KHSRP在食管鳞状细胞癌组织及细胞系中上调。
更重要的是,KHSRP高表达并不只是实验室现象。临床病理分析显示,它与患者的TNM分期和淋巴结转移存在相关性。这意味着,KHSRP表达越高,肿瘤越可能表现出更强的局部进展和转移倾向。
| 观察维度 | 结果方向 | 临床意义 |
|---|---|---|
| 肿瘤组织 vs 癌旁组织 | KHSRP更高 | 提示与肿瘤发生发展相关 |
| 肿瘤细胞系 vs 正常食管上皮细胞 | KHSRP更高 | 支持其为肿瘤相关分子 |
| TNM分期 | 高表达相关 | 提示疾病更进展 |
| 淋巴结转移 | 高表达相关 | 提示更强转移潜能 |
| 性别、年龄、吸烟、饮酒 | 未见明确相关 | 更可能反映肿瘤内在生物学差异 |
KHSRP会直接影响肿瘤生长和转移吗?
答案是“有较强证据支持”。在细胞实验中,研究者分别进行了KHSRP敲低和过表达处理。
- 当KHSRP被敲低时,食管鳞状细胞癌细胞的增殖能力下降。
- 当KHSRP被过表达时,肿瘤细胞增殖增强。
- 在迁移和侵袭实验中,敲低KHSRP可显著减少穿膜细胞数,过表达则使迁移、侵袭能力明显增强。
这说明KHSRP不是单纯的“伴随改变”,而更像是推动肿瘤恶性行为的功能性分子。
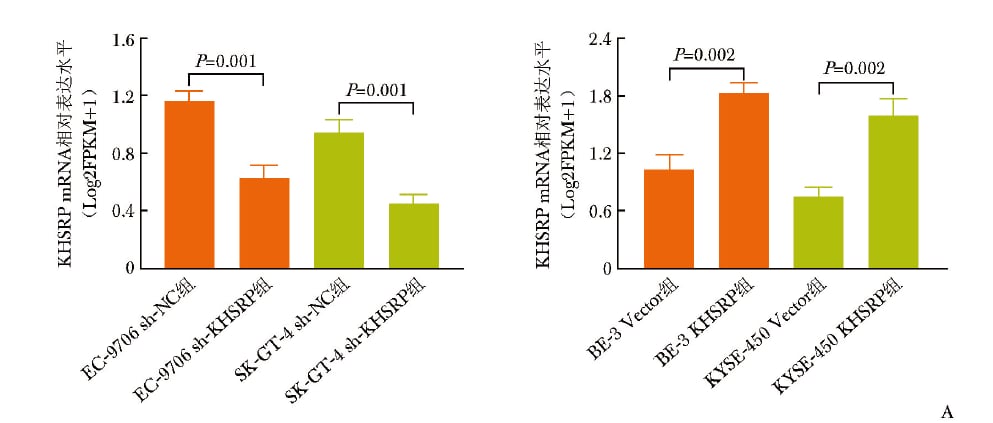
细胞层面完成KHSRP敲低与过表达后,转染效率得到验证。
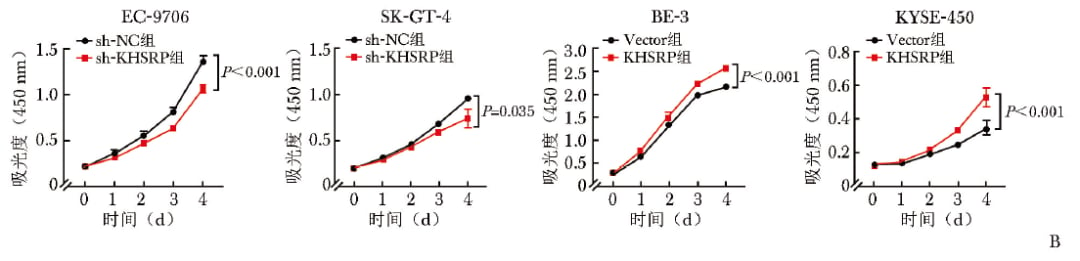
KHSRP升高可促进细胞增殖,敲低则抑制增殖。
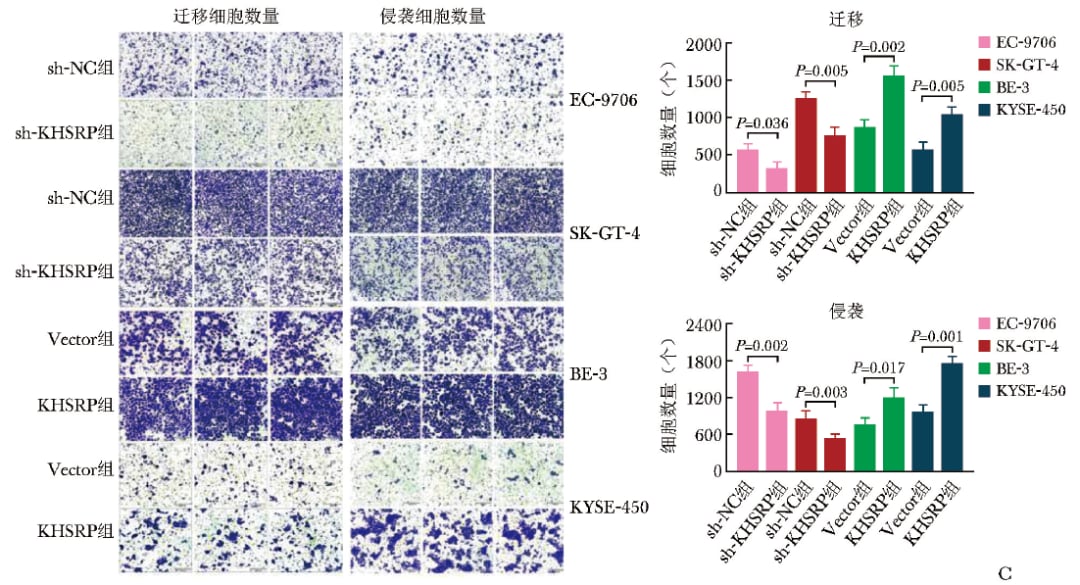
迁移和侵袭实验提示KHSRP与转移潜能增强相关。
动物实验说明了什么?
体外实验能说明趋势,但患者更关心“在活体里是否也成立”。动物实验给出了进一步支持。
在皮下荷瘤模型中,KHSRP敲低后,肿瘤体积和重量下降;KHSRP过表达后,肿瘤体积和重量增加。换句话说,KHSRP越活跃,肿瘤长得越快。
在尾静脉肺转移模型中,KHSRP敲低可减少肺部转移结节,而KHSRP过表达会增加转移灶数量。这一结果和细胞实验方向一致,强化了“它能促进转移”这一结论。
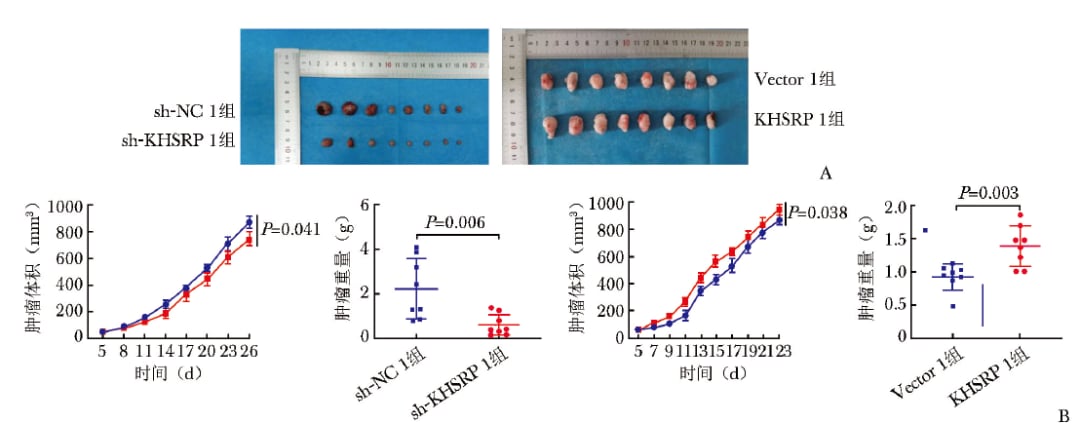
裸鼠皮下成瘤实验显示KHSRP可促进肿瘤生长。
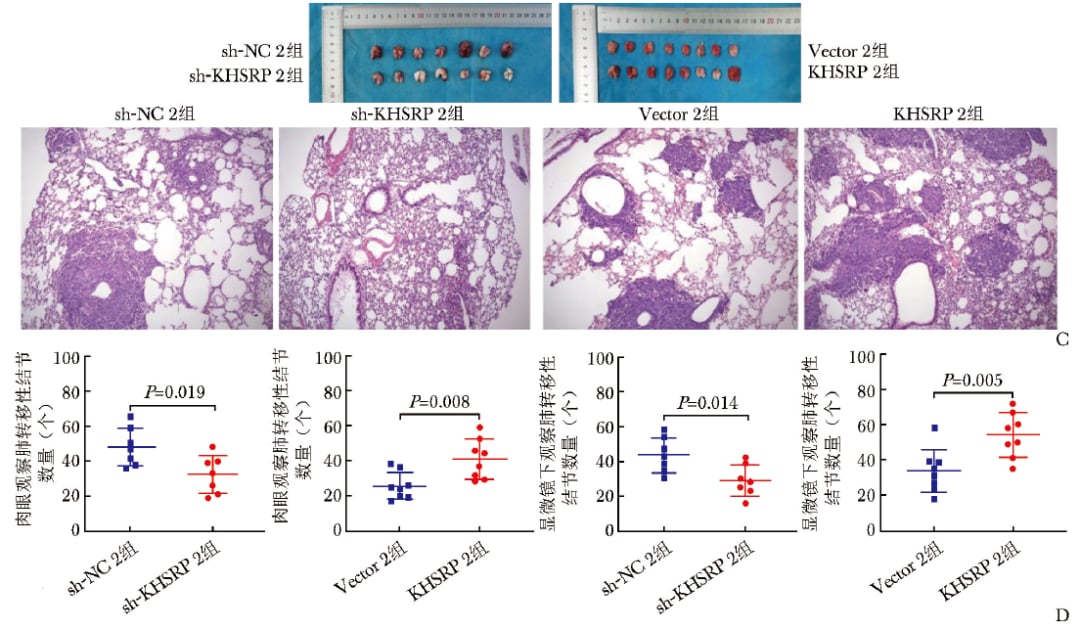
肺转移模型显示KHSRP与远处转移能力增强有关。
KHSRP是如何推动肿瘤恶化的?
核心线索指向JAK1/STAT3信号轴。研究发现,无论在mRNA水平还是蛋白水平,KHSRP上调都与JAK1、磷酸化JAK1、STAT3升高相关;而KHSRP被敲低后,这些指标同步下降。
同时,JAK2、STAT1、STAT2、STAT5等分子并未出现同样明确的变化趋势,提示KHSRP并不是“全面启动整个JAK/STAT家族”,而更偏向于影响JAK1/STAT3这条轴线。这种相对聚焦的调控关系,对未来筛选治疗靶点更有价值。
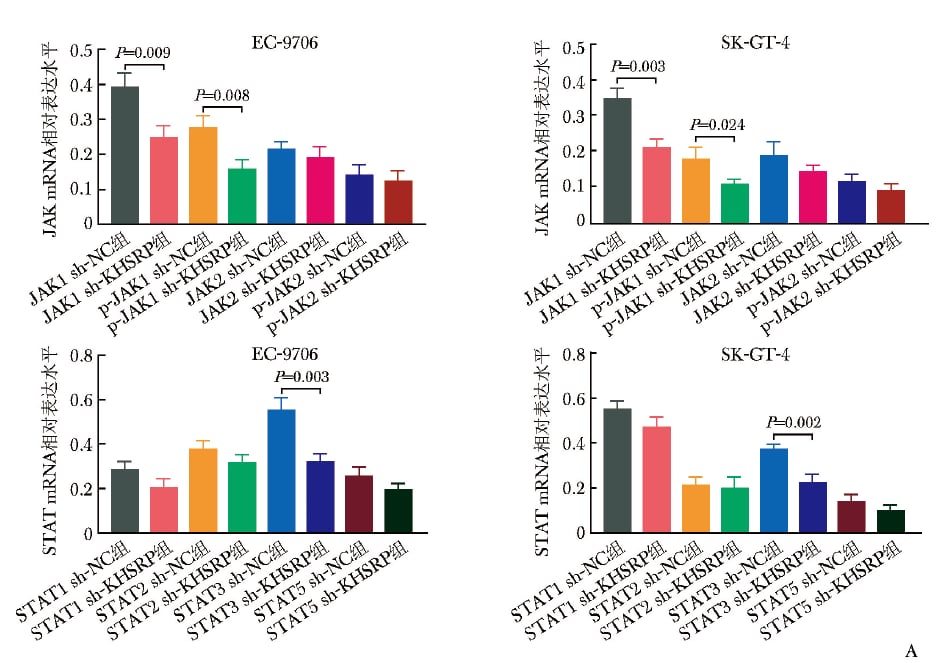
敲低KHSRP后,JAK1与STAT3相关转录水平下降。
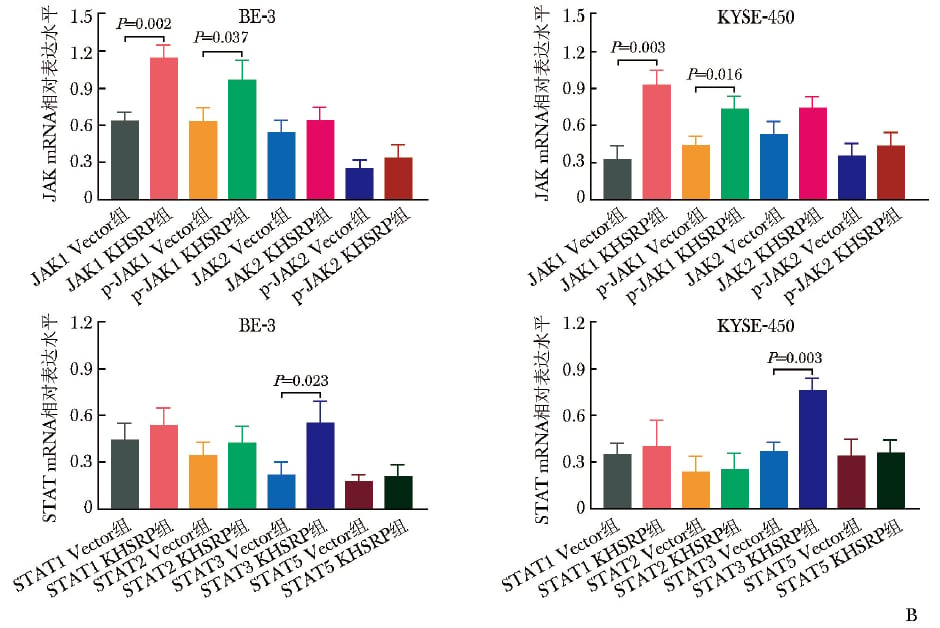
过表达KHSRP后,JAK1与STAT3相关转录水平升高。
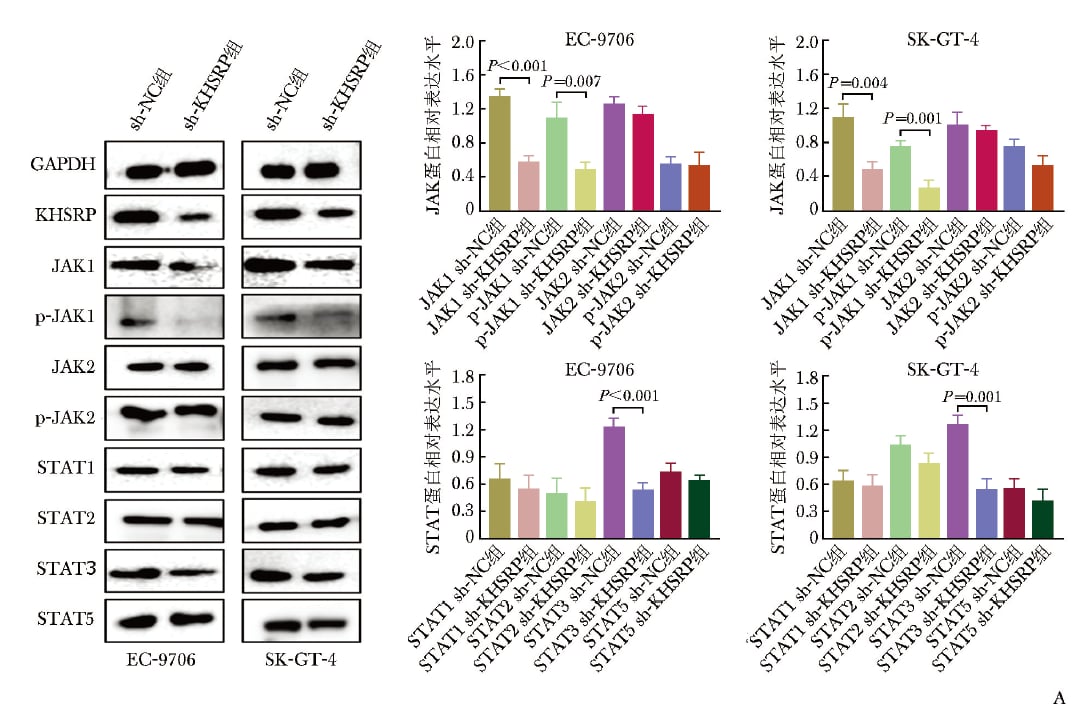
蛋白层面同样显示KHSRP对JAK1/STAT3具有正向调控作用。
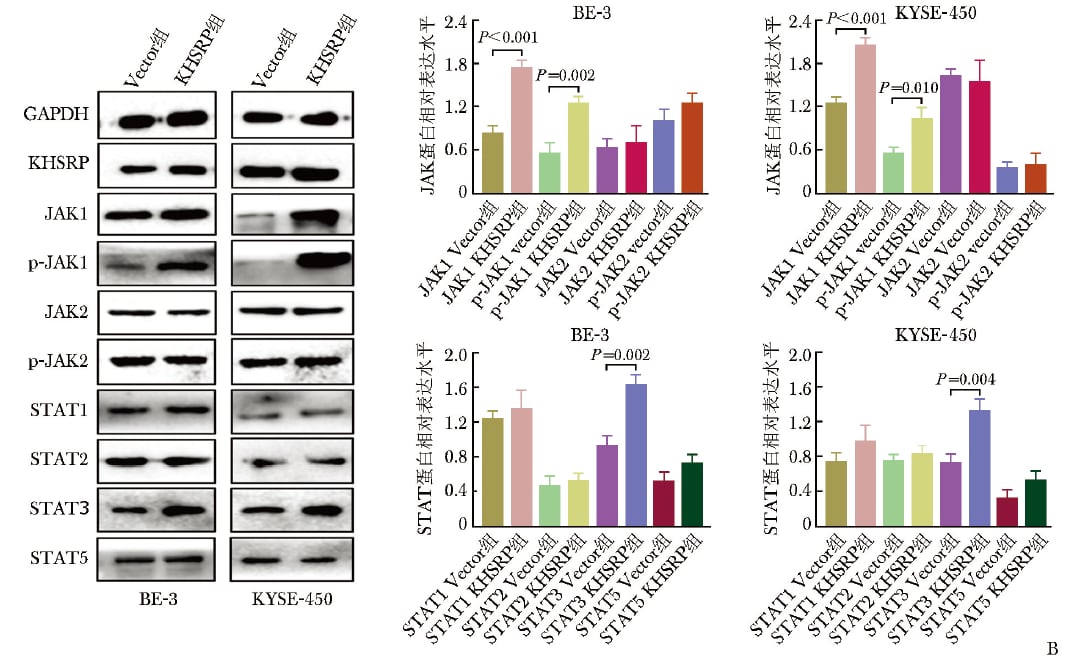
KHSRP升高伴随JAK1、p-JAK1、STAT3蛋白表达上调。
“挽救实验”为什么很关键?
很多基础研究只能证明“相关”,但未必证明“因果链条”。这项研究加入了挽救实验,使结论更扎实。
研究者在敲低JAK1/STAT3后,再过表达KHSRP,观察到肿瘤细胞的增殖、迁移和侵袭能力可被部分恢复。这个结果说明,KHSRP促进食管鳞状细胞癌恶化,并非孤立现象,而是至少部分依赖JAK1/STAT3通路实现。
对患者而言,这意味着未来如果要围绕这条机制开发治疗策略,理论上可以有两类思路:一类是直接瞄准KHSRP本身,另一类是阻断其关键下游通路JAK1/STAT3。
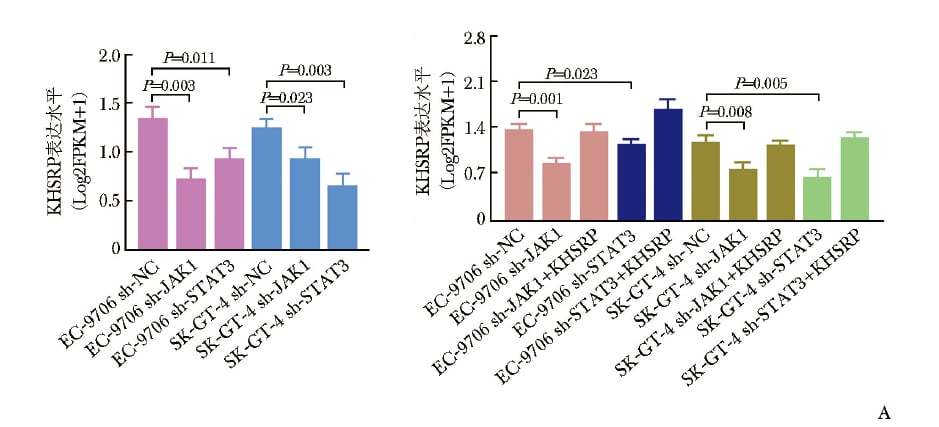
双向验证实验先确认相关基因处理有效。
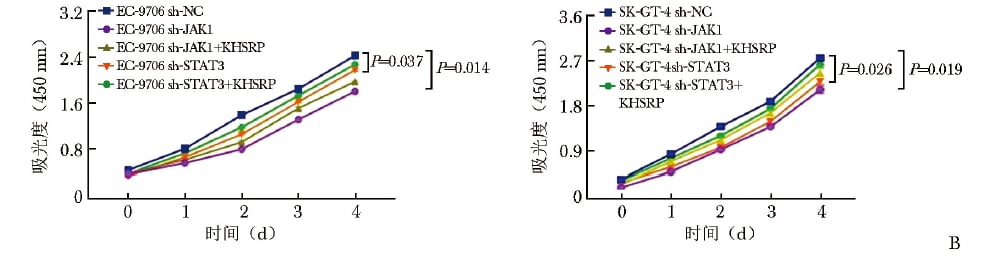
敲低JAK1/STAT3后,KHSRP仍可部分恢复增殖能力。
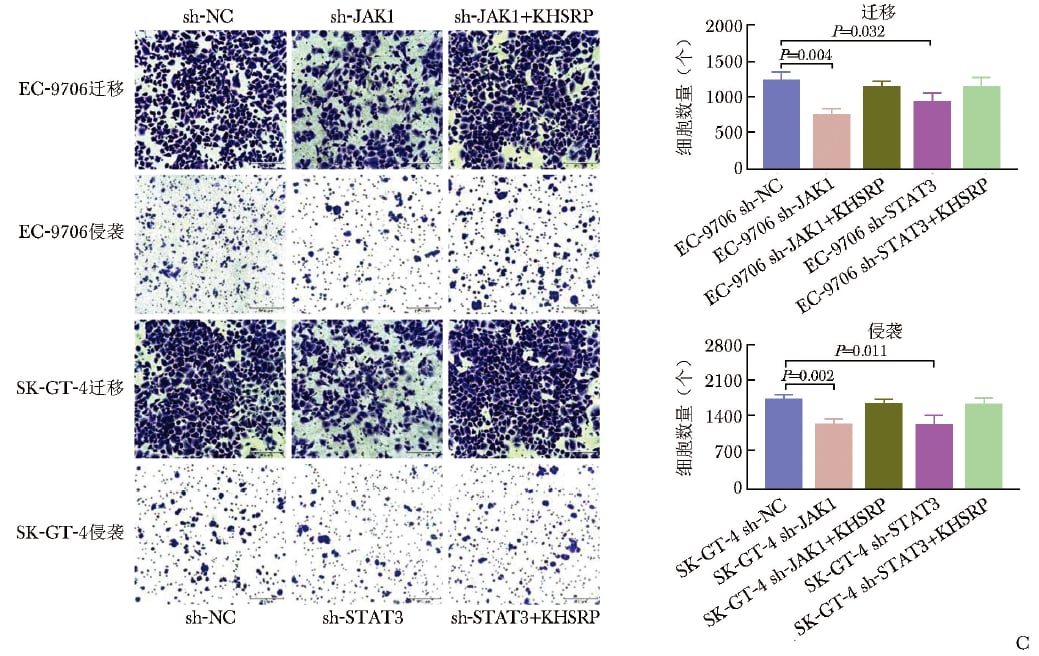
迁移与侵袭能力的部分恢复,支持KHSRP-JAK1/STAT3机制链条成立。
这项研究对患者治疗有什么现实意义?
首先要明确,这是一项机制研究,不是直接改变临床标准治疗的随机对照试验。它不能直接推出“检测KHSRP就一定决定怎么用药”,也不能说明已经有针对KHSRP的成熟上市药物可立即使用。
但它有三层现实意义。
第一层:帮助理解为什么有些肿瘤更凶
同样是食管鳞状细胞癌,不同患者的进展速度、复发风险和转移倾向差异很大。分子层面的差别,是重要原因之一。KHSRP高表达与TNM分期、淋巴结转移相关,为未来风险分层提供了线索。
第二层:为新靶点研发提供方向
食管鳞状细胞癌目前仍以手术、放疗、化疗、免疫治疗及部分围手术期综合治疗为核心。对于复发、转移或耐药患者,真正缺的往往不是“知道要治疗”,而是“下一步还有哪些更精准的选择”。KHSRP-JAK1/STAT3轴提示,未来可能出现更细分的分子干预路径。
第三层:为临床试验筛选提供思路
如果某类患者存在更显著的JAK1/STAT3通路激活,未来更可能成为相关靶向策略、联合免疫策略或转化研究的重点人群。对晚期患者而言,能否进入合适临床试验,常常直接影响治疗机会。
这是否意味着JAK/STAT抑制就是现成答案?
还不能这么理解。JAK/STAT通路很重要,但“机制成立”不等于“临床一定获益”。患者在搜索“JAK1/STAT3抑制剂能治食管癌吗”时,最容易掉进一个误区:把基础研究结果直接等同于现成治疗方案。
更稳妥的理解是:
- KHSRP-JAK1/STAT3是值得追踪的致病机制。
- 它提示某些患者未来可能从相关通路干预中受益。
- 真正能不能用于临床,还要看后续药物研发、人体研究和适应证验证。
因此,患者不应自行把研究结论转化成实际用药决定,而应结合病理类型、分期、既往治疗、PD-L1状态、基因检测结果、体能评分和合并症综合判断。
食管鳞状细胞癌患者现在更该关注什么?
如果已经确诊,最重要的不是被单一分子名词吓到,而是抓住真正影响预后的决策点。
- 先看分期:局限期与转移期治疗路径完全不同。
- 再看病理与分子信息:明确是否为食管鳞状细胞癌,是否有可参考的生物标志物。
- 评估综合治疗机会:手术、放化疗、免疫治疗、围手术期治疗是否还能优化。
- 复发转移后及时重评估:既往方案失败后,是否有二线、三线、临床试验或海外新药信息可参考。
很多患者的真实痛点并不是“完全不知道治疗”,而是“只知道本地常规方案,不知道全球是否还有更新选择”。这正是分子研究的价值所在:它帮助患者和医生更早发现下一步方向。
基础研究离新药还有多远?
从发现一个促癌分子,到真正出现成熟药物,通常要经历靶点验证、药物设计、动物安全性评价、早期临床试验、扩大样本验证等多个环节。这个过程往往漫长,而且淘汰率很高。
但对晚期癌症患者来说,信息价值并不会因此消失。因为很多前沿治疗机会,恰恰出现在“已发现机制、正在临床验证”的阶段。能否尽早识别这些方向,决定了患者有没有机会接触:
- 更匹配自身分子特征的临床试验;
- 海外已上市、国内尚未普及的抗癌药物信息;
- 联合治疗或后线治疗的新证据;
- 针对耐药、转移、复发场景的个体化方案解读。
面对复发转移,患者如何少走弯路?
真正高质量的抗癌决策,通常要同时回答四个问题:
| 关键问题 | 患者常见困惑 | 更合理的应对方式 |
|---|---|---|
| 还能不能治 | 复发转移是否就没有机会 | 重做分期评估,明确是否仍有局部治疗或系统治疗机会 |
| 该用什么方案 | 化疗、免疫、靶向、试验怎么选 | 结合病理、分子标志物、既往疗效和毒性综合判断 |
| 有没有更新药物 | 本地医院没有的药是否值得了解 | 关注全球指南更新、海外获批药和临床试验动态 |
| 怎么买得到 | 新药可及性和正规渠道不清楚 | 优先核实适应证、处方依据与合规获取路径 |
尤其当病情进入后线治疗阶段,单纯依赖零散搜索,容易被片段化信息误导。把论文机制、临床指南、药物可及性和个体病情放在一起看,才更接近真正有用的答案。
为什么“信息差”本身就是治疗差距?
食管鳞状细胞癌治疗正在不断细化:哪些患者适合围手术期强化治疗,哪些患者更适合免疫联合,哪些患者在复发后还有临床试验窗口,哪些分子通路值得继续追踪,答案都在快速更新。
但现实是,不少患者直到标准方案失败后,才开始补课式了解前沿药物、海外批准进展和替代路径,往往已经错过最佳决策时机。对于这类疾病,时间本身就是预后变量。
因此,越早系统梳理病情,越早看懂像KHSRP-JAK1/STAT3这样的新机制,越有机会把“等进展后再说”变成“提前布局下一步”。
下一步可以如何更高效行动?
如果你或家人正面临食管鳞状细胞癌,尤其是出现复发、转移、疗效不佳、耐药或想寻找下一步方案时,最需要的不是更多焦虑,而是更清晰的决策支持:
- 把病理、分期、既往治疗和当前问题整理成一份完整病情摘要;
- 判断是否需要补充分子检测或重新评估现有检测结果;
- 核对国内外指南和最新研究,确认当前方案是否仍是最优选择;
- 了解前沿药物、临床试验和海外可及治疗信息;
- 在合规前提下,评估后续用药与获取路径。
MedFind长期关注全球抗癌新证据、诊疗指南与药物进展,能够帮助患者把复杂研究翻译成可执行的信息:哪些方向值得问医生,哪些药物已有证据基础,哪些治疗仍处于研究阶段,哪些海外药物具备进一步了解的价值。对于需要进一步寻找抗癌药物可及性方案的患者,也可重点了解跨境直邮与辅助问诊服务,减少因信息滞后带来的治疗耽误。
食管鳞状细胞癌并不等于只能被动等待。看懂机制,是为了看清下一步;找对信息,是为了争取真正可能改变结局的机会。
【参考文献】
Uhlenhopp D J, Then E O, Sunkara T, et al. Epidemiology of esophageal cancer: update in global trends, etiology and risk factors. Clin J Gastroenterol, 2020, 13(6): 1010-1021.
Xu J Y, Wang D S, Ma H L, et al. KHSRP combines transcriptional and posttranscriptional mechanisms to regulate monocytic differentiation. Blood Sci, 2022, 4(3): 103-115.
Olguin S L, Patel P, Buchanan C N, et al. KHSRP loss increases neuronal growth and synaptic transmission and alters memory consolidation through RNA stabilization. Commun Biol, 2022, 5(1): 672.
Chen M M, Wang S L. Preclinical development and clinical studies of targeted JAK/STAT combined Anti-PD-1/PD-L1 therapy. Int Immunopharmacol, 2024, 130: 111717.
Qin Z, Yue M T, Tang S J, et al. EML4-ALK fusions drive lung adeno-to-squamous transition through JAK-STAT activation. J Exp Med, 2024, 221(3): e20232028.
Xue C, Yao Q F, Gu X Y, et al. Evolving cognition of the JAK-STAT signaling pathway: autoimmune disorders and cancer. Signal Transduct Target Ther, 2023, 8(1): 204.
Yang M, He D, Sun Y, et al. The intratumoral landscape of T cell receptor repertoire in esophageal squamous cell carcinoma. J Transl Med, 2024, 22(1): 1069.
Liu Z B, Kim M O. Evolving therapeutic strategies in esophageal squamous cell carcinoma: advances and perspectives. J Cancer Prev, 2024, 29(4): 99-104.
Rogers J E, Sewastjanow-Silva M, Waters R E, et al. Esophageal cancer: emerging therapeutics. Expert Opin Ther Targets, 2022, 26(2): 107-117.
Chen L, Zhao T J. Identification of KHSRP-regulated RNAs in esophageal cancer by integrated bioinformatics analysis. Cancer Biother Radiopharm, 2021, 36(5): 412-424.
Fujita Y, Masuda K, Hamada J, et al. KH-type splicing regulatory protein is involved in esophageal squamous cell carcinoma progression. Oncotarget, 2017, 8(60): 101130-101145.
Gou Q H, Gao L B, Nie X W, et al. Long noncoding RNA AB074169 inhibits cell proliferation via modulation of KHSRP-mediated CDKN1a expression in papillary thyroid carcinoma. Cancer Res, 2018, 78(15): 4163-4174.
Erdogan F, Radu T B, Orlova A, et al. JAK-STAT core cancer pathway: an integrative cancer interactome analysis. J Cell Mol Med, 2022, 26(7): 2049-2062.
Shao F, Pang X N, Baeg G H. Targeting the JAK/STAT signaling pathway for breast cancer. Curr Med Chem, 2021, 28(25): 5137-5151.
Tzeng H T, Chyuan I T, Lai J H. Targeting the JAK-STAT pathway in autoimmune diseases and cancers: a focus on molecular mechanisms and therapeutic potential. Biochem Pharmacol, 2021, 193: 114760.
Rah B, Farhat N M, Hamad M, et al. JAK/STAT signaling and cellular iron metabolism in hepatocellular carcinoma: therapeutic implications. Clin Exp Med, 2023, 23(7): 3147-3157.
Hu Q, Bian Q H, Rong D C, et al. JAK/STAT pathway: extracellular signals, diseases, immunity, and therapeutic regimens. Front Bioeng Biotechnol, 2023, 11: 1110765.
Huang I H, Chung W H, Wu P C, et al. JAK-STAT signaling pathway in the pathogenesis of atopic dermatitis: an updated review. Front Immunol, 2022, 13: 1068260.
Miot H A, Criado P R, De Castro C C S, et al. JAK-STAT pathway inhibitors in dermatology. An Bras Dermatol, 2023, 98(5): 656-677.