很多HER2阳性乳腺癌患者和家属在做新辅助治疗时都会纠结:医生说“通常要做6–9个周期”,可自己(或家人)明明前几次治疗后肿块就明显变小,甚至影像上“几乎看不到了”,还要继续“硬撑”满疗程吗?继续做,担心神经麻木、乏力、腹泻、血象下降越来越重;不继续做,又害怕“是不是治疗不够、会不会复发更高”。
一项名为TRAIN-3的临床研究给出了一个非常重要的新思路:在II–III期HER2阳性乳腺癌中,把增强MRI像“导航仪”一样嵌入治疗流程,动态评估疗效;对早期影像学完全缓解的人群,可能不必“一刀切”做满固定周期的化疗,也能获得很好的长期控制,并显著降低毒性。这篇文章将用患者能听懂的方式,讲清楚这项研究做了什么、结果意味着什么、哪些人可能更适合“减法治疗”,以及你可以如何与医生一起做更稳妥的决策。
先弄明白:HER2阳性乳腺癌为什么“既凶又能治”
把乳腺癌想象成一辆“失控的车”。HER2阳性乳腺癌的特点,是肿瘤细胞表面有很多HER2“油门踏板”,让细胞更容易疯狂生长、扩散。因此在过去,它确实更“凶险”。
但好消息是:HER2也是一个很明确的“靶子”。当抗HER2靶向药出现后,相当于有人能精准去“踩刹车”甚至“拔掉油门线”,治疗结局大幅改善。临床上常用的双靶方案,核心就是曲妥珠单抗(赫赛汀, Trastuzumab)联合帕妥珠单抗(帕捷特, Pertuzumab),再配合化疗药物共同“围剿”肿瘤。
在II–III期(可理解为“早期到局部晚期”)HER2阳性乳腺癌中,很多指南推荐术前进行新辅助治疗(先用药把肿瘤打小、提高保乳/手术质量,并通过肿瘤对药物的反应来判断预后与后续用药)。传统上,新辅助化疗常按固定周期进行(例如6–9周期),但问题也随之出现:不同患者对治疗的敏感性差别很大,有的人“打几次就很干净”,有的人需要更长疗程才能控制。
为什么会出现“化疗周期越短,预后反而更好”的现象?
这里要特别澄清一个容易误解的点:TRAIN-3研究中“做得更少、结果更好”,并不是因为“少做更厉害”,而是因为能在早期就达到影像学完全缓解的人,本身往往代表肿瘤对治疗更敏感、生物学行为更好。换句话说,短程治疗组更像是“被筛选出来的好应答人群”。
真正的关键在于:如果我们能用可靠的方法把这类“快速应答者”识别出来,就可能减少不必要的化疗暴露,让疗效与生活质量实现双赢。
TRAIN-3研究做了什么?用MRI做“疗效导航”
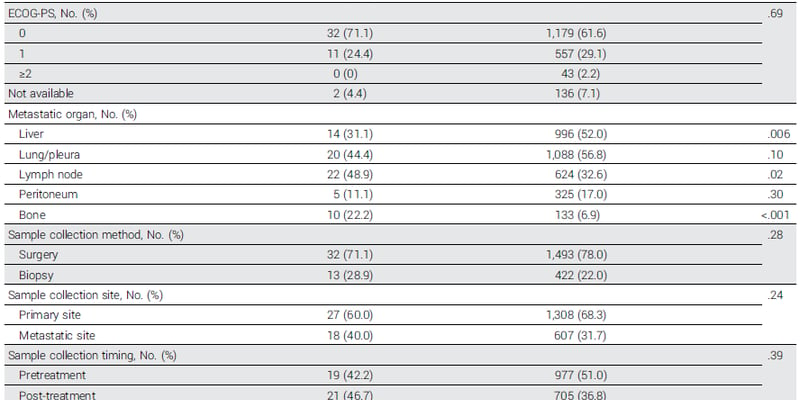
TRAIN-3是一项在荷兰43家医院开展的多中心、单臂、II期临床试验,共纳入467例II–III期HER2阳性乳腺癌患者,其中激素受体阴性235例、激素受体阳性232例。研究的核心不是换新药,而是改变“治疗时长的决策方式”。
1)初始方案:先按统一方案起跑
所有患者起始接受相同的新辅助方案:紫杉醇+卡铂+曲妥珠单抗(赫赛汀, Trastuzumab)+帕妥珠单抗(帕捷特, Pertuzumab),最多计划9个周期。
2)关键步骤:每3周期做一次增强MRI
每完成3个周期,进行乳腺增强MRI评估。如果在“原始肿瘤区域”看不到病理性的对比增强(研究中将其定义为影像学完全缓解),则提前转入手术;如果仍有增强提示残留,则继续化疗,最多到9个周期。
你可以把增强MRI理解为“给肿瘤拍一段短视频”:不是只看“体积变没变小”,更看“肿瘤组织还有没有活跃的血供和代谢特征”。当增强信号消失,往往提示肿瘤活性明显下降。

增强MRI被用于动态评估疗效,决定是否提前手术与缩短化疗周期
3)术后策略:根据病理结果“分层加固”
手术后再根据病理结果决定辅助治疗:
- 病理完全缓解(pCR)者:继续完成1年双靶辅助治疗。
- 有残留病灶者:改用恩美曲妥珠单抗(赫赛莱, Trastuzumab emtansine)强化治疗,并按当地指南接受放疗与(如适用)内分泌治疗。
这一步非常重要:它意味着“提前手术、缩短化疗”并不是“放任不管”,而是把治疗变成更精确的“该加的加、该减的减”。
研究结果怎么解读?把数字翻译成“对患者意味着什么”
研究中位随访40.1个月,给出了3年无事件生存(EFS)和总生存(OS)等关键结局。
1)整体生存:两类人群3年控制率都很高
整体人群中:
- 激素受体阴性患者:3年EFS为92.2%,3年OS为97.8%。
- 激素受体阳性患者:3年EFS为92.0%,3年OS为98.7%。
对患者来说,EFS可以粗略理解为“在随访时间内,不出现复发、进展或死亡等事件的概率”。这类数据越高,通常意味着长期控制更稳。
2)按实际化疗周期分层:早期影像学缓解者结局最好
研究把患者按实际接受的化疗周期分组,出现了非常值得关注的差异:
| 分组(实际化疗周期) | 激素受体阴性 3年EFS | 激素受体阳性 3年EFS |
|---|---|---|
| 1–3周期(早期影像学缓解者) | 96.1% | 98.6% |
| 4–6周期 | 89.2% | 94.2% |
| 7–9周期 | 90.6% | 85.4% |
请注意:这不是在鼓励所有人“越少越好”,而是提示当MRI在早期就显示非常好的应答时,缩短疗程可能是安全的,并且这些患者本身属于预后更佳的一群。

不同化疗周期分层后,早期影像学缓解者的3年EFS最高
3)pCR与长期获益:pCR人群复发风险更低
研究显示:达到pCR者的3年EFS显著优于未达到者(94.8% vs 87.5%,HR=0.40)。
把HR=0.40翻译成人话就是:在这项研究中,达到pCR的人群发生不良事件的风险,大约比未达到pCR的人群低很多。也因此,pCR常被视为新辅助治疗中一个重要的“替代指标”。
4)毒性:少做几个周期,神经病变可能少很多
患者最关心的往往不是抽象的统计学,而是“我会不会更难受”。TRAIN-3给出了非常清晰的毒性梯度:治疗相关不良事件随着化疗周期延长而递增;3–4级不良事件多发生在新辅助阶段,主要包括中性粒细胞减少、贫血、腹泻等。
尤其值得关注的是周围神经病变(常见表现为手脚麻木、刺痛、拿筷子不稳、走路像踩棉花):≥2级神经病变发生率在不同周期组分别为:
- 1–3周期:13%
- 4–6周期:35%
- 7–9周期:51%
这意味着,如果你属于MRI提示早期完全缓解的人群,减少后续化疗暴露,可能显著降低神经损伤的概率,也更有利于工作、睡眠、饮食和情绪的恢复。
5)复发模式:提前手术并未带来更多远处转移
研究中,接受1–3周期化疗后提前手术的患者,仅2例(1%)出现远处复发。这个结果为“提前手术+缩短化疗”的安全性提供了重要支持。
哪些患者可能更适合MRI指导的“反应适应性”策略?
从研究描述看,这一策略在不同亚组中可能存在差异:
- 激素受体阴性:MRI预测pCR的表现更好(研究报告阴性预测值87%),因此用MRI来筛选早期应答者可能更“靠谱”。
- 激素受体阳性:MRI预测价值相对较低(研究中提到为53%),意味着仅凭MRI判断可能更容易出现“不够准”的情况。但即便如此,早期缓解者的生存数据仍然非常出色,提示策略仍有应用空间,未来可能需要叠加更多指标(如PET/CT、ctDNA等)提升筛选准确性。
对患者而言,你可以把它理解为:同样是“导航”,有些路况下GPS更准,有些路况下需要“GPS+路标+经验”一起判断。
患者最常见的4个疑问:我们给出更落地的回答
疑问1:肿块很快变小,是不是就可以少化疗?
不一定。肿块变小是好事,但“变小”不等于“活性消失”。TRAIN-3用的是增强MRI的影像学完全缓解作为决策依据,而不是单纯触诊或普通超声的大小变化。你可以和医生讨论:是否有条件在治疗早期进行更系统的影像评估,并由乳腺影像经验丰富的团队判读。
疑问2:少化疗会不会影响治愈率?
在TRAIN-3的设计里,“少化疗”并不是直接把标准治疗砍掉,而是:当MRI提示早期完全缓解时先手术,术后再用病理结果来决定后续强度。也就是说,它是“前段减量、后段兜底分层”。这也是它能兼顾安全性的关键。
疑问3:如果术后发现没达到pCR怎么办?
研究中对残留病灶的处理是更积极的强化方案:使用恩美曲妥珠单抗(赫赛莱, Trastuzumab emtansine)。这类“术后按残留升级治疗”的思路,正是现代HER2阳性乳腺癌个体化治疗的核心之一。
疑问4:我在国内,MRI指导缩短疗程能照搬吗?
现实中需要满足几个条件:影像设备与判读质量、肿瘤多学科团队(MDT)协作、以及医生是否将“反应适应性”作为可讨论选项。更重要的是:这是一项单臂II期研究,缺少与标准固定周期方案的直接随机对照比较,随访时间也仍在延长中。因此,它更像是一个强有力的“新证据与新方向”,而不是所有人都应立刻照搬的“唯一答案”。
居家管理:如果你正在做紫杉醇/卡铂+双靶,这些细节很关键
无论你最终是标准疗程还是在医生评估后考虑缩短疗程,把副作用管理好,都能直接影响你能否按计划完成治疗、也影响生活质量。
1)手脚麻木刺痛(周围神经病变)
- 尽早记录:用0–10分记录麻木刺痛程度、是否影响扣纽扣/写字/走路,并在每次复诊主动告诉医生。
- 避免加重刺激:减少长时间冰冷刺激(如直接接触冰水)、避免紧鞋和久站久蹲。
- 安全优先:夜间起床开小夜灯;洗澡水温不要过高,防止感觉迟钝导致烫伤。
出现进行性加重、影响日常生活时,应尽快与医生讨论是否需要调整化疗剂量、间隔或对症处理。
2)腹泻(双靶相关更常见)
- 补液与电解质:少量多次喝温水、口服补液盐;若合并头晕、尿量明显减少,尽快就医。
- 饮食:腹泻期选择“低脂、低乳糖、易消化”,如米粥、面条、蒸蛋;暂避辛辣、酒精、油炸、奶茶。
- 警惕红旗:发热、血便、严重腹痛、一天多次水样便止不住,应及时到医院评估感染与脱水。
3)血象下降(中性粒细胞减少、贫血)
- 感染防护:人多处戴口罩、勤洗手;出现发热要把“化疗后发热”当急症处理,按医生给的流程尽快就诊。
- 营养支持:优先保证蛋白质(蛋、鱼、瘦肉、豆制品),少量多餐;恶心时用清淡高蛋白食物替代大油大荤。
4)情绪与睡眠:把“不确定感”变成“可执行清单”
新辅助治疗最折磨人的往往不是某一个副作用,而是反复担心“到底有没有效”。建议你每个周期后做三件事:
- 把症状变化、体重、食欲、睡眠写下来,复诊时带给医生。
- 询问下一步评估节点(例如何时复查MRI/超声、何时讨论手术)。
- 把“我能做的事”具体化:规律散步、蛋白质摄入、避免感染、按时复诊。可控感会显著减轻焦虑。
药物可及性与现实路径:你可以怎样更高效地获得“前沿方案信息”
HER2阳性乳腺癌的治疗是“药物+手术+放疗+(部分人需要)内分泌”的组合拳。很多家庭真正缺的不是“勇气”,而是两件事:第一,是否存在更适合自己的个体化路径;第二,关键药物在不同地区的可及性与用药衔接。
在MedFind,我们更希望把你的决策过程变得清晰可控:
- AI辅助问诊与方案解读:把你的分期、激素受体状态、影像与病理要点整理成“可与医生讨论的清单”,帮助你理解像EFS、pCR、MRI评估这类关键信息,避免在诊室里因为紧张而漏问。
- 抗癌药品跨境直邮信息支持:当你与主治医生共同确定需要某些关键药物或后续方案时,我们可协助你了解不同地区的药物版本、合规获取路径与用药衔接注意事项,让治疗不中断、少走弯路。
最重要的是:无论你是否符合“缩短化疗周期”的条件,都值得把治疗做得更“精准”。如果你已经在新辅助治疗中,建议你准备好三个问题在下一次复诊时问医生:第一,我的激素受体状态与HER2状态具体是什么;第二,我的疗效评估计划是什么(何时做增强MRI或其他评估);第三,如果早期评估非常好,是否存在个体化缩短疗程或提前手术的讨论空间,以及术后若未pCR如何强化。
参考信息
Louis FM, van der Voort A, van Ramshorst MS, et al. MRI-based personalisation of neoadjuvant chemotherapy duration in HER2-positive early breast cancer (TRAIN-3): primary results from a multicentre, single-arm, phase 2 study. Lancet Oncol. 2026;27(3):349-360. doi:10.1016/S1470-2045(25)00707-7