当家里有人确诊癌症,很多人都会在搜索框里反复输入同一个问题:“有没有更有效、但副作用更小的新疗法?”近几年,CAR-T细胞疗法让部分血液肿瘤患者看到长期缓解的希望,但同时也让不少家庭担心细胞因子释放综合征(CRS)、神经毒性和住院监护等风险。于是,越来越多人开始关注另一条正在快速发展的路线:CAR-NK细胞疗法。
这篇文章会用患者能听懂的语言,系统讲清楚:CAR-NK到底是什么、它和CAR-T差在哪、目前临床试验到哪一步、哪些肿瘤更可能获益、风险和局限是什么,以及你去医院或咨询医生时应该问哪些关键问题。希望你读完后,能更踏实、更有方向地做决策。

CAR-NK细胞疗法:更安全的“现货型”细胞治疗正在加速推进
一、CAR-NK细胞疗法是什么?一句话讲明白
CAR-NK细胞疗法可以理解为:把人体或供体的自然杀伤细胞(NK细胞)“升级改造”,给它装上一套能识别肿瘤特定标记的“导航系统”(CAR,嵌合抗原受体),让它更精准、更有力地去杀伤癌细胞。
如果用一个比喻:NK细胞本来像“巡逻的特警”,擅长发现“行为异常”的细胞并快速处置;CAR则像给特警配了一张“精准通缉令”,只要看到肿瘤细胞带着某个特定“身份证”(靶抗原),就能立刻锁定并攻击。
二、CAR-NK vs CAR-T:患者最关心的差异是什么?
很多患者会问:“既然有CAR-T,为什么还需要CAR-NK?”核心原因在于安全性、供给方式与持久性的权衡。
| 对比维度 | CAR-T | CAR-NK |
|---|---|---|
| 主要优势 | 体内扩增强,可能更持久;部分血液肿瘤疗效明确 | 理论与早期数据提示更低CRS与GvHD风险;更有望做成“现货型” |
| 典型风险 | CRS、神经毒性等需要严密监护 | 总体毒性更轻,但仍需警惕感染、发热、血象变化等 |
| 是否容易做“现货” | 多为自体定制,制备周期与成本较高 | 更适合同种异体批量化(如脐带血、iPSC来源) |
| 体内持久性 | 往往更强,可形成记忆样细胞 | 常仅持续数周,可能需要细胞因子支持或重复给药 |
对多数家庭来说,CAR-NK最吸引人的点通常是:更安全的可能性与更可规模化的供给。但同时也要清楚:它目前仍处在快速迭代的早期阶段,很多问题仍在临床试验中回答。
三、NK细胞为什么能“天生会杀癌”?关键机制用通俗方式解释
NK细胞属于先天免疫的重要成员,它的本领来自一套“平衡系统”:一边是“可以打”的信号,一边是“别误伤自己人”的刹车信号。
- 加速器(激活受体):例如NKG2D、DNAM-1、NCR家族(NKp30、NKp44、NKp46)等,它们更容易识别那些“受了刺激、受损或发生恶变”的细胞,因为这些细胞表面会出现一些“应激信号”。
- 刹车(抑制受体):健康细胞表面通常会表达MHC I类分子,相当于挂着“我是自己人”的牌子;NK细胞上的KIR等抑制性受体看到后,会阻止攻击,避免误伤。
肿瘤细胞有时会“耍赖”:要么伪装自己人,要么改变表面信号躲过识别。CAR-NK的意义就在于:在NK细胞原有识别能力上,再加一个“明确指向某个肿瘤抗原”的识别模块,提高命中率。
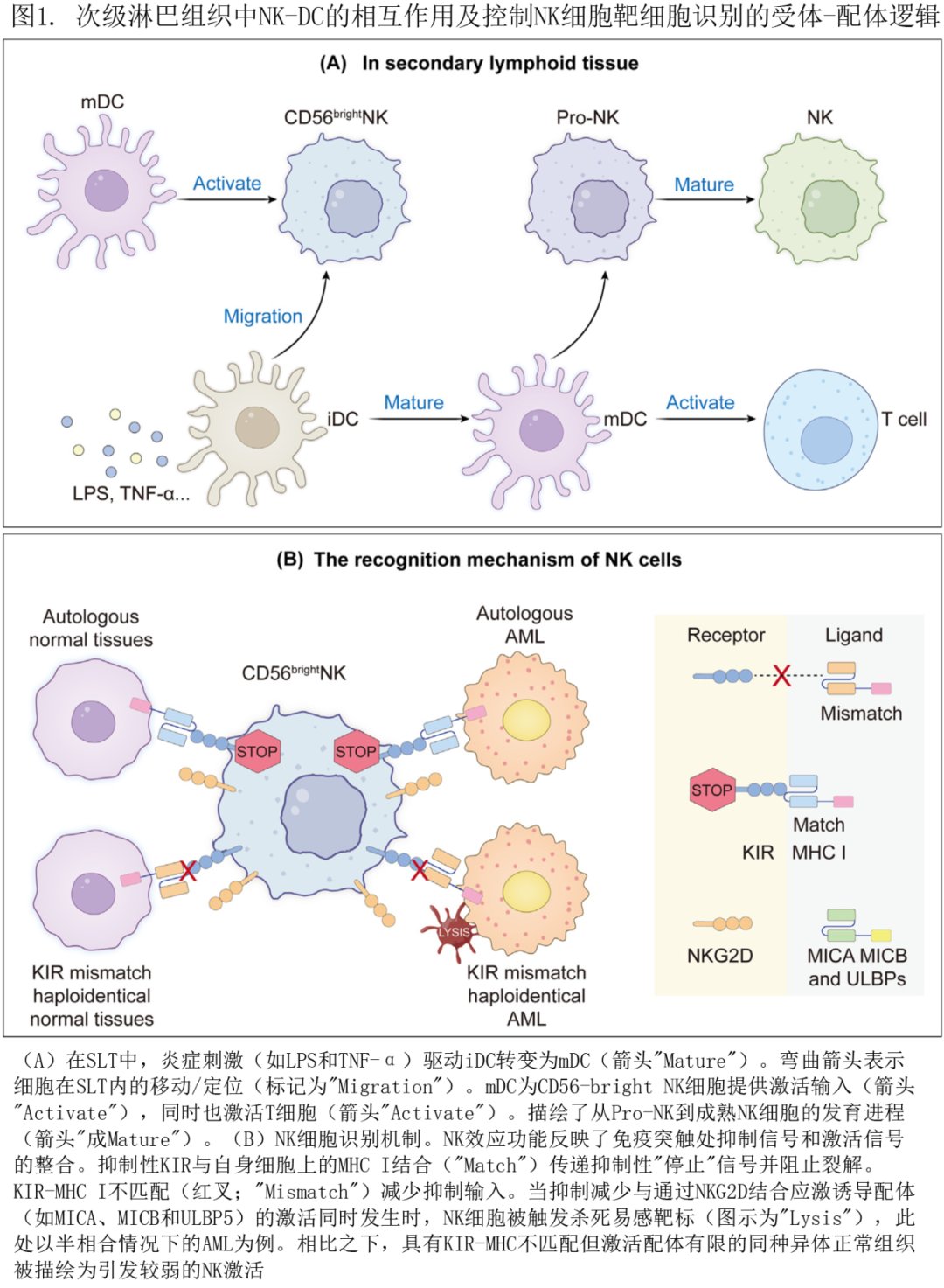
NK细胞依靠“激活与抑制信号平衡”来区分异常细胞与健康细胞
四、CAR结构怎么“装”到NK细胞上?理解模块化设计,能帮你看懂新技术
CAR并不是一个“单一零件”,更像由三部分组成的可拼装模块:
- 胞外结合区:常来自抗体的scFv,负责“认人”——识别肿瘤抗原。
- 跨膜区(TM):像“螺丝钉”,把CAR固定在细胞膜上,并影响信号传导质量。
- 胞内信号区:像“启动按钮”,一旦识别成功,就触发杀伤、脱颗粒、细胞因子分泌等反应。
很多患者看到“双靶点CAR”“逻辑门控”“装甲CAR”等术语会很迷糊。你可以这样理解:
- 双靶点/多靶点:相当于“核对两张证件”,减少肿瘤逃逸,也尽量降低误伤正常组织的风险。
- 逻辑门控(如AND门):只有当肿瘤同时满足多个条件,CAR才“真正开火”。
- 装甲CAR:给CAR-NK加上“抗干扰装备”,例如抵抗肿瘤微环境抑制或自带细胞因子支持。
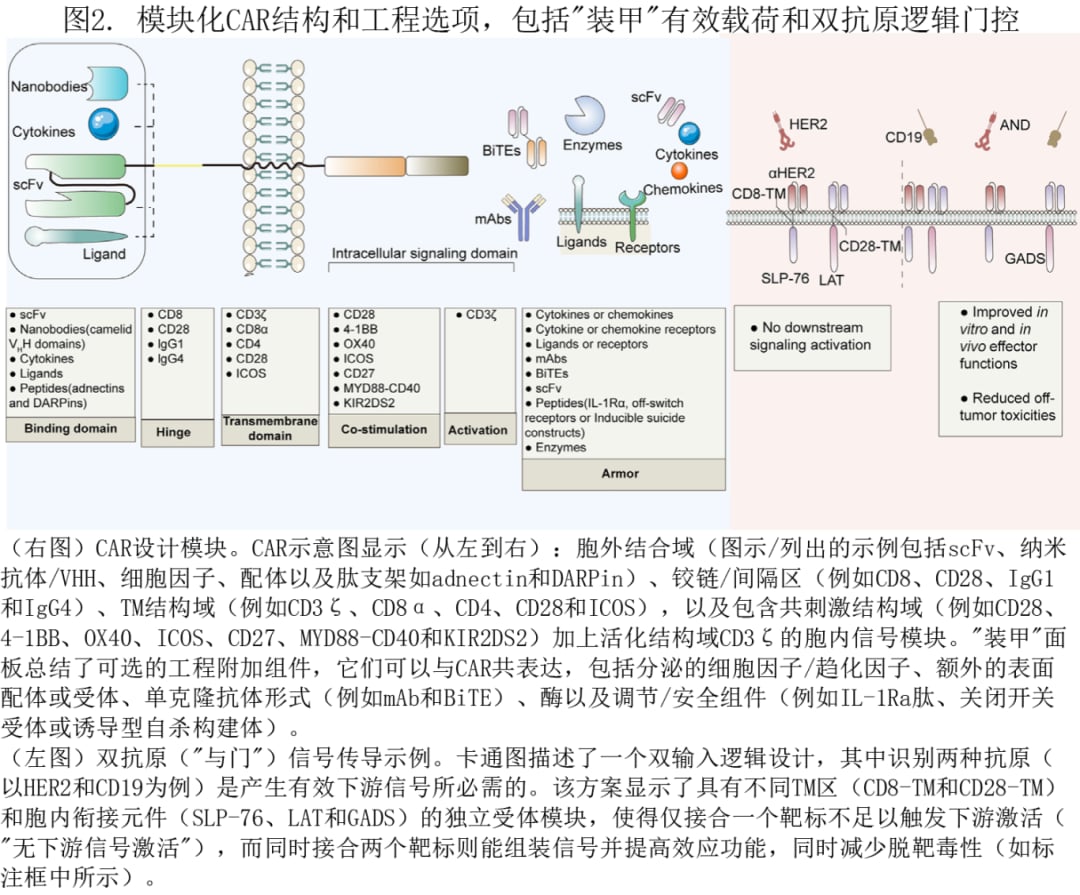
CAR的模块化结构让研究者能像“搭积木”一样迭代安全性与疗效
五、CAR-NK怎么生产?为什么“细胞来源”会影响疗效与可及性
一个CAR-NK产品大致要经历:获取NK细胞→导入CAR基因→扩增→质控→制成输注剂型→静脉回输。
不同来源的NK细胞,决定了它更像“私人订制”还是“现货供应”。目前常见来源包括:
- 外周血来源(PB-NK):更接近“研究者发起或患者特异”产品,但供体差异、扩增能力限制较明显。
- 脐带血来源(UCB-NK):更适合建库和标准化,早期临床中也有较突出的安全性信号。
- 诱导多能干细胞来源(iPSC-NK):更有潜力做成稳定批量化“现货型”,但制造体系与监管要求更复杂。
- NK-92细胞系:易扩增、易改造,常用于概念验证;但由于其特殊来源及对IL-2依赖等特性,临床使用时往往需要额外处理(例如输注前照射),可能影响体内持久性。
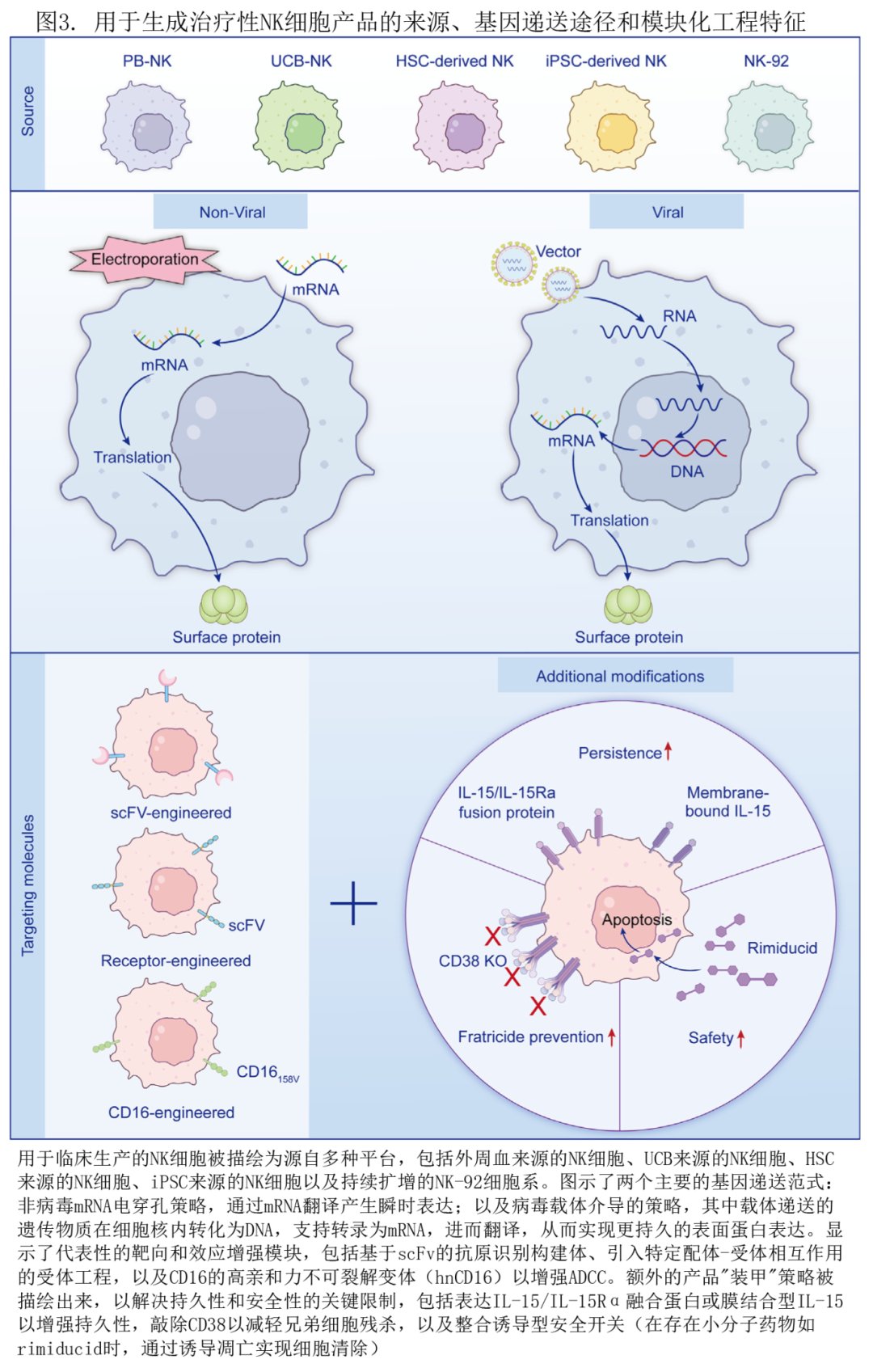
CAR-NK常见“升级项”:CD16增强ADCC、IL-15支持持久性与安全开关
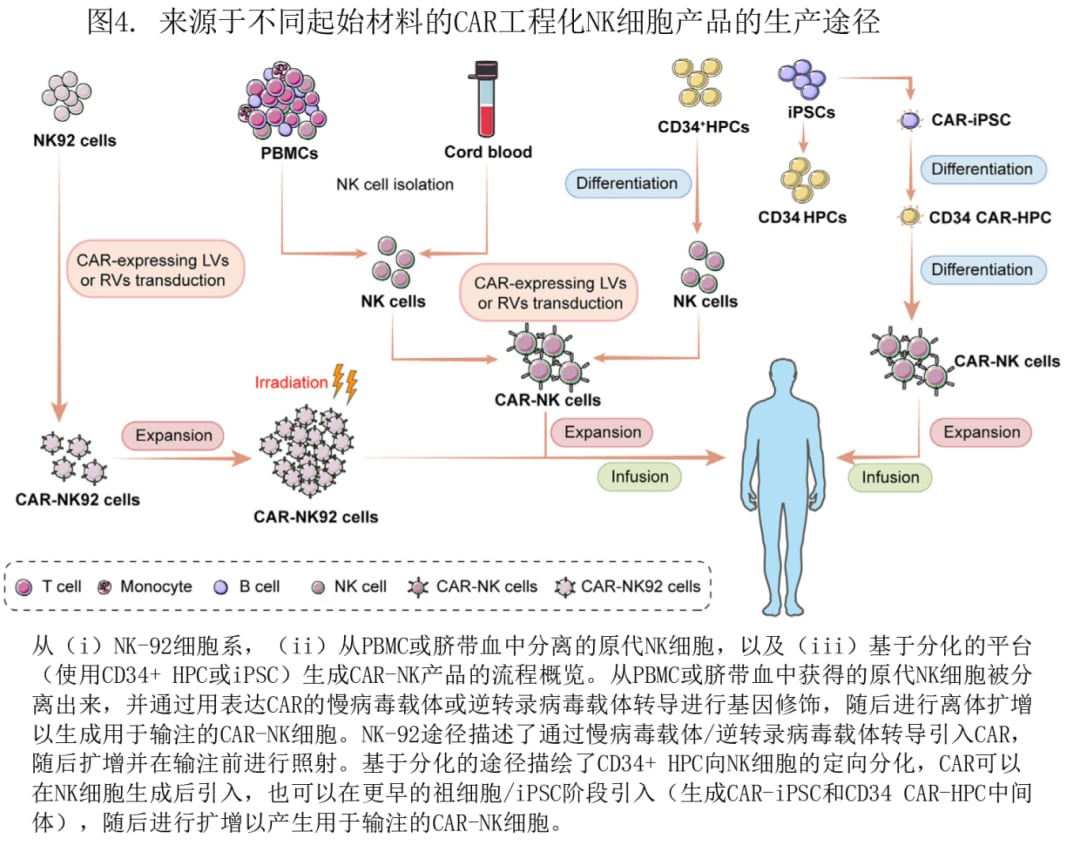
不同细胞来源与递送方式,会影响产量、标准化、成本与持久性
六、目前有哪些“有数字”的临床证据?把关键结果讲清楚
1)里程碑:脐带血来源CD19 CAR-NK早期研究(NCT03056339)
在一项早期临床试验中,同种异体、脐带血来源、靶向CD19的CAR-NK用于治疗复发/难治性CD19阳性恶性肿瘤(包括非霍奇金淋巴瘤和慢性淋巴细胞白血病)。关键点包括:
- 样本量:n=11。
- 疗效信号:7名患者在单次输注后达到完全缓解;中位完全缓解持续时间为13.8个月。
- 安全性:未观察到≥3级CRS或GvHD。
- 剂量与反应:在1×10^6细胞/kg剂量下客观缓解率为73%,而在0.1×10^6细胞/kg剂量下为36%。
对患者家庭来说,这组数据最“打动人”的往往是:在高风险人群中,出现了可观的缓解,同时严重CRS与GvHD并未成为主要障碍。但也要理性看待:这是早期、小样本研究,不能简单等同于“已经成熟的标准疗法”。
2)实体瘤探索:HER2、CD30、EGFRvIII等靶点正在推进
目前临床管线已覆盖多种抗原和适应症,例如:
- HER2靶向CAR-NK:用于HER2阳性实体瘤的探索性研究中,曾报道复发乳腺癌伴肺转移患者的疾病控制率为55%,并有一例肿瘤缩小40%;且外周血中可检测到CAR-NK持续存在长达4周。
- CD30靶向CAR-NK:被推进用于复发或难治性CD30阳性淋巴瘤(含霍奇金淋巴瘤)。
- 胶质母细胞瘤方向:在NCT04116993研究中,EGFRvIII-CAR-NK联合化疗使中位总生存期达到14.2个月,比单独化疗改善5.3个月。
实体瘤往往更难,是因为肿瘤细胞“长得不一样”(抗原异质性)、免疫细胞“不好进去”(归巢障碍),以及肿瘤微环境像“沼泽地”(TGF-β、腺苷、缺氧、营养竞争等抑制因素)。因此,实体瘤中的CAR-NK更常走“联合策略”和“装甲设计”的路线。
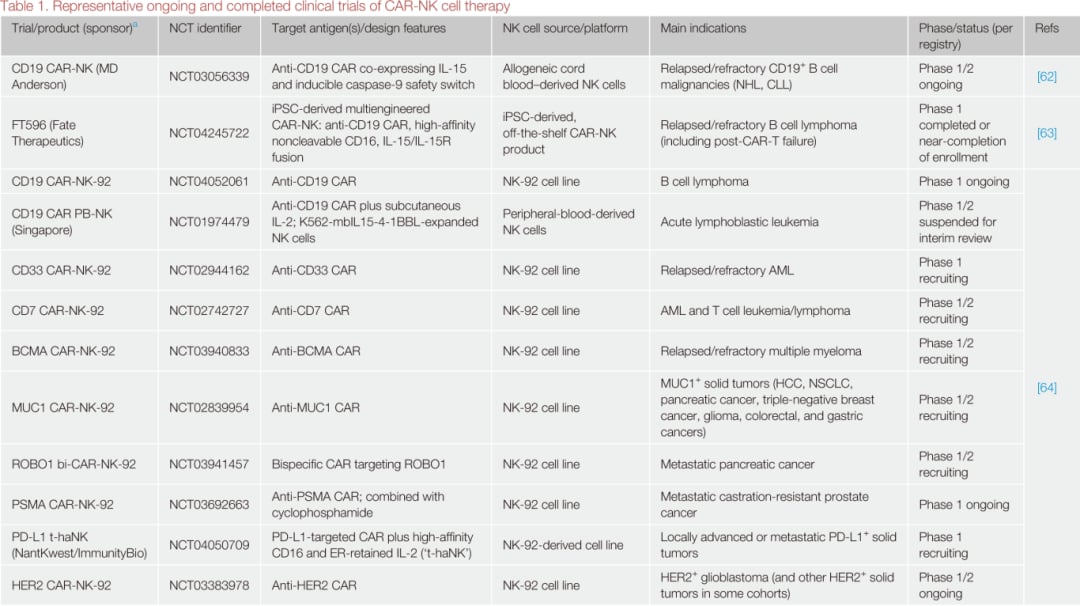
CAR-NK临床试验正在覆盖更多靶点与肿瘤类型,但多数仍处于早期阶段
七、CAR-NK为什么被认为“更安全”?患者需要知道的风险边界
CAR-NK被寄予“更安全”的期待,核心来自其生物学特点与早期临床观察:严重CRS与GvHD发生率可能更低。但“更安全”不等于“没有风险”。你需要和医生重点确认以下几类问题:
1)CRS仍可能发生:识别早期信号很关键
CRS常见早期表现可能包括发热、乏力、心率增快、血压变化等。即使风险相对更低,临床上依然会严格监测,因为一旦进展会影响多器官功能。
2)感染与血象变化:很多细胞治疗都绕不开
多数细胞治疗前后会配合清淋或其他治疗,患者可能出现白细胞、淋巴细胞等变化,感染风险会上升。家庭护理上要做到:
- 发热及时就医:不要在家硬扛。
- 减少聚集与交叉感染:尤其在血象低谷期。
- 饮食卫生:避免生食、隔夜食物,注意厨房案板分开。
3)神经毒性:CAR-NK总体较少见,但仍需警惕
出现意识改变、持续头痛、抽搐、语言障碍等情况,应立即联系治疗中心。
八、最大瓶颈:为什么CAR-NK“打得快”,但可能“留不久”?
目前CAR-NK面临的核心障碍之一是体内持久性不足:NK细胞往往只持续数周,体内扩增能力有限。对患者来说,这意味着:
- 肿瘤控制可能需要重复输注或更强的支持策略。
- 研究者会尝试在不增加毒性的前提下,让细胞“更能活、更能打”。
因此你会看到很多“增强持久性”的策略,最典型的是IL-15支持:要么外源给药,要么让CAR-NK自身共表达IL-15或IL-15Rα,形成更持续的生存信号。但同样重要的是:任何增强免疫活性的设计,都必须平衡潜在全身毒性与安全开关的配置。
九、肿瘤微环境(TME):实体瘤患者一定要理解的“隐形对手”
很多患者会困惑:为什么血液肿瘤看起来更容易出效果,而实体瘤更难?可以把肿瘤微环境想象成肿瘤给自己修建的“堡垒”:
- TGF-β等抑制信号像“催眠剂”,让NK细胞变钝。
- 缺氧与营养竞争像“断粮断氧”,让免疫细胞打不动。
- 腺苷等代谢物像“烟雾弹”,干扰杀伤功能。
因此,很多CAR-NK研发会走“装甲化”路线,例如引入显性负性TGF-β受体,让细胞在高TGF-β环境下也能保持部分效应功能;或采用联合治疗,先“拆堡垒”,再让CAR-NK进入战场。
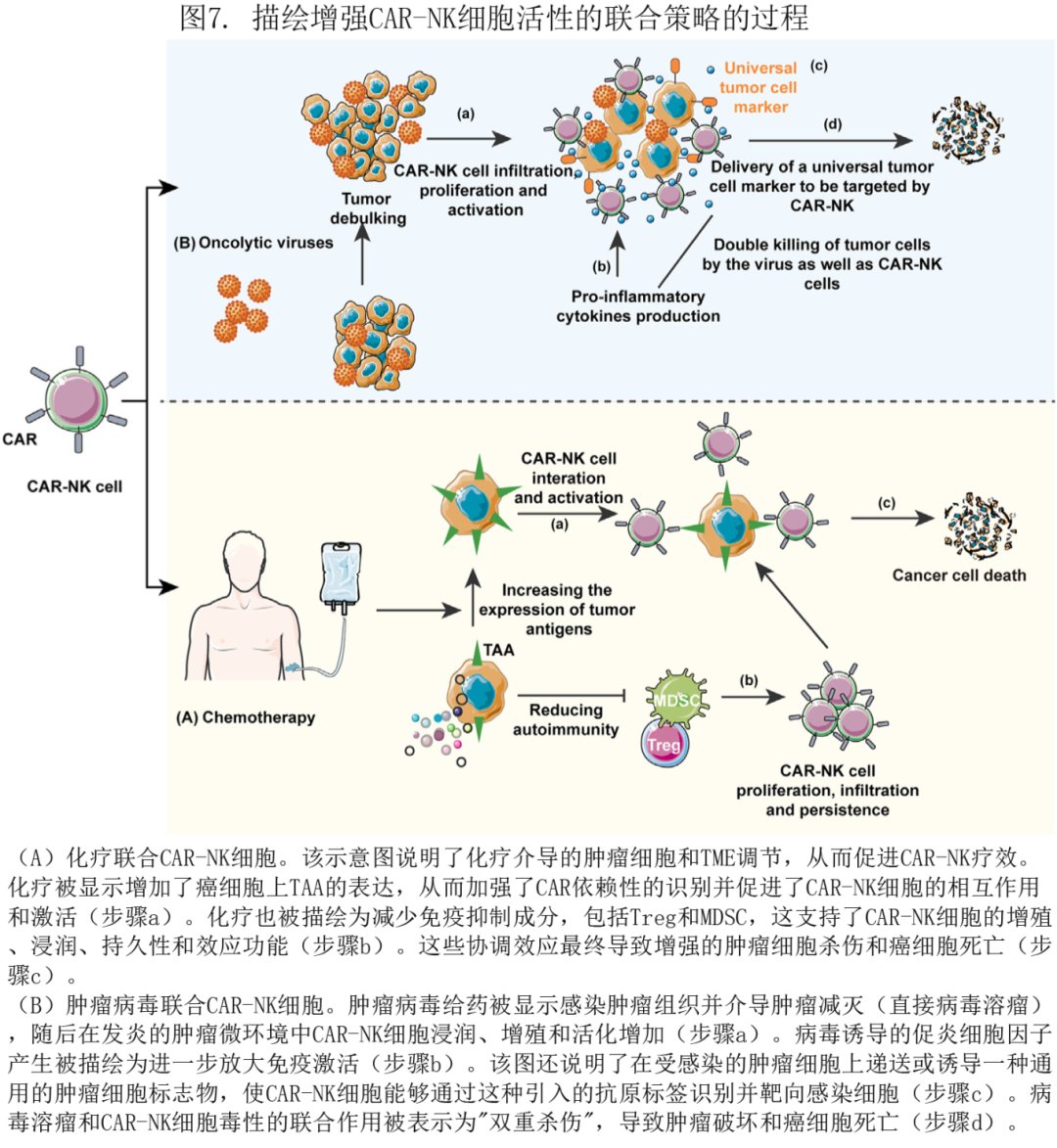
面对实体瘤,CAR-NK常需要联合治疗或装甲设计以对抗肿瘤微环境
十、技术升级:CRISPR、双靶点、SynNotch为什么重要?
1)CRISPR/Cas9:让细胞“按图纸精准改造”
基因编辑的意义在于:不仅能更稳定地插入CAR,还能“拆掉刹车”或“装上防护”。例如:
- 敲除CISH可解除IL-15信号抑制,使CAR-NK增殖能力提高三倍(属于研究中机制数据,临床获益仍需更多试验验证)。
- 在PD-L1高表达肿瘤背景下,删除PD-1基因后,CAR-NK细胞毒性提高约40%(为研究数据,具体人群获益仍需临床证据)。
- 通过破坏KLRC1(与NKG2A相关)可增强对HLA-E阳性肿瘤的脱颗粒与杀伤。
对患者而言,你不需要记住每个基因名字,但要理解:这些改造的目标是让CAR-NK在人体内更持久、更不怕抑制、更不易被排斥。
2)双靶点与逻辑门:减少“逃逸”和“误伤”
肿瘤最常见的“耐药方式”之一,是把目标抗原“藏起来”或换装。双靶点CAR的理念是:让肿瘤更难通过单一抗原丢失来逃脱。在临床前模型中,双靶点CAR-NK消除CD19逃逸肿瘤的效果比单靶点高出2.8倍(属于实验模型结果)。
十一、生产与可及性:为什么很多人关心“现货型”
现实世界里,治疗是否能用上,不只取决于疗效,还取决于生产、成本、时间与质量一致性。CAR-NK之所以被认为更有希望实现“现货型”,是因为脐带血与iPSC等来源更容易标准化建库与批量生产。
但生产仍有硬挑战:扩增、冻存、运输、冻融都可能影响活力、迁移能力和ADCC等功能;而不同中心、不同批次之间的一致性也需要严格的GMP与放行检测来保障。
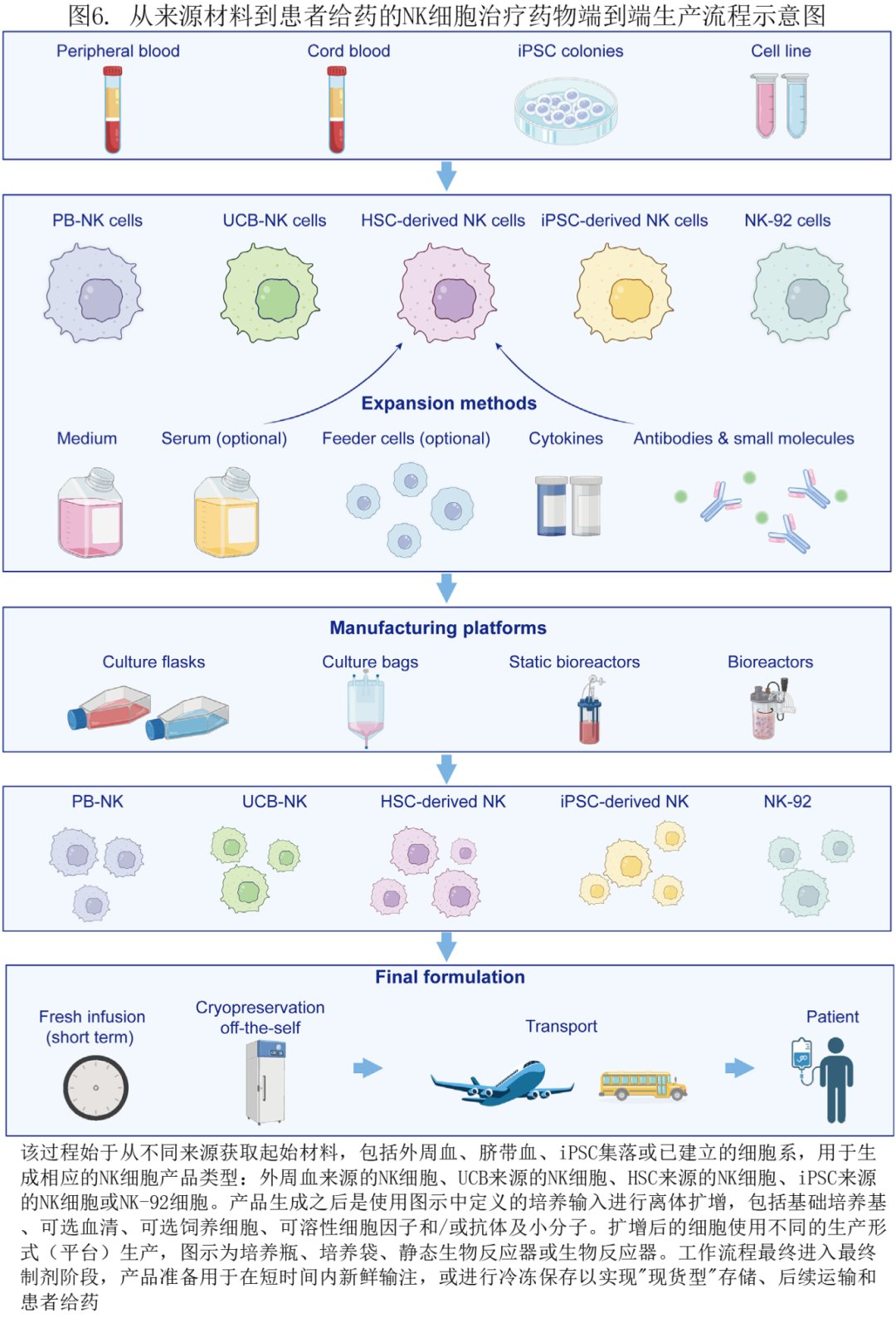
从小规模到工业化放大:质量控制与一致性是“现货型”落地的关键
十二、患者行动清单:如果你想了解或尝试CAR-NK,建议这样准备
1)先确认自己是否“适合去评估”
- 疾病类型与靶点:是否有明确靶抗原(如CD19、CD30、HER2、EGFRvIII等),肿瘤是否检测过相关标志物。
- 既往治疗史:是否复发/难治,是否做过移植、CAR-T、放化疗等。
- 身体状态:感染控制、器官功能、体能评分等是否满足试验入组或治疗要求。
2)与医生沟通时,建议把问题问到“可落地”
- 这项CAR-NK是临床试验还是已常规可用?研究阶段是什么?主要终点是什么?
- 细胞来源是什么(外周血/脐带血/iPSC/NK-92)?是否为同种异体“现货型”?
- 预计的主要风险是什么?中心对CRS、感染、神经毒性有哪些应急流程?
- 是否需要清淋或联合化疗?住院多久?复查频率如何安排?
- 如果复发或无效,有哪些后续路径(其他试验、靶向药、放疗、移植等)?
3)居家管理要点:把“警报线”写下来
- 体温与症状记录:发热、寒战、呼吸困难、持续腹泻、意识改变等,任何一项出现都要及时联系治疗中心。
- 用药与复诊遵从:免疫相关治疗往往对时间窗敏感,不要擅自停药或延误复查。
- 营养与睡眠:优先保证蛋白质摄入与足够热量;在食欲差时用少量多餐、能量密度更高的食物。
- 心理支持:细胞治疗常伴随等待和不确定性,建议家庭把“信息收集、沟通、陪护”分工,减少单人承压。
十三、写在最后:把希望放在“更清晰的路径”上
CAR-NK细胞疗法之所以值得关注,是因为它正在尝试解决细胞治疗长期存在的痛点:在保持抗肿瘤效应的同时,尽可能降低严重CRS与GvHD风险,并推动“现货型”规模化可及。与此同时,它也确实面临现实难题:体内持久性、实体瘤微环境、宿主排斥、制造一致性与成本。
对患者家庭来说,最重要的不是追逐每一个新名词,而是把问题落到三件事上:你是否适合评估、证据处在什么阶段、风险是否可管理。只要这三点清楚,你就能更有底气地选择下一步。
如果你正在寻找更系统的路径,MedFind可以提供两类帮助:第一,整理并解读前沿治疗与临床试验信息,结合你的病理分型、靶点检测与既往治疗,辅助你与医生沟通关键问题;第二,对于已经明确需要的抗癌药物(例如在脑肿瘤联合方案中常被讨论的替莫唑胺(泰道, Temozolomide)等),可协助了解不同地区的用药信息与获取路径,帮助你更快、更稳地把治疗推进下去。你不需要一个人硬扛,把信息和行动路线理清,往往就是走向希望的第一步。
参考信息
Trends Biotechnol. 2026 Feb 16:S0167-7799(25)00541-4. doi: 10.1016/j.tibtech.2025.12.020.