2026年2月,国际顶尖科学期刊《Cell》再次刊载了一系列重磅研究,这些突破性成果不仅刷新了我们对生命基础机制的认知,更在癌症、神经系统疾病等重大医学难题的治疗领域点燃了新的希望。对于正在寻求新治疗方案的癌症患者及家属而言,了解这些前沿进展至关重要。本文将为您深入解读这些研究亮点,帮助您把握未来医学趋势,为您的治疗决策提供更多参考。
一、颠覆认知:巨型DNA病毒的蛋白质合成之谜
传统生物学认为,病毒是严格依赖宿主细胞进行蛋白质合成的,自身不具备完整的翻译机制。然而,近期发表在《Cell》上的一项研究,彻底挑战了这一根深蒂固的观点。科学家们在一种名为棘阿米巴多食棘阿米巴米米病毒的巨型DNA病毒中,发现了一种与真核细胞(如人类细胞)功能相当的新型蛋白质生成机制。通过质谱、晶体学和同源性搜索等尖端技术,研究团队成功识别并命名了病毒IF4A和病毒IF4E这两种关键蛋白质,它们与真核细胞中负责翻译起始的eIF4A和eIF4E蛋白高度同源,共同组成了病毒特有的IF4F帽结合翻译起始复合物。
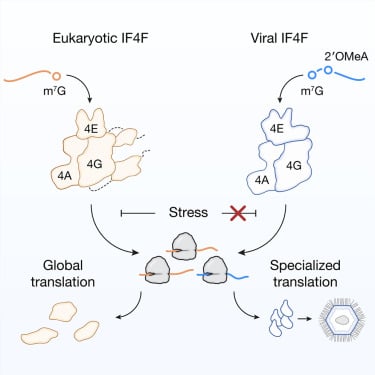
进一步的研究揭示,这个病毒IF4F复合物在病毒感染后期,能够协调结构蛋白的合成,并且通过一种进化的创新,介导m7G帽识别,从而实现对转录的特异性调控。实验结果显示,一旦破坏vIF4F,病毒的复制和结构蛋白合成会受到严重损害,这强有力地证明了病毒对这一复合物的生存依赖性。这项发现不仅模糊了病毒与细胞生命之间的界限,更深远地影响了我们对生命起源和演化的理解。对这一机制的深入探索,有望为未来抗病毒药物的研发提供全新的思路和潜在靶点,例如通过靶向病毒特有的翻译机制来抑制病毒复制,从而为治疗各种病毒感染性疾病带来新的可能。
二、全球连接:微生物组的生态奥秘及其潜在医学价值
微生物组,即我们体内及周围环境中数万亿微生物的集合,对人类健康有着深刻的影响。一项同样发表于《Cell》杂志的开创性研究,揭示了微生物组在全球范围内的相互连接性。EMBL海德堡分校Bork课题组的科学家通过分析数万个宏基因组数据,发现生活在相似栖息地中的微生物,其相似性远高于仅仅居住在同一地理区域的微生物。更令人惊讶的是,他们识别出了一类被称为“通才型”的微生物,它们具备极强的生态耐受性,能够在截然不同的栖息地中繁盛,并与其他微生物进行广泛的相互作用和基因转移,从而构建了一个相互连接的全球性微生物组网络。
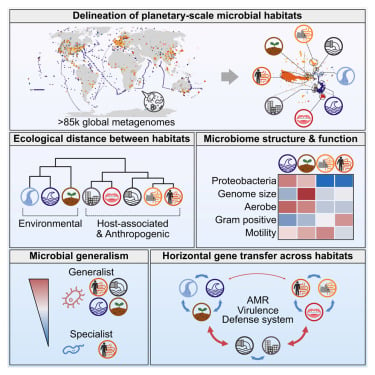
研究团队通过名为SPIRE的公开数据库,整合了来自世界各地85,604个宏基因组样本,精确识别出40种不同的微生物栖息地类型。这项研究不仅为我们描绘了微生物生态系统的宏伟蓝图,也为理解微生物如何在不同环境间传播、如何影响宿主健康提供了宝贵线索。深入了解这些“通才型”微生物及其基因转移机制,有望为我们开发针对感染性疾病、肠道疾病、甚至肿瘤的新型诊断和治疗策略开辟道路,例如通过调节特定微生物群落来改善免疫反应或药物疗效,开启个性化微生物组干预的新时代。
三、细胞精微结构:蛋白酶体储存颗粒的准晶体之谜
细胞内部并非一盘散沙,而是高度组织化的。除了线粒体、细胞核等有膜细胞器外,科学家们近年来还发现了许多没有膜的细胞器,例如应激颗粒和蛋白酶体储存颗粒(proteasome storage granules, PSG)。这些无膜细胞器在细胞内行使着重要的功能。一项发表在《Cell》上的最新研究,首次利用先进的冷冻电子断层扫描技术,清晰地定义了PSG中分子的详细结构,揭示了其准晶体结构。
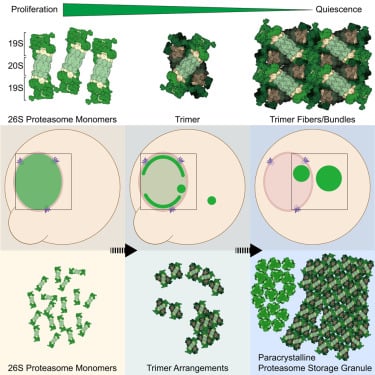
蛋白酶体是细胞内的“垃圾处理站”,负责降解异常或不再需要的蛋白质,对于维持细胞正常功能至关重要。PSG作为其储存颗粒,在细胞应激状态下可能起到保护或调控蛋白酶体活性的作用。通过与冷冻电子断层扫描领域的先驱Wolfgang Baumeister教授合作,研究人员得以在分子层面理解PSG的功能。这一突破性进展为深入探索细胞内无膜细胞器的结构与功能提供了关键工具和新视角。理解这些精微结构如何运作,对于揭示许多与蛋白质错误折叠、降解相关的疾病(如神经退行性疾病、某些癌症类型中蛋白质异常积累)的机制,乃至开发新的靶向治疗干预手段,都具有重要的基础意义。
四、修正教科书:DNA复制核心机制的意外发现
DNA复制是生命活动的基础,每次细胞分裂,都需要精确复制其整个基因组,确保每个子细胞都能继承一套完整的遗传物质。在这个复杂而精密的生物学过程中,聚合酶负责沿着DNA链快速移动,复制遗传密码。为了确保聚合酶不会在中途“脱轨”,一种环状的蛋白质夹子会将其牢牢拴在DNA上,而复制因子C(Replication Factor C, RFC)则被认为是负责将这个夹子扣紧的关键蛋白。这一认知在基础生物学教科书中已沿用数十年。
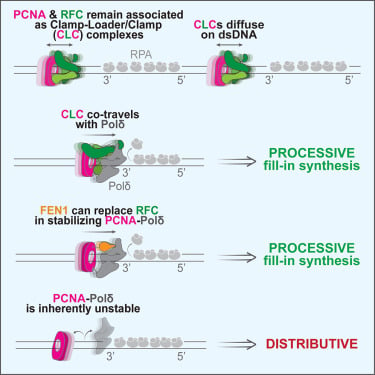
然而,《Cell》杂志上的一项最新研究颠覆了这一传统观念。研究团队发现,RFC的作用远不止于此。令人意外的是,即使在蛋白夹子加载到DNA上之后,RFC并不会立即离开,而是持续与其结合。更重要的是,RFC、蛋白夹子和聚合酶这三个单元会作为一个整体,协同沿着DNA滑动,共同确保DNA复制的快速和可靠性。这一发现深刻修正了我们对DNA复制核心机制的理解,揭示了细胞如何更高效、更精确地完成遗传物质的传递。由于DNA复制过程中的错误或异常与癌症(如肿瘤细胞的无限增殖)、神经系统疾病(如基因组不稳定性导致神经元功能障碍)等多种疾病的发生发展密切相关,这项基础研究的突破,有望为我们理解这些疾病的分子根源,乃至开发出更精准的靶向治疗策略,提供全新的理论基础。
五、胶质母细胞瘤新希望:单次溶瘤病毒注射的突破性疗效
胶质母细胞瘤是最常见、恶性程度最高的原发性脑肿瘤,患者预后极差,平均生存期短,治疗选择有限。传统的免疫疗法在其他癌症类型中取得了显著成功,但在胶质母细胞瘤中效果不佳,原因在于其“冷肿瘤”特性——即肿瘤微环境抑制了抗癌免疫细胞的浸润和活性,导致免疫细胞难以穿透到肿瘤深处。然而,一项发表在《Cell》杂志上的重磅研究,为这一困境带来了曙光。
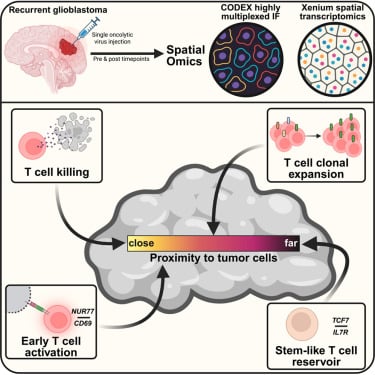
麻省总医院布莱根和丹娜-法伯癌症研究所的研究团队证明,通过单次注射溶瘤病毒(一种经过基因改造、能选择性感染并摧毁癌细胞的病毒),可以有效地招募免疫细胞穿透并持久存留在脑肿瘤深处。这种溶瘤病毒由单纯疱疹病毒改造而成,其基因被精确修改,使其只能在胶质母细胞瘤细胞中复制增殖,而对正常健康细胞无害。在针对41名复发性胶质母细胞瘤患者的I期临床试验中,溶瘤病毒治疗显著延长了患者的生存期,尤其是在那些预先存在病毒抗体的患者中效果更佳。
进一步的机制研究揭示,该疗法能够诱导免疫T细胞长期浸润到患者肿瘤中。研究人员发现,细胞毒性T细胞与濒死脑肿瘤细胞的距离越近,与患者治疗后更长的生存期呈现正相关。此外,该疗法还能扩大患者大脑中预先存在的T细胞库。这一发现表明,溶瘤病毒不仅能直接杀伤癌细胞,还能有效“加热”肿瘤微环境,克服了胶质母细胞瘤对传统免疫疗法的抵抗,为这种致命性脑肿瘤的治疗开辟了全新的途径。对于正面临胶质母细胞瘤挑战的患者而言,这项研究无疑带来了巨大的希望。面对复杂且前沿的抗癌药物信息,MedFind可以提供专业的药物信息咨询与AI辅助问诊服务,帮助患者更好地理解治疗方案,并协助构建跨境购药渠道,确保您能及时获取所需新药。
六、解码免疫通讯:细胞因子调控机制的新发现
免疫系统是人体健康的守护者,它通过复杂的分子网络与其他细胞类型进行交流,其中细胞因子扮演着至关重要的“信使”角色。这些小分子蛋白质在启动、协调和终止免疫反应,以及维持身体稳态方面发挥着多种重要功能。尽管科学家们对免疫细胞何时、为何以及如何产生和发送细胞因子已有深入了解,并基于此开发了许多重要的药物来对抗感染、癌症和自身免疫性疾病,但长期以来,一个核心问题始终未能得到解决:哪些细胞接收特定的细胞因子信号,以及它们在被召唤时如何响应?
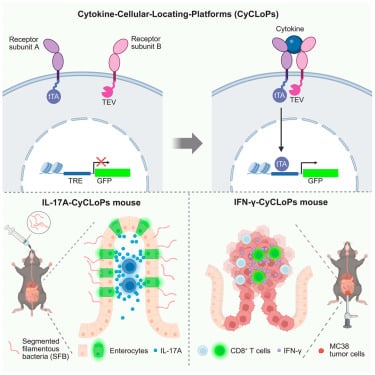
哈佛医学院和麻省理工学院的科学家们在《Cell》杂志上发表了一项突破性研究,他们创建了一个名为细胞因子细胞定位平台(cytokine cellular locating platforms, CyCLoPs)的新型工具家族,首次揭示了免疫系统如何使用细胞因子进行沟通的另一半图景。这个新工具能够让研究人员在特定条件下,精确标记出对特定细胞因子作出反应的细胞。理解免疫系统沟通的“发送方”和“接收方”全貌,对于全面掌握免疫反应的动态过程至关重要。这项研究的成功,无疑将为开发针对传染病、癌症、过敏和自身免疫性疾病的新一代药物提供变革性的视角和更精准的靶点,有望极大地提升现有免疫疗法的效果,实现更具针对性的免疫调节治疗。
七、胰腺癌的生存策略:肿瘤微环境决定其生长与耐药
胰腺癌以其高侵袭性和对传统化疗的顽固抵抗而闻名,是预后最差的恶性肿瘤之一。了解其独特的生存策略对于开发有效疗法至关重要。一项由纽约大学朗格尼医学中心领导的最新研究,发表在《Cell》杂志上,揭示了胰腺癌细胞所处微环境的一个关键特征——细胞外基质(extracellular matrix, ECM),即肿瘤周围由纤维蛋白和多糖等构成的复杂网络,如何决定癌细胞是快速生长还是对化疗产生耐药性。研究指出,胰腺癌细胞具备快速适应并在不同生物学反应之间切换的能力,这使其更难被清除。
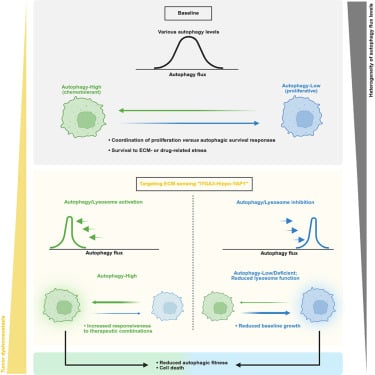
这项研究深入探讨了胰腺癌细胞如何调节其自噬水平。自噬是一种细胞“自我进食”的过程,癌细胞可以通过分解自身成分来获取营养以求生存。当自噬水平较高时,癌细胞会专注于生存而非分裂增殖,这使得它们能够抵抗旨在攻击快速分裂细胞的化疗药物。相反,当自噬水平较低时,细胞则会更快增殖。研究最关键的发现是,决定胰腺癌细胞是否提高自噬水平的一个主要因素,就是它们感知ECM的能力。那些未能检测到ECM、处于“未锚定”状态的癌细胞,会显著提高自噬水平以寻求生存。这一发现揭示了胰腺癌细胞如何利用肿瘤微环境的特性,灵活地切换其代谢策略来逃避治疗。它为开发针对胰腺癌的新型靶向药物和治疗方案提供了重要的理论依据,例如通过干扰癌细胞对ECM的感知或调控其自噬路径,有望增强化疗效果,打破胰腺癌的治疗僵局。
八、T细胞“增压器”:真菌来源燃料突破肿瘤内葡萄糖竞争
在实体瘤治疗中,CAR-T细胞等免疫疗法面临着一个巨大挑战:肿瘤微环境中的侵袭性癌细胞会“劫持”关键营养物质葡萄糖,导致前来攻击的T细胞因能量匮乏而功能受损,无法有效杀伤肿瘤细胞。这种葡萄糖竞争是实体瘤免疫治疗效果不佳的关键原因之一。一项发表在《Cell》杂志上的突破性研究,为这一难题提供了创新的解决方案。
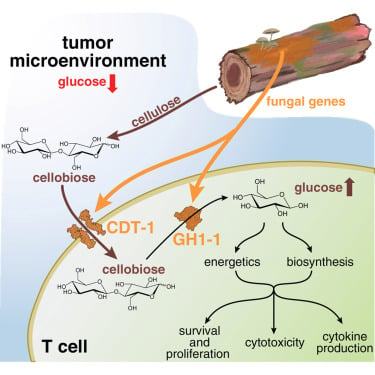
加州大学洛杉矶分校的研究团队找到了一种方法,可以用肿瘤无法窃取的燃料来源为免疫细胞“增压”。他们将目光投向了纤维二糖,一种存在于植物纤维中的天然糖。纤维二糖对人体无毒,并被美国食品药品监督管理局普遍认为是安全的,但人类细胞和肿瘤细胞都无法直接分解和利用它。然而,一些微生物和真菌却可以。基于此,研究人员巧妙地将两种源自真菌的蛋白质“武装”到T细胞上,使这些经过基因工程改造的T细胞能够导入纤维二糖,并在细胞内将其转化为可用的葡萄糖。在模拟肿瘤营养贫乏环境的实验室实验中,这些“增压”的T细胞表现出惊人的能力:它们不仅能持续存活、分裂,还能高效地产生抗癌细胞因子并有效杀死肿瘤细胞,而未经改造的T细胞则迅速失去功能。这项创新策略成功绕过了肿瘤内的葡萄糖竞争,为增强CAR-T及其他免疫疗法在实体瘤中的疗效开辟了全新路径,有望显著提高实体瘤患者的治疗成功率,让更多患者从免疫疗法中受益。
九、罕见病新希望:维生素B3疗法成功治疗致命儿童疾病
对于罕见遗传病患者而言,寻找有效疗法往往充满挑战。传统研究模式通常是从疾病入手寻找治疗方案,但格拉德斯通研究所的科学家们却逆向思维,采用了一种创新方法:他们从维生素入手,系统性地识别出可能受益于高剂量补充剂的遗传疾病。这项发表在《Cell》杂志上的研究,为一种名为NAXD缺乏症的毁灭性遗传疾病带来了前所未有的希望。
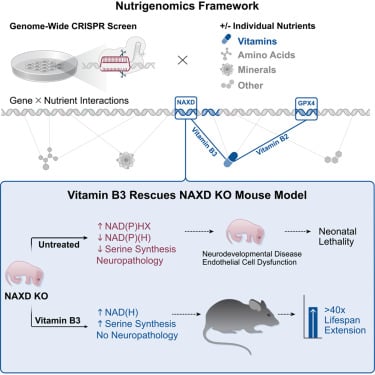
NAXD缺乏症是一种极其罕见且致命的儿童疾病,患儿通常在出生后的最初几个月内便会夭折,缺乏有效的治疗手段,给家庭带来沉重打击。研究团队利用其独特的“维生素生物学”框架,在新型小鼠模型中测试了维生素B3疗法。结果令人震惊:维生素B3补充剂不仅将患病小鼠的寿命延长了40多倍,还完全消除了疾病症状。这一戏剧性的成功为NAXD缺乏症患儿带来了生命的曙光。更重要的是,该研究还通过这一系统性方法,识别出其他几十种可能对维生素B2或维生素B3疗法有反应的遗传疾病,为利用安全、廉价的维生素补充剂治疗一系列罕见遗传病开辟了广阔的新途径,有望惠及全球无数受罕见病折磨的家庭,提供可及且有效的治疗方案。
十、惊人发现:癌症竟能“防御”阿尔茨海默病?
在医学界,癌症和阿尔茨海默病(AD)是两种最令人恐惧的诊断,但一个长期存在的流行病学现象是:它们很少同时发生在同一个人身上。多年来,科学家们注意到,癌症患者似乎更不容易患阿尔茨海默病,反之亦然,但其中的具体原因一直是个谜,引发了“生存竞争”等猜测。

近日,《Cell》杂志上的一项突破性研究给出了惊人答案:来自华中科技大学等机构的科学家发现,外周癌症并非仅仅通过“生存竞争”来减少AD的发生,而是会主动分泌一种名为胱抑素 C(Cyst-C)的蛋白质。这种蛋白质能够穿过血脑屏障,激活大脑中的免疫细胞——小胶质细胞表面的TREM2受体,从而精准降解与AD相关的β淀粉样蛋白(Aβ)斑块,为AD治疗开辟了全新的路径。
阿尔茨海默病的核心病理特征是β淀粉样蛋白寡聚体聚集形成的神经炎性斑块,特别是Aβ₁₋₄₂。这些斑块会严重破坏神经信号传递,引发胶质细胞活化,最终导致患者认知功能衰退。为验证癌症与AD的关联,研究团队在经典AD小鼠模型(5×FAD小鼠)体内植入多种肿瘤细胞(如Lewis肺癌、RM1前列腺癌、MC38结肠癌等)。结果显示,无论何种肿瘤,都在30天内显著抑制了小鼠脑内可溶性与不可溶性Aβ₁₋₄₂、Aβ₁₋₄₀的积累,皮层、丘脑、齿状回等关键脑区的Aβ斑块面积大幅缩小。更令人鼓舞的是,这些携带肿瘤的AD小鼠在认知测试中表现出明显的改善,空间记忆能力显著优于未携带肿瘤的对照组。
进一步的研究证实,这种保护效应并非来自肿瘤的物理负担,而是源于肿瘤分泌的蛋白质。通过蛋白质组学和转录组学分析,研究团队最终锁定了胱抑素 C。无论是癌症小鼠的血浆,还是肺癌、前列腺癌、乳腺癌等多种人类癌症患者的血液中,胱抑素 C的水平都显著升高。实验进一步证实,敲除肿瘤细胞的胱抑素 C编码基因(Cst3)后,肿瘤对AD小鼠的保护作用完全消失;而重新回补人源胱抑素 C,不仅能恢复Aβ斑块清除效果,还能拯救小鼠的认知缺陷。这项跨领域的突破性研究,不仅揭示了癌症与AD之间意想不到的生物学联系,更指明了通过调控胱抑素 C和TREM2通路来治疗阿尔茨海默病的全新方向,为全球数千万AD患者带来了新的希望,为未来新型药物研发提供了坚实基础。
结语:科技之光,照亮生命前程
2026年2月《Cell》杂志的这些研究成果,从基础生命科学到疾病治疗策略,无不展现了前沿科技的巨大潜力。无论是对病毒、细胞机制的深刻理解,还是在癌症、神经退行性疾病和罕见病领域的创新突破,都为人类健康带来了前所未有的希望。对于面临重大疾病挑战的患者和家庭而言,这些科研进展是宝贵的信息来源,理解它们有助于更好地规划未来治疗路径。MedFind致力于为患者提供最新、最专业的抗癌资讯、诊疗指南和药物信息。如果您对文中提及的任何前沿治疗方案感兴趣,或者正在寻找特定药物的跨境直邮渠道,请随时联系MedFind,我们专业的团队将为您提供个性化咨询服务,并利用AI辅助问诊,帮助您在全球范围内寻找最适合您的治疗方案,让您不再孤单面对,一同迎接治疗新曙光。