对于肝细胞癌(HCC)患者和家庭来说,每一次新药研发的突破,都像是一束穿透阴霾的阳光,带来了无尽的希望。近日,一种名为PLT012的创新型抗CD36单克隆抗体药物,获得了美国食品药品监督管理局(FDA)的快速通道认定,这无疑为全球肝细胞癌患者带来了令人振奋的消息。这项认定旨在加速针对严重疾病且存在巨大未满足医疗需求的疗法的开发和审查,意味着PLT012有望更快地抵达亟需治疗的患者身边。MedFind深知患者在抗癌路上的艰辛,我们致力于及时分享全球最新抗癌资讯、药物信息,并协助患者了解前沿治疗方案。
肝细胞癌(HCC)治疗面临的挑战与未满足的需求
肝细胞癌(HCC)是全球最常见且最具致命性的恶性肿瘤之一。在我国,肝细胞癌的发病率和死亡率更是居高不下,给无数家庭带来了沉重负担。这种癌症通常发生在慢性肝病和肝硬化背景下,而近年来越来越多的研究表明,代谢功能障碍相关脂肪性肝炎(MASH,此前称为非酒精性脂肪性肝炎NASH)也正在成为HCC发病的重要风险因素。尽管近年来肝细胞癌的治疗取得了显著进展,包括手术切除、肝移植、局部消融、介入治疗、靶向药物和免疫治疗等,但许多患者最终仍然会经历疾病进展。一旦一线和后续治疗方案用尽,可选择的治疗手段便会变得非常有限,这凸显了开发新型有效药物的紧迫性。
肝细胞癌的复杂性在于其高度异质性,以及肿瘤微环境(TME)的独特生物学特性。肝脏作为重要的代谢器官,其肿瘤微环境富含脂质,这不仅为肿瘤细胞的快速增殖提供了能量,也对免疫细胞的功能造成了抑制。因此,寻找能够有效干预这种复杂肿瘤微环境,并激活抗肿瘤免疫反应的新型疗法,成为了当前肝细胞癌治疗研究的焦点和突破口。
FDA快速通道与孤儿药认定:PLT012为何备受关注?
PLT012获得FDA的快速通道认定,并非偶然,而是基于其在解决肝细胞癌治疗困境上的巨大潜力。那么,FDA快速通道究竟意味着什么?
- 加速开发与审查: 获得快速通道资格的药物,能够享有与FDA更频繁的沟通机会,这意味着药物研发过程中遇到的问题可以更快地得到解决,从而加速整个开发进程。同时,这类药物还有资格获得优先审评或加速批准,这可能使治疗药物比常规审批流程更早地送达患者手中。对于肝细胞癌这种预后不佳、治疗选择有限的疾病来说,时间就是生命。
- 针对严重疾病与未满足需求: 快速通道旨在鼓励创新药物开发,以应对那些对患者生命构成严重威胁、且现有治疗方案不足的疾病。肝细胞癌无疑符合这一标准,PLT012的快速通道认定,正是FDA对其治疗潜力的认可。
除了快速通道认定,PLT012还获得了FDA授予的肝脏和肝内胆管癌的孤儿药认定。孤儿药认定是FDA为鼓励开发治疗罕见疾病的药物而设立的,通常提供研发税收抵免、上市后7年市场独占期等激励措施。这项认定进一步强调了PLT012在治疗这类相对罕见但同样预后不佳癌症类型中的重要性和潜力。
颠覆性机制:PLT012如何“重编程”肿瘤微环境?
与传统的免疫检查点抑制剂(如靶向PD-1/PD-L1或CTLA-4通路)不同,PLT012采取了一种全新的、更具创新性的策略——它聚焦于由脂肪酸受体CD36介导的“代谢检查点”。要理解PLT012的作用机制,我们首先需要了解肿瘤微环境与代谢的关系。
肿瘤微环境中的“代谢失衡”
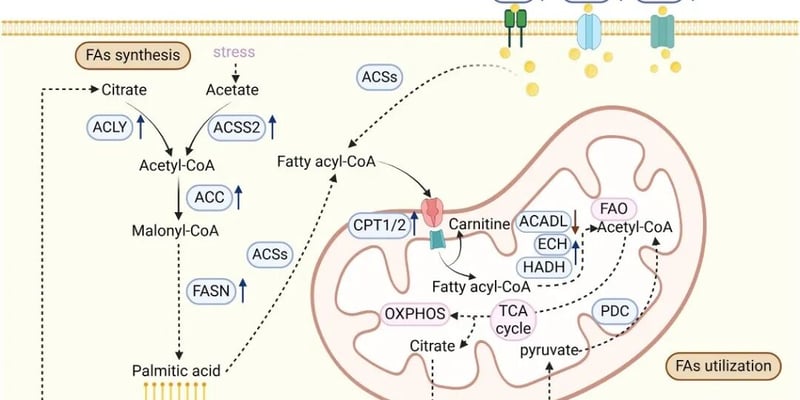
肝细胞癌的肿瘤微环境(TME)通常表现出高脂质水平,这是HCC的一个显著特征。癌细胞为了快速生长,会大量摄取和利用脂肪酸作为能量来源,甚至会诱导周围的基质细胞释放脂肪酸。这种高脂质环境不仅为肿瘤细胞提供了“燃料”,更重要的是,它对免疫细胞的功能产生了严重的负面影响。
- 免疫细胞的代谢耗竭: 在高脂质环境下,效应T细胞和自然杀伤(NK)细胞等抗肿瘤免疫细胞会因为持续暴露于过量的脂质而发生“代谢耗竭”。这意味着它们失去了正常的代谢功能,无法有效地产生能量,从而导致抗肿瘤活性下降甚至功能丧失。简单来说,它们“吃”得太多,反而“消化不良”,变得疲惫无力,无法有效识别和清除癌细胞。
- CD36的关键作用: CD36是一种在多种细胞(包括肿瘤细胞和免疫细胞)表面表达的脂肪酸转运蛋白。在HCC中,高水平的CD36被发现与肿瘤的进展密切相关。CD36如同一个“大胃王”,促进肿瘤细胞和某些免疫抑制细胞(如调节性T细胞和肿瘤相关巨噬细胞)大量摄取脂质。对于效应T细胞来说,CD36介导的脂质摄取会诱导其功能性耗竭,使其失去杀伤肿瘤细胞的能力。
PLT012的“代谢重编程”策略
PLT012作为一种人源化IgG4单克隆抗体,其作用机制正是通过选择性地阻断CD36介导的脂质摄取。通过中断这一关键过程,PLT012旨在实现“重编程”抗肿瘤免疫,从而促进更强的抗肿瘤活性:
- 恢复效应T细胞和NK细胞的活力: 当CD36被阻断后,肿瘤微环境中效应性CD8阳性T细胞和NK细胞对脂质的过度摄取被抑制,从而减轻了它们的代谢负担。这使得这些关键的抗肿瘤免疫细胞能够恢复其正常的代谢功能和效应器功能,重新获得识别和杀伤肿瘤细胞的能力。可以理解为,PLT012帮助这些“疲惫”的战士重新获得能量,拿起武器。
- 抑制免疫抑制细胞: 同时,调节性T细胞(Tregs)和促肿瘤巨噬细胞是肿瘤微环境中重要的免疫抑制细胞,它们同样依赖CD36介导的脂质代谢来维持其生存和抑制活性。PLT012阻断CD36,能够减少这些免疫抑制细胞对脂质的利用,从而抑制它们的生存和免疫抑制功能。这意味着,PLT012不仅增强了“好”的免疫细胞,还削弱了“坏”的免疫细胞,双管齐下,共同对抗肿瘤。
这种全新的作用机制,使得PLT012能够从“代谢根源”上干预肿瘤微环境,改变了传统的抗肿瘤免疫策略。它不仅仅是简单地解除免疫抑制,更像是对肿瘤微环境进行了一次“清理”和“重塑”,为免疫细胞创造一个更有利于发挥作用的环境,从而促进更强大的抗肿瘤反应。这种“代谢免疫疗法”的理念,为肝细胞癌的治疗开辟了一条崭新的道路。
临床前研究的曙光:PLT012单药与联合治疗潜力
在进入人体临床试验之前,任何新药都必须经过严格的临床前研究,以评估其安全性和初步疗效。PLT012在临床前模型中展示出了令人鼓舞的结果,这为其后续的临床开发奠定了坚实的基础:
- 强大的单药抗肿瘤活性: 临床前研究显示,作为单一药物,PLT012就表现出强大的抗肿瘤活性。这意味着即使不与其他药物联合使用,PLT012也有望单独发挥抑制肿瘤生长的作用。
- 与PD-1/PD-L1抑制剂的协同潜力: 更令人兴奋的是,研究还发现PLT012与PD-1/PD-L1抑制剂具有潜在的协同作用。这意味着在未来的临床实践中,PLT012可能与其他免疫检查点抑制剂联合使用,从而产生“1+1>2”的治疗效果,为患者带来更持久、更深度的缓解。这种联合疗法的策略,正是当前肿瘤治疗领域的一个重要发展方向,因为它有望克服单一疗法的耐药性和局限性。
这些积极的临床前数据,有力地支持了PLT012作为单药和联合疗法在肝细胞癌领域持续开发。它预示着PLT012不仅可能成为肝细胞癌治疗的新选择,更可能通过与其他药物的巧妙组合,为患者提供个性化且高效的治疗方案。
人类首项临床试验(NCT07337525):揭开PLT012的神秘面纱
在获得FDA的临床试验申请(IND)批准后(了解PLT012 IND获批详情),PLT012的首个人体I期临床试验(NCT07337525)已正式启动。这是一项至关重要的研究,旨在初步评估PLT012在人体内的表现。
I期临床试验设计详解
这项I期临床试验采用开放标签、剂量递增的设计。这意味着研究人员和患者都知道正在接受哪种药物治疗,并且会逐步增加药物剂量,以找到既安全又有效的最佳剂量。
- 主要研究目的: I期试验的核心目标是评估PLT012在成人晚期实体瘤患者中的安全性、耐受性以及药代动力学(即药物在体内如何被吸收、分布、代谢和排出)。同时,研究也会观察PLT012的初步疗效。
- 广泛的患者群体: 该试验计划招募患有多种晚期实体瘤的患者,并专门设置了一个针对肝细胞癌(HCC)的独立队列。这种设计能够帮助研究人员了解PLT012在不同类型肿瘤中的潜在活性。
- HCC患者的特定入组标准: 为了确保研究的严谨性,对于肝细胞癌患者,入组标准较为严格:患者必须具有Child-Pugh A级肝功能(Child-Pugh分级用于评估肝硬化患者的肝功能,A级代表肝功能良好,预后较好),并且在过去6个月内,不得有需要治疗性腹腔穿刺的腹水或需要药物干预的肝性脑病。这些标准旨在确保入组患者的肝功能相对稳定,能够更好地耐受试验药物,并减少肝功能不全可能带来的混杂因素。
- 治疗方案: 试验中的患者将通过静脉输注的方式,每3周接受一次PLT012治疗,直至疾病进展或出现不可耐受的毒性。
- 研究地点与人数: 该试验目前正在美国德克萨斯州的两个研究中心进行,预计将招募约36名患者。此外,研究还计划设立针对特定肿瘤类型的扩展队列,以进一步探索PLT012在不同癌症中的应用潜力。
I期试验的意义
I期试验是新药研发过程中的第一步,它的成功是药物能否继续开发的关键。虽然主要关注安全性,但如果能观察到初步的疗效信号,将为后续更大规模的II期和III期临床试验提供重要依据。对于肝细胞癌患者来说,参与I期试验意味着有机会接触到最前沿的创新疗法,但同时也需要充分理解其探索性和潜在风险。MedFind提醒您,任何新药在上市前都需要经过严格的临床验证,患者应在专业医生的指导下做出治疗选择。
肝细胞癌的未来展望:PLT012能否改变格局?
PLT012的出现,为肝细胞癌的治疗带来了多重维度的想象空间。
- 干预MASH-HCC连续体: Pilatus Biosciences的联合创始人Ping-Chih Ho博士指出,PLT012不仅有望重塑肿瘤微环境,更重要的是,它有望通过干预疾病的代谢根源,重新定义代谢功能障碍相关脂肪性肝炎(MASH)到肝细胞癌(HCC)的连续体治疗方法。这意味着PLT012不仅可能用于治疗已形成的肝细胞癌,甚至可能在MASH阶段进行干预,以预防疾病向肝癌进展,这将是肝癌预防和治疗领域的重大突破。
- 联合治疗的巨大潜力: 鉴于其独特的代谢重编程机制,PLT012与现有疗法(如PD-1/PD-L1抑制剂)联合使用的潜力巨大。未来的研究将探索最佳的联合方案,以期达到更优异的治疗效果和更持久的疾病控制。
- 新一代免疫疗法: PLT012代表了新一代免疫疗法的方向,即不再局限于经典的免疫检查点,而是通过调控肿瘤代谢来“武装”免疫系统,从而更有效地对抗肿瘤。这种多元化的治疗策略,有望克服当前免疫疗法面临的部分耐药性问题。
当然,从I期临床试验到最终获批上市,还有漫长的道路要走。但PLT012所展现出的创新机制和积极前景,无疑为全球肝细胞癌患者带来了新的希望。它提醒我们,科学的进步永无止境,每一次探索都可能为患者的生命带来转机。
MedFind温馨提示
面对复杂多变的癌症治疗信息,患者和家属往往感到迷茫和焦虑。MedFind致力于成为您抗癌路上的可靠伙伴。我们持续追踪全球抗癌药物研发的最新进展,深度解读各类创新疗法的作用机制、临床数据和潜在价值,力求将最前沿、最准确的医学信息以通俗易懂的方式呈现给您。
如果您正面临肝细胞癌或其他癌症的治疗困境,希望了解更多新药信息、诊疗指南,或者需要专业的AI辅助问诊服务,MedFind平台将竭诚为您提供支持。我们相信,通过科学的信息武装和专业的指导,每位患者都能做出最适合自己的治疗选择,勇敢地与病魔抗争。
参考文献
- 1. Pilatus Biosciences receives FDA fast track designation for metabolic checkpoint inhibitor PLT012 in hepatocellular carcinoma. News release. Pilatus Biosciences. February 19, 2026. Accessed February 19, 2026. https://tinyurl.com/yptd496n
- 2. Pilatus Biosciences Inc. receives orphan drug designation from FDA for PLT012 in treatment of liver and intrahepatic bile duct cancer. News release. Pilatus Biosciences. November 1, 2024. Accessed February 19, 2026. https://tinyurl.com/y56wtkvw
- 3. Luo X, Zheng E, Wei L, et al. The fatty acid receptor CD36 promotes HCC progression through activating Src/PI3K/AKT axis-dependent aerobic glycolysis. Cell Death Dis. 2021;12(4):328. Published 2021 Mar 26. doi:10.1038/s41419-021-03596-w
- 4. Tzeng SF, Yu YR, Park J, et al. PLT012, a humanized CD36-blocking antibody, is effective for unleashing antitumor immunity against liver cancer and liver metastasis. Cancer Disc. 2025;15(8):1676-1696. doi:10.1158/2159-8290.cd-24-1409
- 5. A first in human study of PLT012 in participants with solid tumor cancers. ClinicalTrials.gov. Updated February 18, 2026. Accessed February 19, 2026. https://clinicaltrials.gov/study/NCT07337525