宫颈癌,作为全球女性健康的重大威胁,其发病率和死亡率居高不下。据统计,2020年全球新增宫颈癌病例超过60万,死亡病例达34.2万。在中国,2022年预估新发病例高达15.07万,死亡病例约5.57万,且发病呈现年轻化趋势,农村地区尤为严峻。面对这一严峻挑战,医学界正不断探索更为精准、高效的治疗策略,其中靶向治疗和免疫治疗的崛起,为晚期宫颈癌患者带来了新的希望。然而,要实现这些先进疗法的最大效益,精准的生物标志物检测至关重要。本文将深入探讨宫颈癌靶向与免疫治疗中需要关注的关键生物标志物检测,并解析相关创新药物的应用,旨在为患者和家属提供全面、实用的抗癌资讯。
免疫治疗基石:PD-L1检测在宫颈癌中的核心价值
免疫检查点抑制剂(ICI)已成为晚期宫颈癌治疗的有效手段,而PD-L1表达作为预测患者从ICI治疗中获益的关键生物标志物,其检测价值日益凸显。荟萃分析数据显示,宫颈癌患者中PD-L1的总体阳性率高达58.1%,不同病理类型之间存在差异:鳞癌患者的阳性率最高,达到67.8%;腺癌患者相对较低,为36.6%;腺鳞癌和透明细胞癌的阳性率分别为48.4%和22.0%。这种较高的总体阳性率为免疫治疗在宫颈癌领域的广泛应用奠定了基础。
除了PD-L1,最新的诊疗指南,如2025年CSCO宫颈癌指南,还明确指出与ICI治疗相关的其他生物标志物包括微卫星不稳定性(MSI)、错配修复缺陷(MMR)以及肿瘤突变负荷高(TMB-H)。这些指标共同构成了评估患者是否适合免疫治疗的重要依据。
哪些免疫药物治疗前需检测PD-L1?
根据2025年CSCO宫颈癌指南,多种免疫药物在治疗前需要进行PD-L1检测以指导用药:
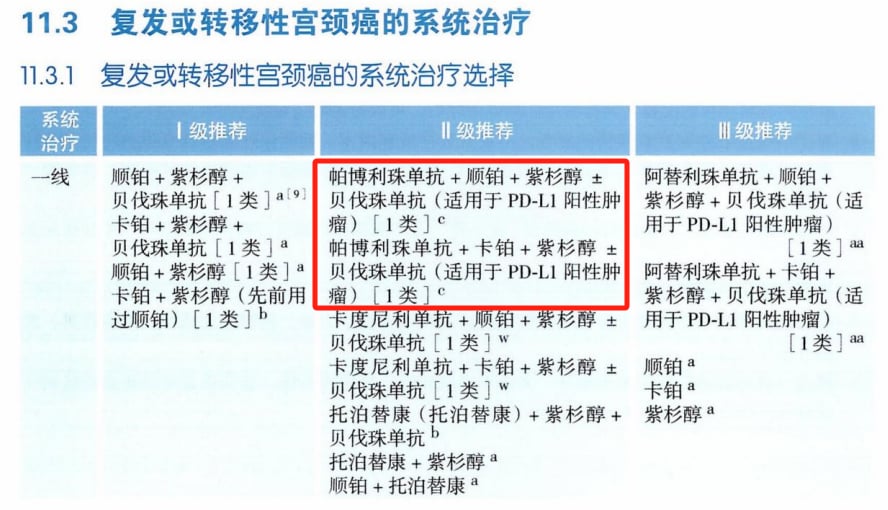
- 帕博利珠单抗(Pembrolizumab):作为一线治疗复发或转移性宫颈癌时,需PD-L1阳性(CPS≥1)方可联合铂类、紫杉醇±贝伐珠单抗。在二线及以上治疗中,PD-L1阳性、TMB-H或MSI-H/dMMR患者可单药使用。
- 纳武利尤单抗(Nivolumab):适用于PD-L1表达(CPS≥1)的复发、转移性宫颈癌的二线治疗。
- 恩朗苏拜单抗和赛帕利单抗:适用于既往接受含铂化疗失败的PD-L1阳性(CPS≥1)复发或转移性子宫颈癌患者。
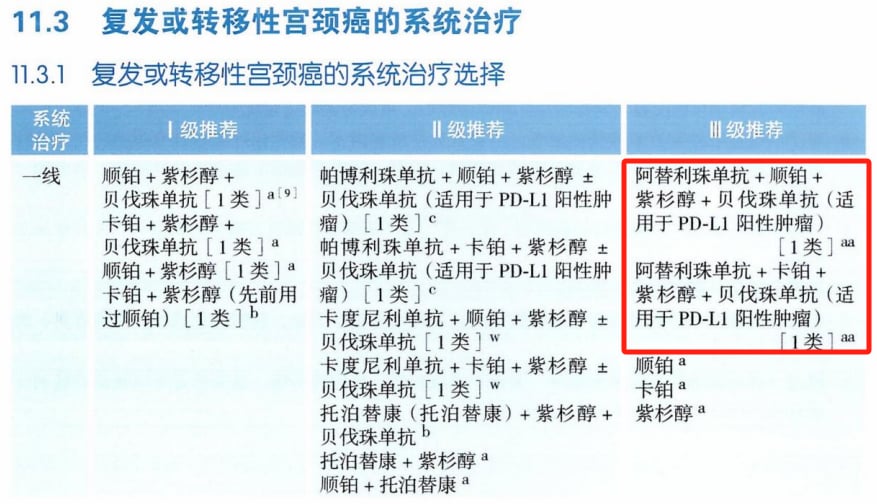
- 阿替利珠单抗(Atezolizumab):2025年CSCO宫颈癌指南新增,与铂类、紫杉醇+贝伐珠单抗联用于一线治疗时,仅适用于PD-L1阳性肿瘤患者。
这些详细的指南建议强调了PD-L1检测在宫颈癌免疫治疗决策中的核心地位。对于希望了解这些创新药物的患者,及时进行分子检测是迈向精准治疗的第一步。如果您对这些药物的获取途径、价格或海外购药流程有疑问,可以访问MedFind的药品代购与直邮服务,获取专业的购药指导。





HER2靶点:宫颈癌靶向治疗的新突破
HER2(人表皮生长因子受体2)作为ERBB家族的跨膜酪氨酸激酶受体,在细胞增殖、分化与存活中扮演着关键角色。其异常变异,包括过表达、扩增及突变,在多种实体瘤中被证实与肿瘤的发生发展及预后密切相关,如乳腺癌和胃癌。近年来,HER2在宫颈癌中的重要临床价值也逐渐被揭示,为宫颈癌的靶向治疗开辟了新途径。
德曲妥珠单抗:HER2阳性宫颈癌的希望之光
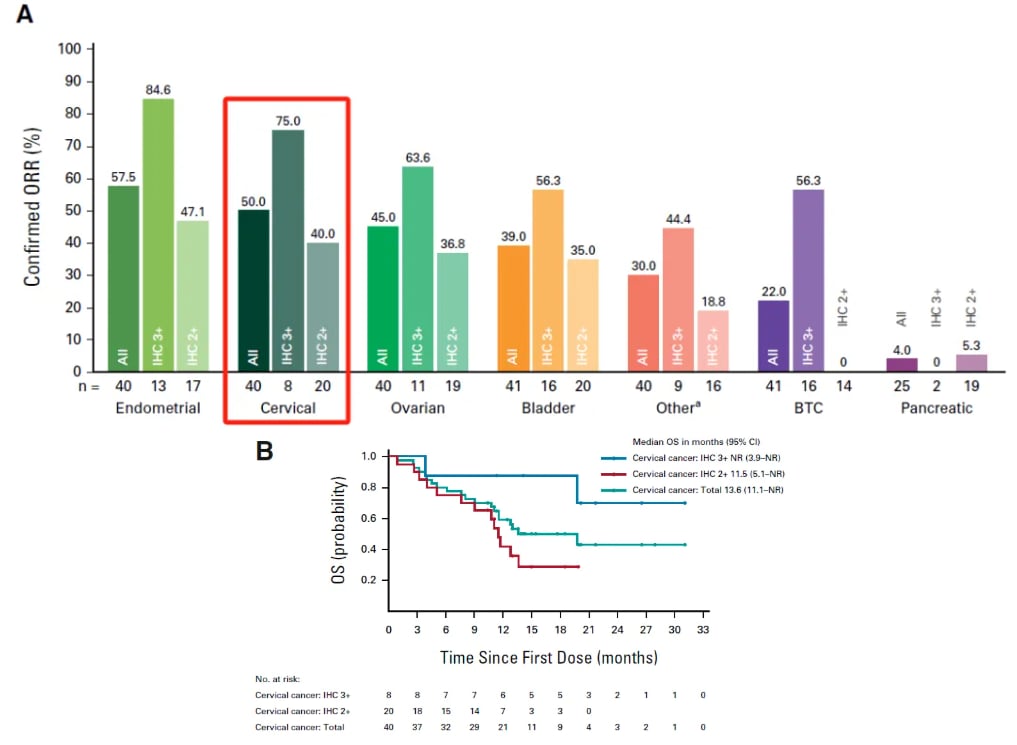
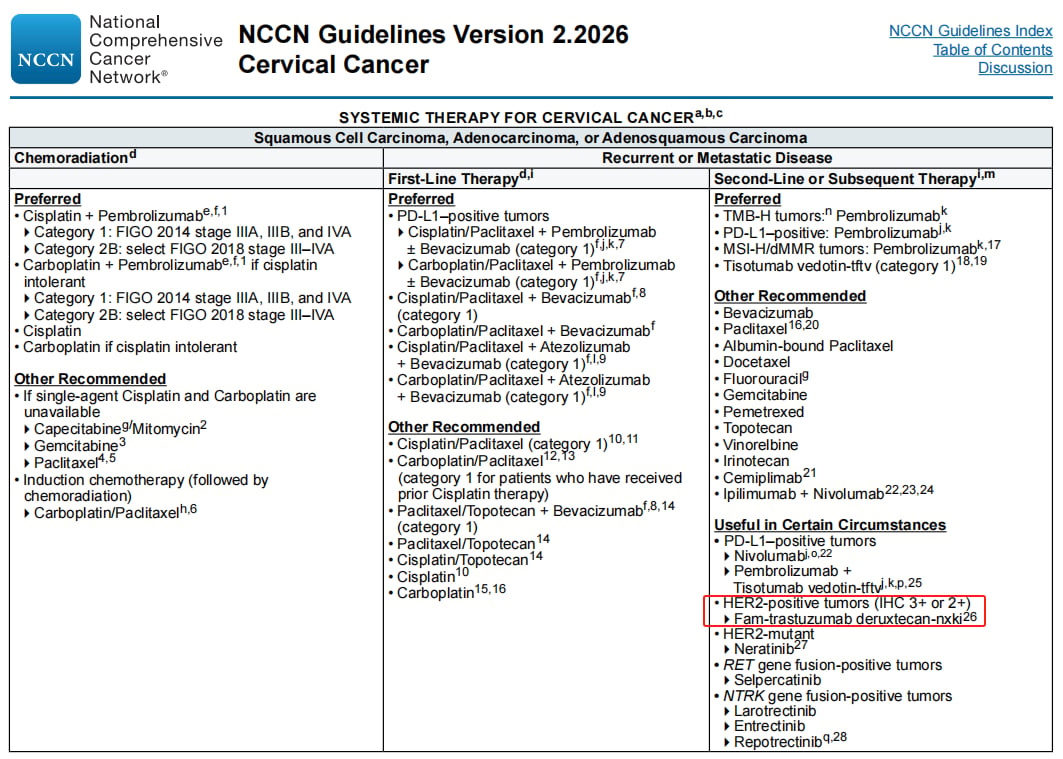
HER2阳性宫颈癌的靶向治疗已取得突破性进展,其中德曲妥珠单抗(Trastuzumab deruxtecan)的应用尤为关键。这款创新的抗体药物偶联物(ADC)以曲妥珠单抗为靶向载体,精准地将拓扑异构酶抑制剂递送至癌细胞内部,实现“精准打击”。2024年4月,FDA加速批准德曲妥珠单抗用于经系统性治疗后进展的HER2阳性(IHC3+)实体瘤,其中就包括宫颈癌。DESTINY-PanTumor02研究的宫颈癌队列数据显示,整体客观缓解率(ORR)达到50%,而HER2 IHC3+亚组的ORR更是高达75%,充分彰显了HER2检测在指导德曲妥珠单抗用药中的重要性。
因此,国内外权威指南均推荐晚期宫颈癌患者进行HER2检测。对于HER2阳性(IHC3+或2+)的患者,可积极考虑德曲妥珠单抗治疗。此外,NCCN指南明确指出,HER2扩增/过表达的宫颈癌患者往往面临更高的复发风险和更差的预后,这进一步凸显了HER2检测的必要性。
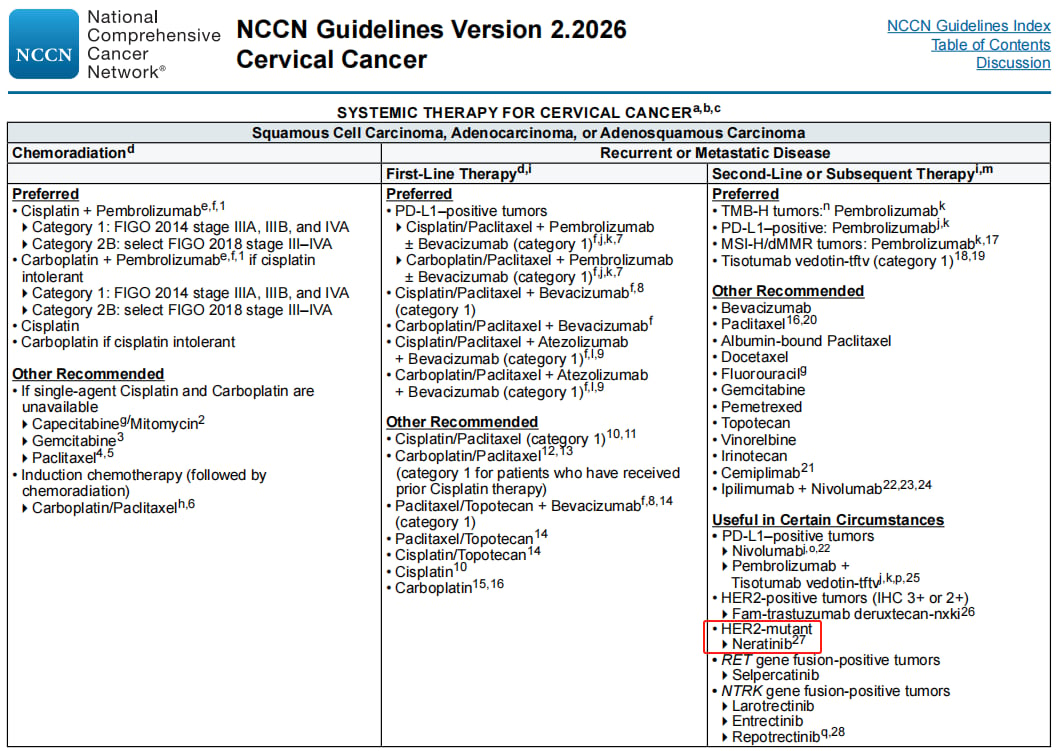
HER2突变:奈拉替尼的治疗潜力
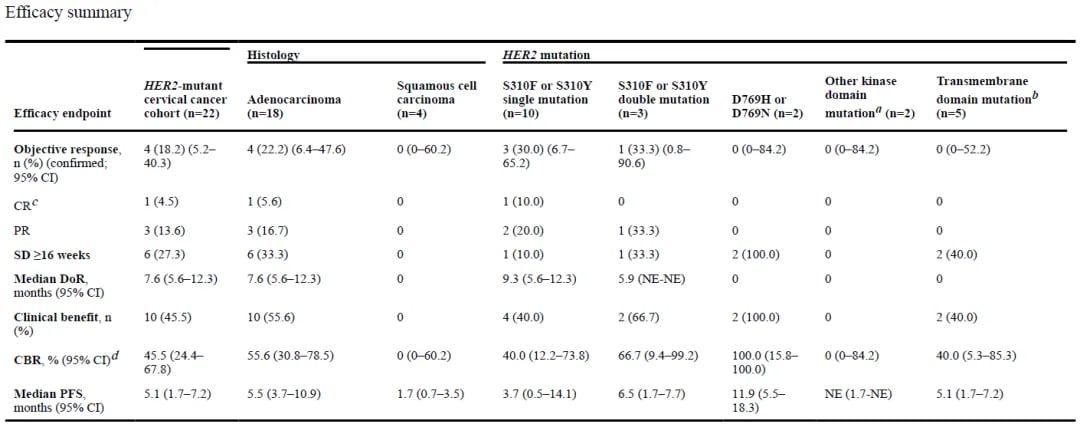
除了HER2的扩增/过表达,HER2突变同样值得重点关注。权威指南推荐此类患者检测该靶点以指导奈拉替尼(Neratinib)治疗。II期SUMMIT篮子试验中,18例HER2突变宫颈内膜腺癌患者接受奈拉替尼治疗后,客观缓解率(ORR)达到18.2%,其中6例患者疾病稳定持续时间超过16周,中位缓解持续时间(DoR)为7.6个月,为这部分患者带来了新的治疗希望。对于寻求这些创新靶向药物的患者,了解其适应症和获取途径至关重要。MedFind致力于为癌症患者提供全球范围内的药品代购和直邮服务,帮助患者更便捷地获取所需的治疗药物。




新型ADC靶点:宫颈癌治疗的未来方向
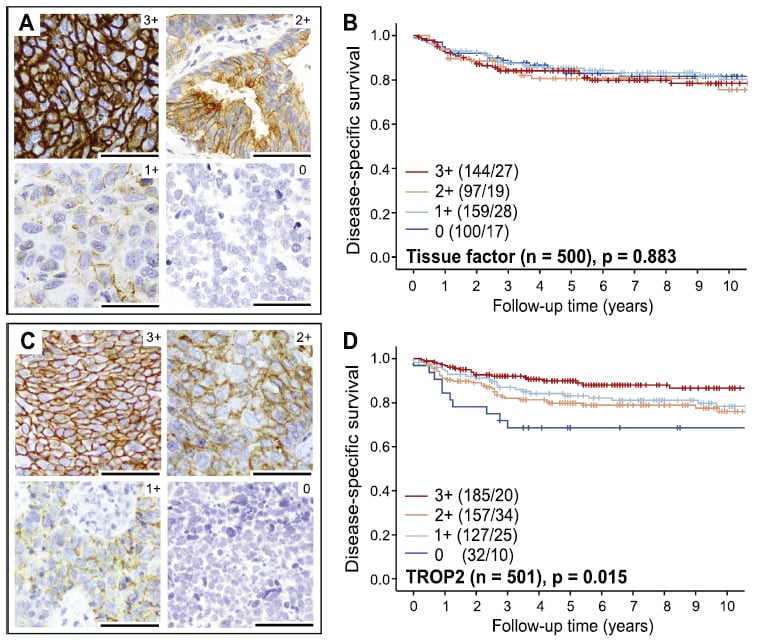
在宫颈癌靶向治疗领域,除了HER2,还有三大新型抗体药物偶联物(ADC)靶点正成为研究热点,它们凭借明确的表达特征和巨大的潜在治疗价值,为难治性宫颈癌患者带来了新的希望。这些靶点包括组织因子(TF)、滋养层细胞表面抗原2(TROP2)以及Nectin-4。
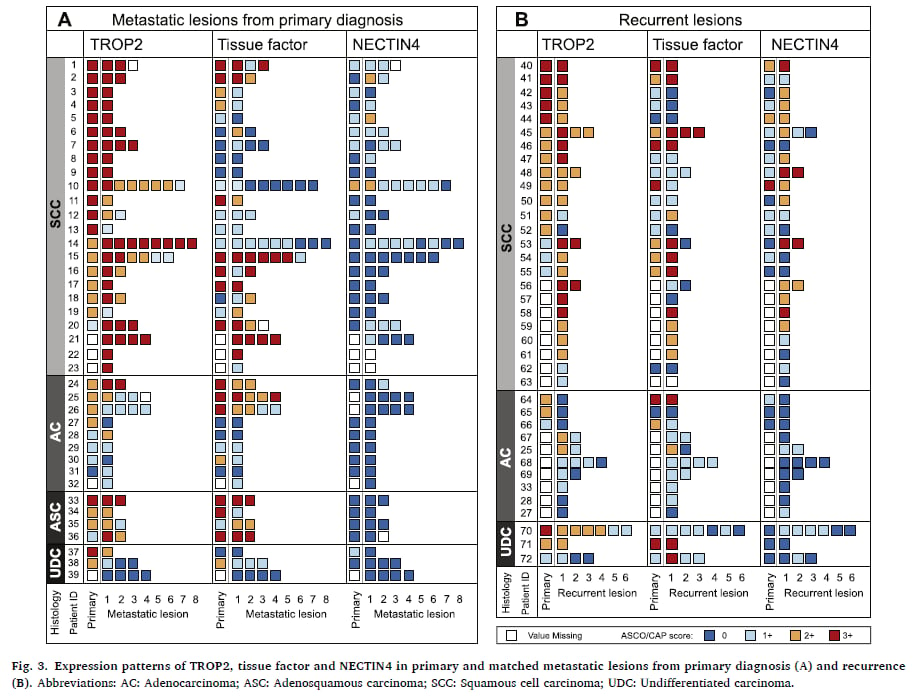
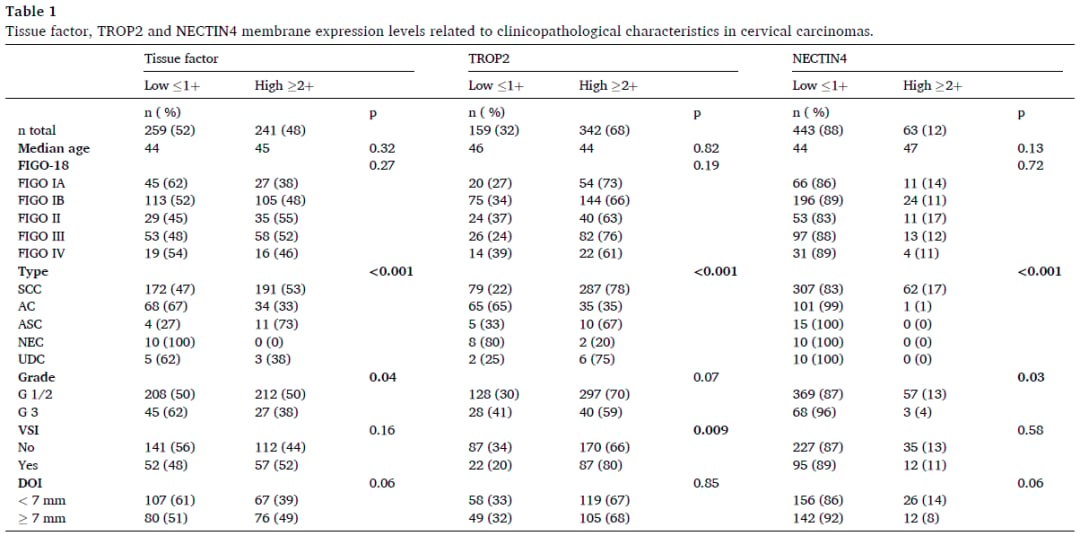
一项针对522个原发灶和194个转移灶宫颈癌样本的免疫组化(IHC)检测显示,TF、TROP2和Nectin-4的膜表达强阳性(3+)比例分别为29%、37%和4%,高表达(≥2+)比例分别达到48%、68%和12%。其中,TF和TROP2在原发、转移及复发病灶中均表现出稳定的高表达,而Nectin-4则在复发病灶中的表达率更高。在病理类型方面,鳞状细胞癌中这三个靶点均高表达,腺鳞癌中则以TF和TROP2高表达为主,这些发现为精准用药提供了重要的生物学依据。
靶向TF、Nectin-4、TROP2的创新ADC药物
针对这些新型靶点,药物研发已取得阶段性突破:
- 靶向TF的维替索妥尤单抗(Tisotumab vedotin,TV):作为首创的ADC药物,已获得FDA常规批准,用于治疗化疗期间或化疗后疾病进展的复发性或转移性宫颈癌。
- 靶向Nectin-4的9MW2821(Bulumtatug fuvedotin):凭借其突出的治疗潜力,已获得FDA“快速通道认定”,适用于既往接受过含铂化疗方案治疗失败的复发或转移性宫颈癌。
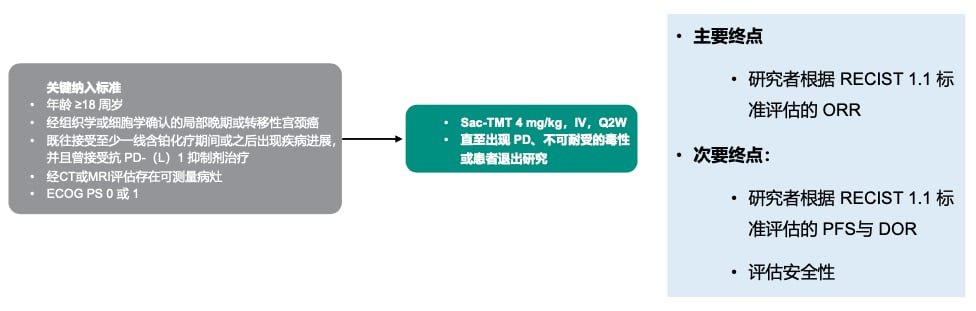
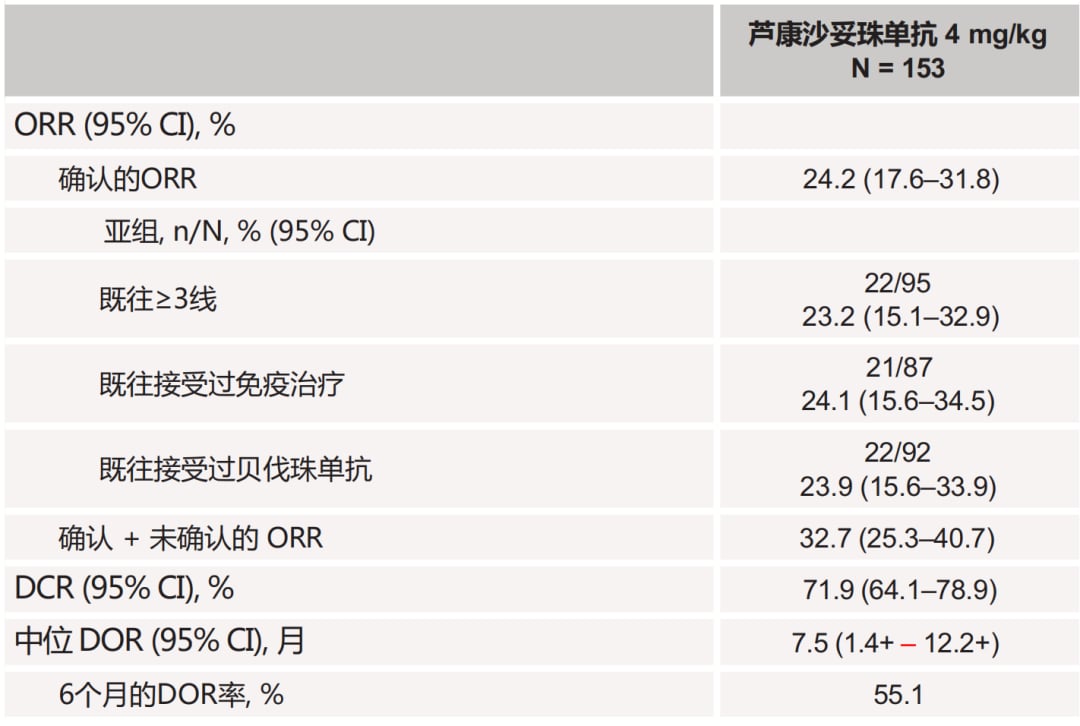
- TROP2靶向药物芦康沙妥珠单抗(Sacituzumab govitecan):其I/II期研究的最新数据在2025年ESMO大会上公布。该研究共纳入153例既往接受过至少一线含铂化疗期间或之后出现疾病进展,且接受过抗PD-(L)1抑制剂治疗的复发/转移性宫颈癌患者,确认客观缓解率(ORR)达到24.2%,为患者带来了新的治疗选择。
这些新型ADC药物的出现,极大地丰富了宫颈癌的治疗选择。对于面临治疗瓶颈的患者,了解这些前沿疗法并进行相应的分子检测,是寻找突破的关键。MedFind提供全面的抗癌资讯,帮助患者了解最新的药物信息和诊疗指南,并通过AI问诊服务,为患者提供个性化的治疗建议。
特殊亚型宫颈癌的分子检测策略
宫颈癌并非单一疾病,其包含多种组织学亚型,其中一些罕见亚型具有独特的生物学行为和治疗挑战。针对这些特殊亚型,精准的分子检测更是指导靶向免疫治疗的关键。
子宫颈神经内分泌癌(NECC):罕见而凶险的挑战
子宫颈神经内分泌癌(NECC)是一种极为罕见的宫颈癌亚型,仅占所有宫颈恶性肿瘤的0.9%-1.5%,其中子宫颈小细胞神经内分泌癌(SCNECC)占比高达87%。尽管发病率低,但NECC具有极强的侵袭性,发病年龄早,即使早期积极治疗也易出现广泛转移,预后极差,平均总生存期(OS)仅为40个月,5年总生存率仅34%。因此,在精准分子检测指导下的靶向免疫治疗对于改善NECC患者预后至关重要。
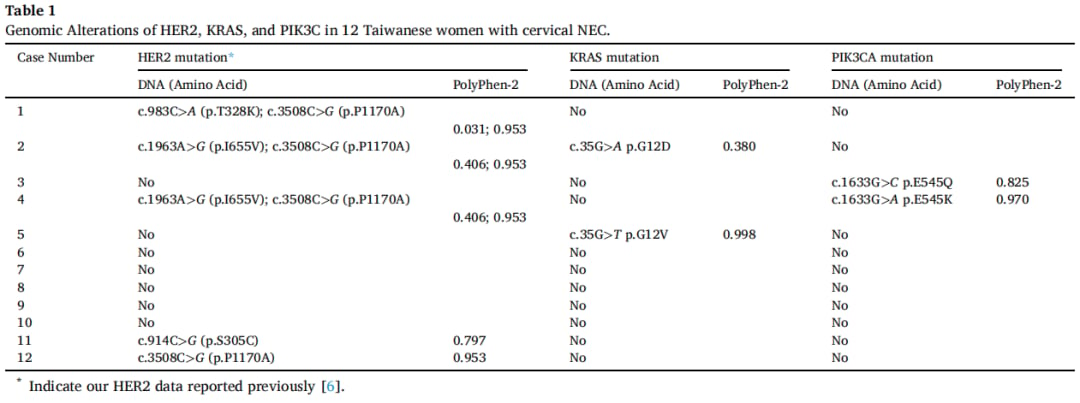
研究发现,约半数SCNECC患者存在至少一个驱动突变,主要集中在RTK/RAS、PI3K/AKT/mTOR、TP53/BRCA等信号通路以及PTEN、MAPK、MYC基因。一项针对12例晚期NECC的二代测序(NGS)检测显示,HER2突变发生率为41.67%,KRAS和PIK3CA突变发生率均为16.67%。此外,该研究还发现HER2/KRAS共突变和HER2/PIK3CA共突变的发生率均为8.3%,这提示多靶点疗法或双通路抑制剂可能提高疗效。
免疫相关标志物检测在NECC中同样具有重要意义。约70%的SCNECC表现为局灶性PD-L1阳性,33%存在dMMR。根据《子宫颈神经内分泌癌诊治专家共识(2025版)》,PD-L1阳性、MSI-H或TMB-H患者可考虑免疫检查点抑制剂单药或联合抗CTLA-4抑制剂治疗;而BRCA1/2突变或同源重组修复缺陷(HRD)患者则可尝试PARP抑制剂。综上所述,对于NECC患者,推荐进行多分子检测,并在多学科团队的指导下,结合患者的分子特征、临床分期及耐受性,制定个体化治疗方案,以期优化治疗效果并减少不良反应。



子宫颈透明细胞癌(CCAC):精准检测指引治疗方向
子宫颈透明细胞癌(CCAC)是宫颈癌中另一种相对罕见的类型,约占所有子宫颈腺癌的4%-9%。CCAC的发病年龄呈现“年轻女性”与“绝经后女性”的双峰特征。例如,宫内己烯雌酚(DES)暴露者约80%在15-31岁发病,多累及宫颈外部及阴道前上部,5年生存率约86.1%;而非DES暴露者多为65-80岁,以宫颈内膜受累为主,5年生存率约81.2%。
《子宫颈透明细胞癌诊治指南(2024年版)》明确推荐:CCAC患者在关注免疫治疗时,可进行PD-L1、dMMR/MSI-H或TMB-H检测;而靶向治疗则应重点检测HER2、TROP2、Claudin18.2,以及RET、NTRK融合基因。这些全面的分子检测能够为患者提供更精准的治疗方向。
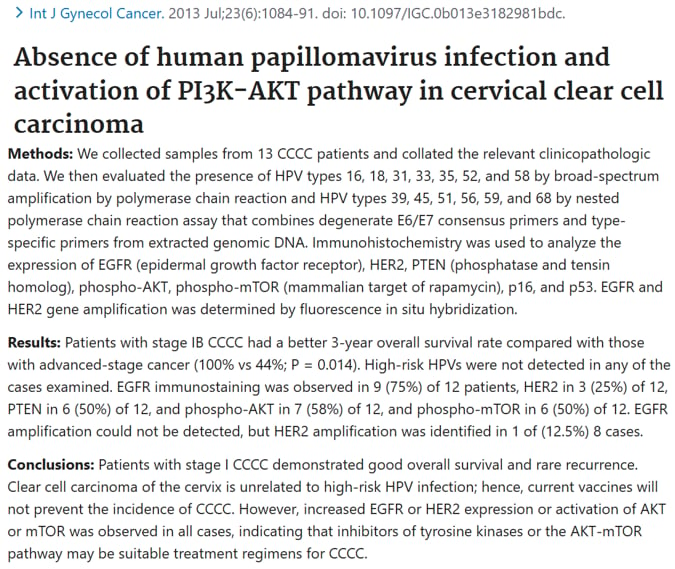
此外,研究还揭示了更多潜在的靶点:EGFR-PI3K-AKT-mTOR通路被发现参与CCAC的癌变过程,提示酪氨酸激酶抑制剂和mTOR抑制剂可能成为新的治疗方向。同时,14%的CCAC存在p53突变,18%存在PTEN突变。在条件允许的情况下,这些基因突变也应纳入检测范围,以便全面评估治疗潜力,为患者提供真正个体化的诊疗方案。对于这些复杂且罕见的癌症类型,获取最新的诊疗信息和专业的医疗咨询至关重要。MedFind的抗癌资讯平台和AI问诊服务,能帮助患者更好地理解病情,并探索适合自己的治疗路径。



结语:精准检测,开启宫颈癌治疗新纪元
随着分子生物学和基因测序技术的飞速发展,宫颈癌的治疗已从传统的“一刀切”模式,逐步迈向以患者分子特征为导向的精准医疗时代。无论是PD-L1在免疫治疗中的指导作用,HER2在靶向ADC药物中的突破,还是TF、TROP2、Nectin-4等新型靶点的涌现,都深刻改变了宫颈癌的治疗格局。对于子宫颈神经内分泌癌和透明细胞癌等特殊亚型,多分子检测更是制定个体化治疗方案、改善患者预后的关键。
对于广大宫颈癌患者而言,了解自身的分子特征,积极与医生沟通,选择最适合的靶向或免疫治疗方案至关重要。然而,许多创新药物和先进检测技术可能在国内尚未普及或价格昂贵。MedFind致力于为全球癌症患者提供便捷、可靠的药品代购与直邮服务,帮助患者跨越地域限制,获取所需的海外新药。同时,我们还提供专业的AI问诊服务和丰富的抗癌资讯,旨在为每一位患者提供全方位的支持,共同对抗癌症,重获健康与希望。